周末抽空听了一下大俊总在2024JP摩根的演讲,这里记录下一些没有出现在PPT里的信息和一些简单的理解,有哪些地方漏掉或者不正确,欢迎大家指正。
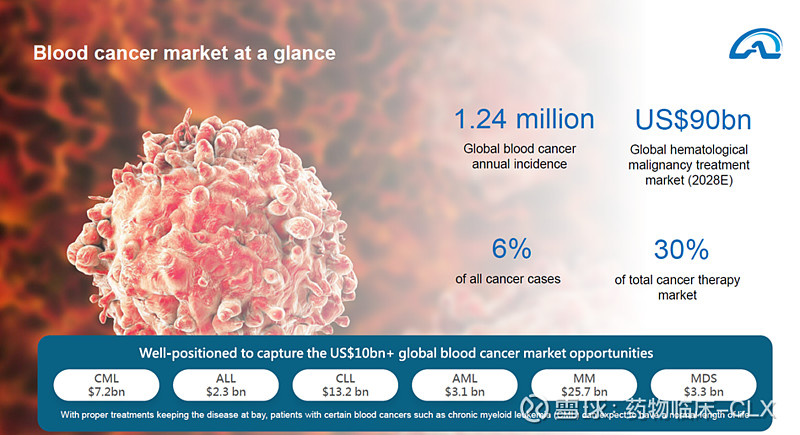
第4页:很多人说奥雷巴替尼的适应症人群很小,潜力有限。杨总说了血液瘤人群确实很小(发病率6%),但是市场非常大(肿瘤领域占30%销售)。有些人可能没有明白,这里就提一下,血液瘤人群很多都是长期带瘤生存(五年甚至十年),且需要一直吃药维持带瘤生存,所以治疗的人群能够不断富集(假如每年新增1000个患者用药,每年退出治疗10%,五年以后在用药的人群就有(第一年的500 + 第二年的600 + 第三年的700 + 第四年的800 + 第五年的900)=3500个患者,这还是每年新增不变的情况下,所以不能简单的说适应症人群很小,市场就大不了。
第5页:值得骄傲的几件事事,第一以非常好的价格续约医保,第二是奥雷巴替尼获得了CDE的完全批准,扩大了适应症人群;第三,Lisaftoclax已公开的3个注册研究,另外还有会前不久Lisaftoclax刚刚被CDE获批AML全球注册研究。还提到亚盛的优势(差异化)是所有管线都有全球的权益以及很多试验在全球范围内开展(国内很多BIOTECH是没有全球范围内开展试验的能力的)(very good price covered by NRDL; full approval for the resistant CML, not just limited to the mutation; news to this meeting: clearance by CDE for AML global registration study; pipeline all have global rights, conduct the trial not only China but US and global (differentiation) )
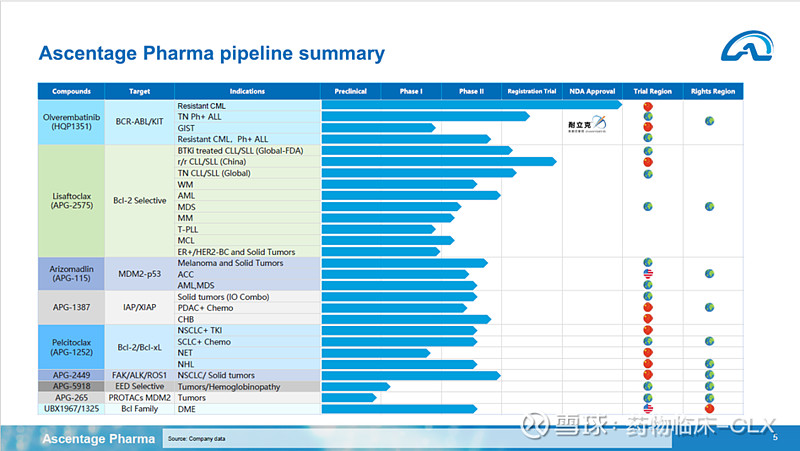
第六页: 强调项目最终拿到FDA的批准开展注册研究是没那么容易的。(project ultimum? is not that easy to get the FDA clearance for the global registration study)

第7页:仅仅是CML这个疾病,两个二代TKI抑制剂在过去三年的年销售额达到40亿美金;作为Veneclax后第二个进入临床和注册临床的BCL2,基于将于发生的NDA和开展的注册研究,预期它将是全球范围内第二款上市的BCL2抑制剂,另外还提到得益于最佳的无化疗联合靶向治疗,Lisaftoclax 国际III期试验入组很快(CML alone, two of second generation TKI generate 4 bn US$ for the last three years; Lisaftoclax, the second one to Venetoclax enter to clinical trial and registration trial, I think with NDA filing and other global registration studies, we anticipate to be the second enter the market globally. very fast enrolment benefit patients with best combination to target agent, chemo-free

第9/10页:提到奥雷巴替尼刚刚在NCCN里被列为潜在治疗选择,让奥雷巴替尼在全球CML治疗领域得到了更多的关注和认可。此外,还提到了奥雷巴替尼美国注册研究的沟通进展,用词是waiting for the clearance,意思应该是最终方案交了正在等回复?,基于已有美国临床试验的数据,获批没啥问题。预期一两个月能有结果?we have a more recognition of Olverembatinib in the global CML community; we have great discussion with FDA about the global registration studies; I think we have agreed most of the global registration study design, of course, we’re waiting for the final clearance which we don’t think there is any problem, as we have very strong data in US study.


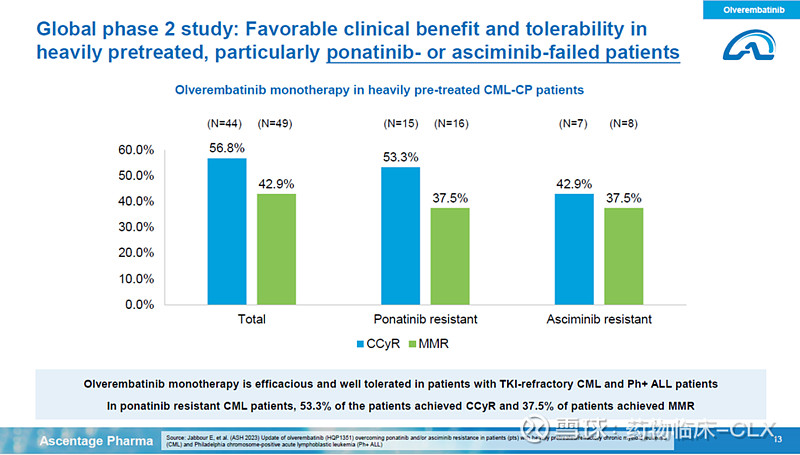
第13页:数据说明了我们的产品是3G TKI里全球最好的(Strong evident that our drug is truly the best in class globally)
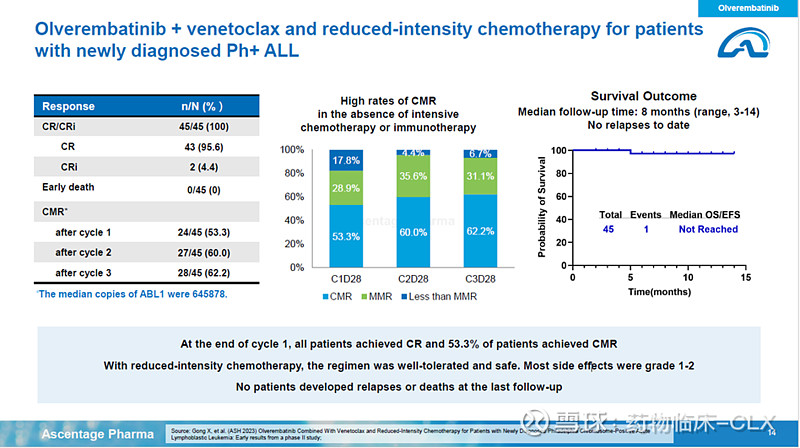
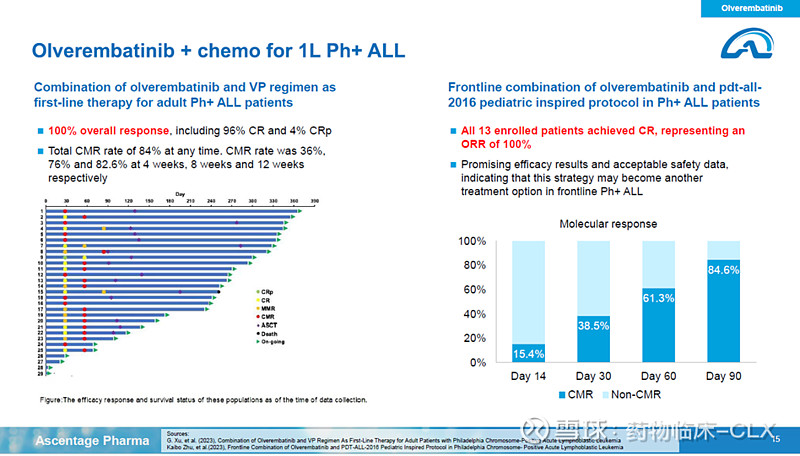
第14/15页:优异的数据也是得到CDE认可开展Ph+ ALL注册研究的基础;而且患者很快能达到深度的缓解(解读: 越快越深的缓解代表越好的获益)(that is the base for our clearance by CDE for the first line Ph+ ALL; achieve response very rapidly, especially deeply response (CMR) very high)
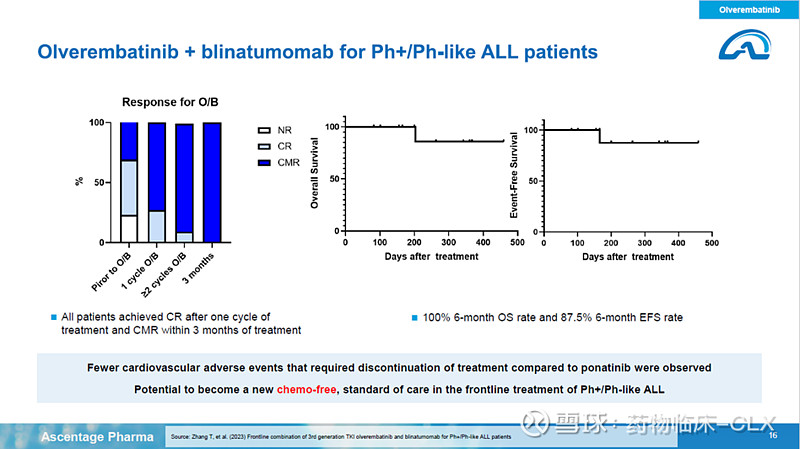
第16页:我们最终的目标是无化疗达到可持续的缓解并且无需进行移植,患者如果无需移植就能够长期存活,那无疑是巨大的获益。Our goal moving chemo-free, more durable response, I think eventual goal for ALL is chemo free and also transplant free, if ALL patient can survive without the transplantation, that will be huge benefit for the patient globally.
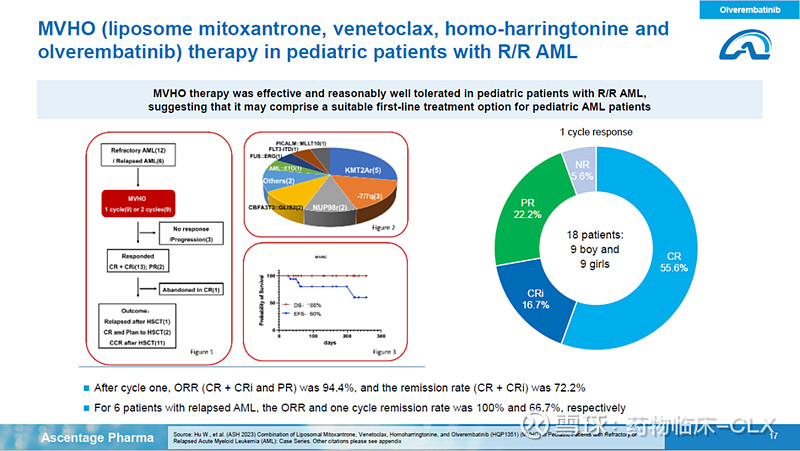
第17页:奥雷巴替尼具有多机制的抑制剂,能够显著抑制FLT3(这个没听懂),与维奈克拉,未来与APG-2575联用用于治疗AML。总体来说,基于已有的疗效和安全性数据,尤其是普纳替尼或阿西米尼或两者都耐药的患者都能达到深度且广泛的缓解,我们认为奥雷巴替尼的是3代TKI里最好的一个。(Our drug is multi-mechanism inhibitors and also potently inhibit FLT3?; with Venetolax, in the future, 2575 to treat the AML; Overall, we consider our Ovlerembatinib is globally best in class of 3G TKI in term of efficacy and safety, more importantly with patient who failed either Ponatinib or Acinimib or both, still see very deep and broad response)
第19页:再次提到Lisaftoclax的国际III期,1.5线被公司认可并进行宣传 @雨霖冰 @flcq (With FDA clearance, very smart design in the face of CLL landscape and competition, we call this simply the 1.5 line treatment, because we take the patients who doesn’t achieve best response of single agent of BTKi, and then ADDON to our drug. We already know all of clinical data, this is the best combination of CLL patients)
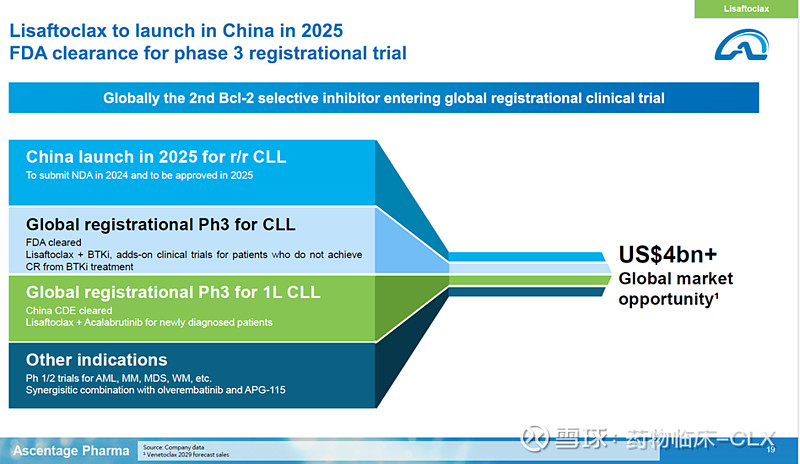
第20页:这里我还是有个疑问,尽管TLS的风险非常低,是否有必要采取跟百济11417一样设计,先BTKi抑制剂治疗几个周期再引入APG-2575彻底消除TLS风险。@flcq
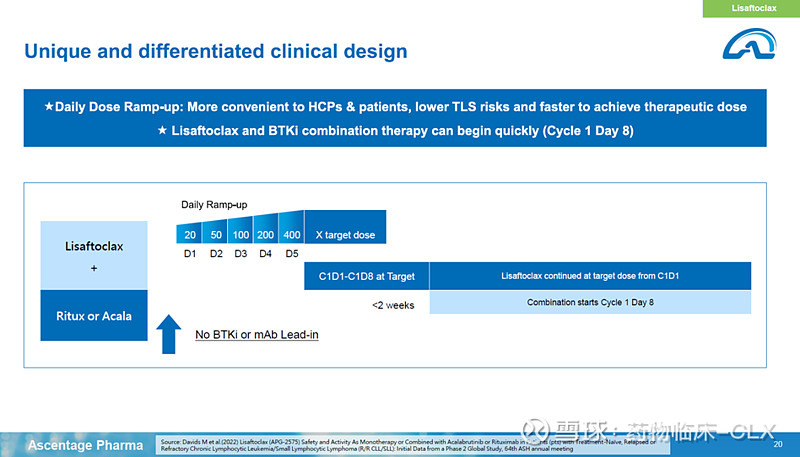
第21页:APG-2575在重度治疗过的CLL人群与维奈克拉当时试验的人群相似,也得到了跟维奈克拉接近或相似的疗效,但是在给药方面对患者是非常友好的。(解读:有很多人认为单纯的安全性和给药便利前景不大,这里举一个大家熟悉的例子,阿卡替尼当时头对头伊布替尼的时候也是疗效的非劣,但是展现更优秀的安全性,因为病人更好更容易管理,所以医生就更愿意开处方,阿卡替尼自2017年上市,今年销售额已经超过20亿美金)If you looked at the CLL population, it’s very similar to Venetoclax, if you looked the PFS and also MRD, is very close a similar with Venetoclax. More importantly, that is our key differentiation, our design is patient friendly.
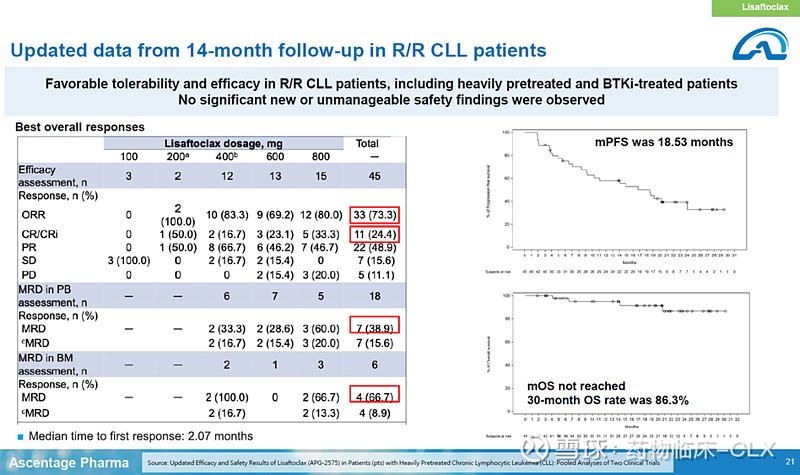
第23页:提到了在Lisaftoclax比维奈克拉有更好的安全性,尤其是Neutropenia。并且说了右侧部分安全性数据来自于已经入组的800例患者包括400多例CLL患者。TLS发生率确实非常低(If you look at the Grade 3 or 4 AE, especially Neutropenia, is much less than Venetoclax。With over 800 patients treated with this drug in last five years, 400 subjects in CLL)
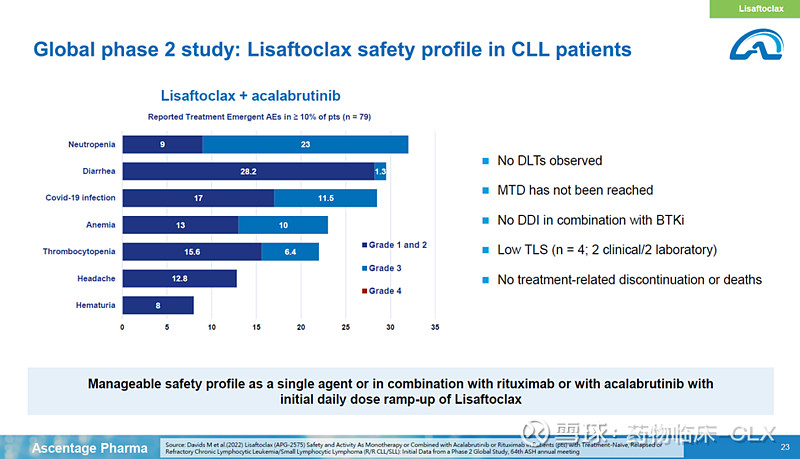
最后说亚盛将会是一个全球化的BIOTECH公司,三年后能够有全球的销售并成为一个真正的制药公司并且靠自己的产品收入产生盈利(我没理解错吧)。然后提到目前的开发策略,单药先搞定CML/CLL,联合用药搞定AML/ALL,最后搞定MDS/MM。大家可以轻易的看出我们在全球领先位置的这种巨大潜力。很多人总是问我要指引,我觉得自信和数据就是最好的指引,我们也已经在全世界范围内耕耘研发了15年,在港交所上市4年来,我认为,也是显而易见的,亚盛有非常大的潜力成为血液瘤领域全球巨头,目前被极大的低估。谢谢大家啊!Moving forward, we really anticipate Ascentge will be a global leading Biotech company three years from now (2026?), we will have global sales, can be truly pharma company where we generate revenue and profit from our own products.
We move single agent first, single agent CML, already marketing, going to the global registration trial; single agent CLL, finish registration study and filling NDA and then combination with standard care to the AML/ALL, and then after that, is MDS and MM. you can easily calculate this hugely potential in the global leading position. I think, moving forward, a lot of people always asked me what is the guidance. I think the guidance come from the confidence and the data. one thing I have to say, with our 15 years in the world R&D, 4 years HK stock market. I can say this is very clearly that Ascentage is currently hugely undervalued and also have huge potential to be global leader in the hematological space. Thank you!