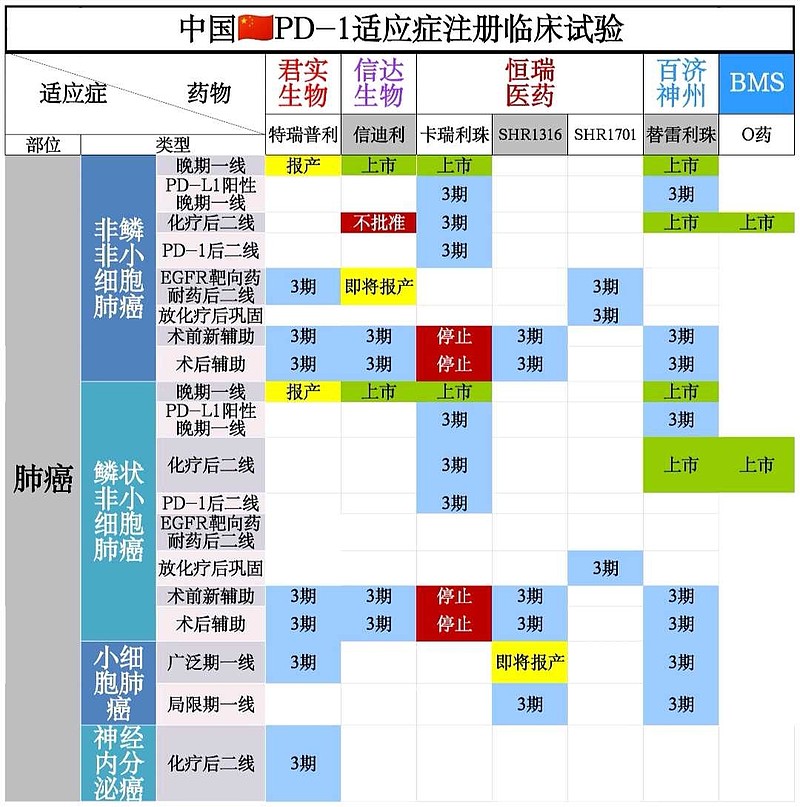
(一)$信达生物(01801)$
信达生物的信迪利单抗,单药二线治疗(含铂化疗后)鳞状非小细胞肺癌,3期临床orient-3研究,其实是失败了。
2021年已经被中国🇨🇳NMPA否决,不予批准上市。
信达生物公司的回应是——#主动撤回注册申请# 。
中国🇨🇳NMPA不批准的理由很简单:
①信迪利单抗的老毛病了,对于肺癌疗效较差。
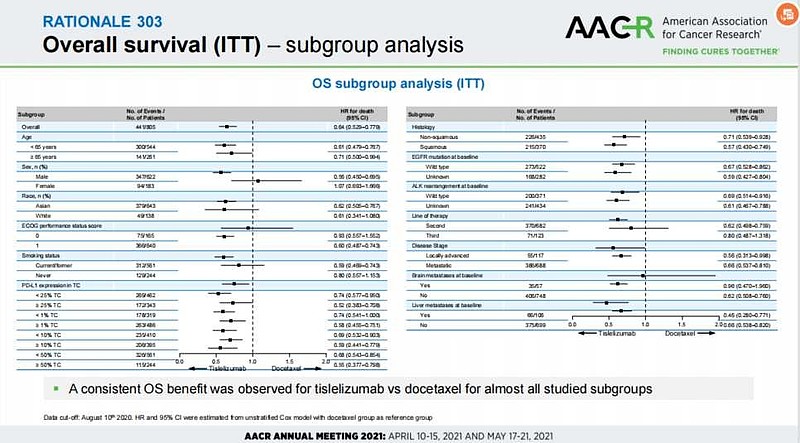
对于PD-L1 TPS<1%亚组的肺癌,疗效差, OS HR=1.055。
另外,对于ECOG评分=0分亚组的肺癌,疗效差,OS HR=1.284。
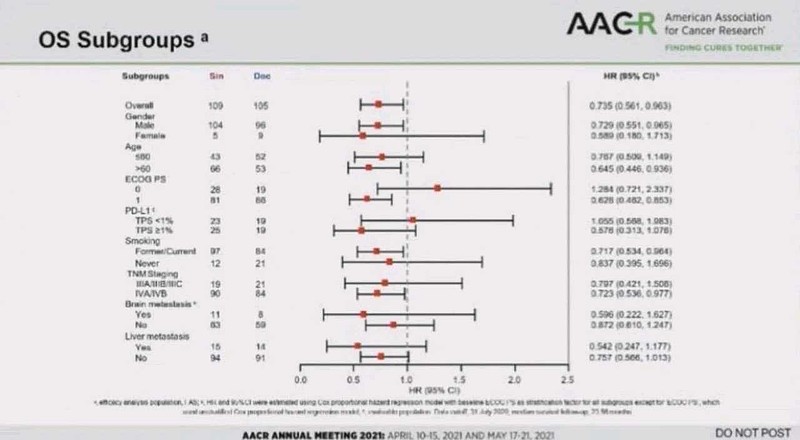
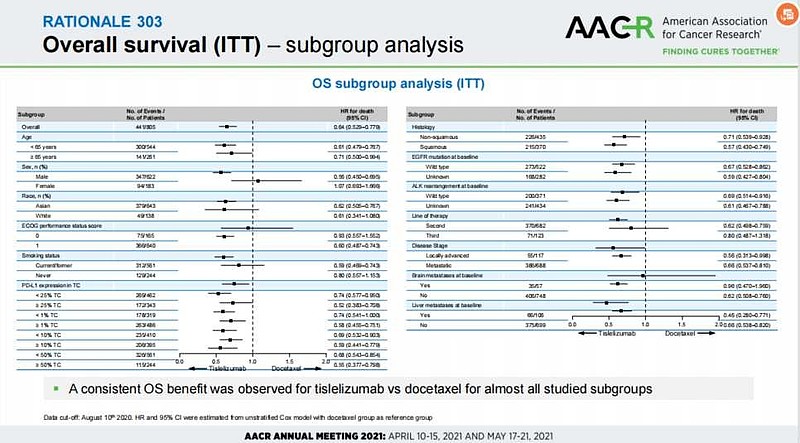
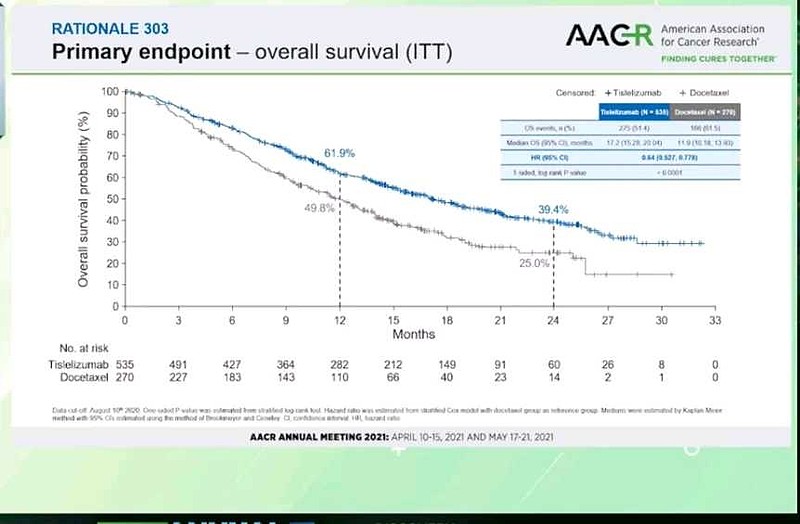
可以对照的是——$百济神州-U(SH688235)$ rationale303研究,
对于PD-L1 TC<1%亚组的肺癌,疗效较好, OS HR=0.74。
另外,对于ECOG评分=0分亚组的肺癌,有获益趋势,OS HR=0.90(0.557-1.562)。
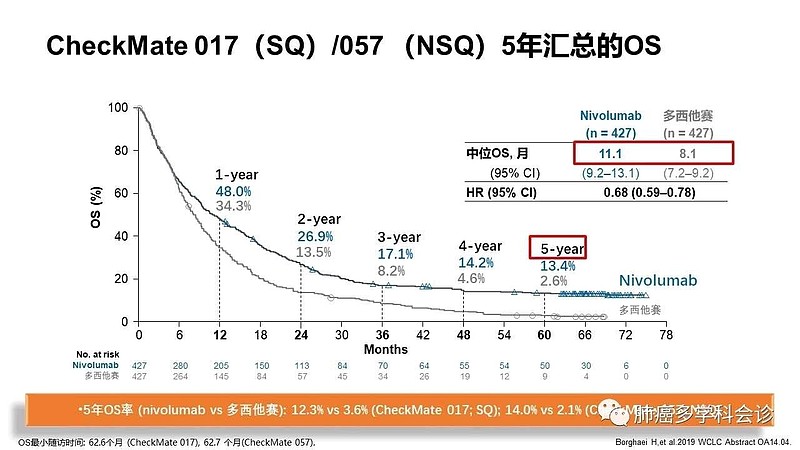
还可以对照的是——#百时美施贵宝# checkmate017研究和checkmate057研究。
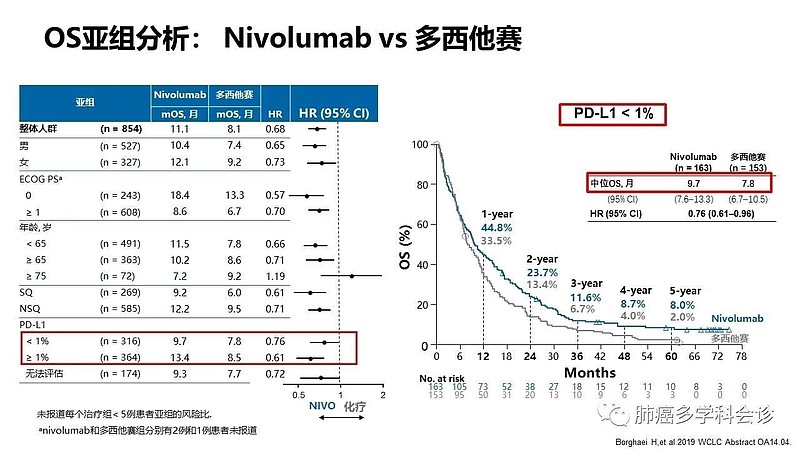
对于PD-L1 TPS<1%亚组的肺癌,疗效较好, OS HR=0.76。
另外,对于ECOG评分=0分亚组的肺癌,疗效较好,OS HR=0.57。
②orient-3研究不是双盲对照试验,而是开放标签,让人难以理解。
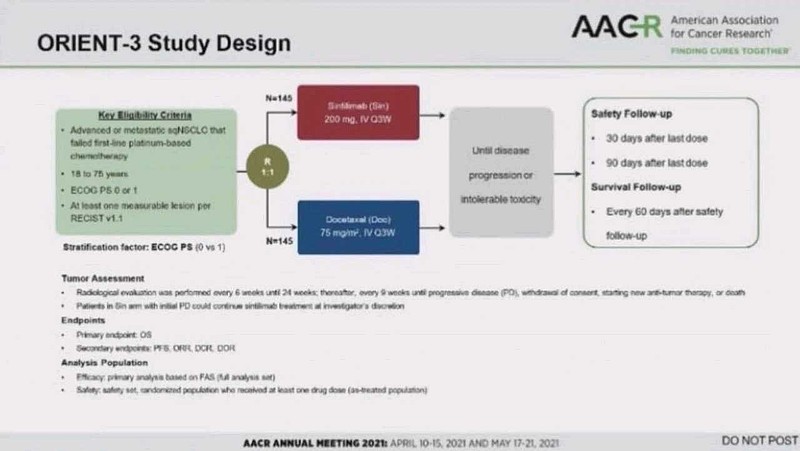
毕竟,信迪利单抗治疗方案是1次/3周,多西他赛治疗方案也是1次/3周。
没有必要开放标签呀。
事实上,最终的结果就是,入组患者平均接受了8周期信迪利单抗治疗,2周期多西他赛治疗(范围:1-15周期)。
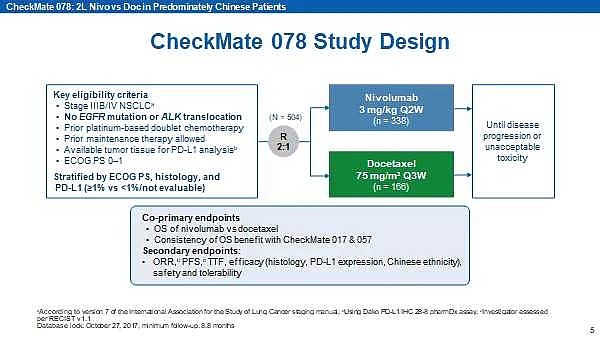
百时美施贵宝的中国人群3期临床试验,checkmate078研究,O药治疗方案是1次/2周,多西他赛治疗方案是1次/3周。设计成为开放标签,可能是合理的。
显而易见,信达生物还需要大规模增加3期临床试验招募入组患者数量。
(二)百济神州
百济神州的替雷利珠单抗,单药二线治疗(含铂化疗后)非鳞+鳞状非小细胞肺癌,3期临床rationale303研究,临床试验达到了OS主要终点。
即将于2022年,向美国🇺🇸FDA/欧洲🇪🇺EMA,提交注册申请。
美国🇺🇸FDA可能有50%概率不会批准注册,理由很简单:
①3期临床不是双盲对照试验。
百时美施贵宝的全球人群3期临床试验,checkmate017研究和checkmate057研究,O药治疗方案是1次/2周,多西他赛治疗方案是1次/3周。设计成为开放标签,可能是合理的。
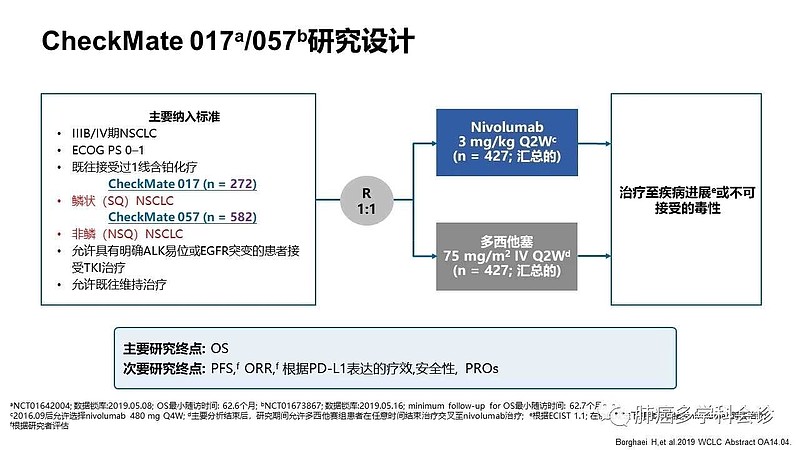
百济神州的全球人群3期临床试验,rationale303 研究,替雷利珠单抗治疗方案是1次/3周,多西他赛治疗方案也是1次/3周。设计成为开放标签,难以理解。

②欧美国家白种人招募入组比例较低。
总计招募入组805例,其中白种人入组138例,白种人入组比例只有17.14%。
亚裔患者入组643例,其中中国患者入组比例高达641例。
③替雷利珠单抗向美国FDA提交注册适应症,<百时美施贵宝O药在美国🇺🇸FDA获批适应症。
百济神州替雷利珠单抗即将提交注册适应症是——单药二线治疗(含铂化疗后)非鳞+鳞状非小细胞肺癌。
百时美施贵宝O药已经获FDA批准的适应症是——单药二线治疗(含铂化疗,或者EGFR靶向药物治疗后)非鳞+鳞状非小细胞肺癌。
百时美施贵宝PD-1适应症范围更广。
④百时美施贵宝的OS生存期数据长达5年,百济神州的OS生存期数据只有2年。
海外临床医生更喜欢长期生存OS数据。
诺华/百济神州替雷利珠单抗的食管鳞癌二线、非小细胞肺癌二线适应症,直接面临百时美施贵宝的市场竞争压力。
⑤女性患者入组比例太少,疗效较差。
对于女性患者亚组的肺癌,疗效较差, OS HR=1.07(0.693-1.666)。
(三)$君实生物-U(SH688180)$
没有开展特瑞普利单抗非小细胞肺癌二线治疗的3期临床试验。
(四)恒瑞医药
2021年,开展了卡瑞利珠单抗+法米替尼,联合用药二线治疗(化疗后、PD-1经治)非小细胞肺癌,国际多中心3期临床试验。