回顾辉瑞特效药临床试验及审批时间线,预测VV116一切顺利的前提下,上市时间线,见下图:
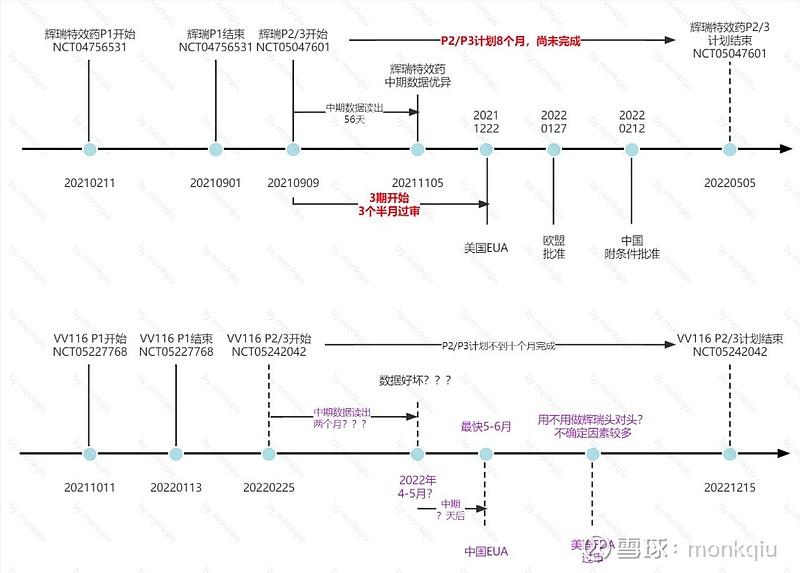
结论如下:
1、理论上,比对辉瑞特效药,vv116 3期中期数据最快也要到4-5月,国内批准上市流程走完估计得5-6月了。
备注20220305:20220218电话会议上提到,官方科技日报的口径是年内获批,当然这个和三期临床实验进度一致。但个人始终坚定一个信念,能否提前获批,取决于临床数据,还有疫情发展情况,以及国内特效药物发展情况。如同FDA评审一样,优先的核心是,是否是未被满足的需求,以及足够的数据支撑。
2、由于开始P2/3的时间已经是2022年2月了(实验设计在1月左右,如果和FDA有过沟通也应该在这个时候),是否需要和辉瑞特效药做头对头是个问题。辉瑞自己的3期都没做完,如果不故意卡就好说,否则FDA的时间可能无限延长。另外已经是国际多中心了,人种分布的风险感觉没那么大。
3、近期应该会公布一期数据(12日电话会提到两周,差不多了),个人理解一期数据应该不会有大问题,毕竟瑞德西韦衍生物,瑞已经用了一年多了。而且116在乌国已经用了,虽然数据也没公开。
4、不确定因素:
4a、辉瑞快速审批的前提是欧美疫情不可控,从这点上说,对中国监管而言vv116似乎没有同样的紧迫性,也就是说有可能更晚;
4b、乌国三期的数据是否能提前出来,如何看待乌国的三期数据?
4c、如果辉瑞特效药的产量在中国厂家的帮助下快速放大,还有多少空间给vv116及后来者?
至于中国别的药,这样说吧,至少晚2个月没跑。
所以原料药,代工厂走势好于国产特效药,是有合理逻辑支撑的。
以岭药业之类的中药同样好于特效药,人家不用审批啊,![]() 。
。
但是,中国需要自己的特效药,自用以及走出去。