11月10日,CDE官网显示信达生物/Incyte制药的Parsaclisib片在中国获得临床默示许可,适应症为复发/难治滤泡性淋巴瘤和复发/难治边缘区淋巴瘤。

Parsaclisib是一种高活性、高选择性的新一代口服PI3Kδ抑制剂,CITADEL 系列的II期临床研究中探索了Parsalisib针对非霍奇金淋巴瘤,包括滤泡性淋巴瘤、边缘区淋巴瘤和套细胞淋巴瘤的疗效和安全性。此外,Parsalisib在骨髓纤维变性、局部晚期或转移的实体瘤以及弥漫性大B细胞淋巴瘤里均开展了相应的I期和II期临床研究。
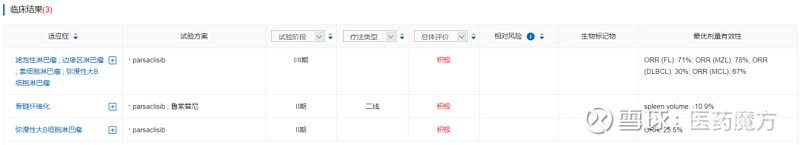
来源:医药魔方NextPharma
2018年12月,信达生物与Incyte就pemigatinib(FGFR1/2/3抑制剂)、itacitinib(JAK1抑制剂)和parsaclisib(PI3Kδ抑制剂)3款药物达成战略合作,信达生物获得这3款药物在中国大陆及港澳台的开发和商业化权利。
信达生物在2019上半年业绩报告中表示,IBI-376(parsaclisib)正于美国对复发或难治性边缘区型淋巴瘤患者进行II期研究,并且计划于2020年上半年进行两场针对二线滤泡性淋巴瘤及边缘区型淋巴瘤以及一线被套细胞淋巴瘤患者的III期试验。Incyte计划于2020年Q2向FDA提交NDA。