在乳腺癌领域展现出惊人的效果后,ADC药物的呼声越来越高。但这并不意味着,ADC药物就没有焦虑时刻。
全球最成功的ADC药物之一,眼下就遭遇了PD-1的挑战。
守擂者是2023年全球医药行业最大并购案的主角——Seagen。其ADC药物Adcetris,雄踞霍奇金淋巴瘤一线疗法已经多年。
攻擂者则是百时美施贵宝。作为PD-1的开拓者,O药对Adcetris所在的市场虎视眈眈。
药企之间的竞争不像抛硬币,结果是正面或反面的概率一样。胜利的天平,永远倾向于实力最为强劲的那一方。
如今看来,在这场强者之间的对决中,O药笑到最后的概率越来越大。
在2023年的ASCO大会上,百事美施贵宝公布了O药联合多柔比星(阿霉素)、长春碱和达卡巴嗪(AVD方案)一线治疗霍奇金淋巴瘤的三期临床试验结果。
数据显示,相比于ADC药物Adcetris联合AVD,O药联合疗法效果更优。
这也意味着,O药大概率将直击Adcetris腹地。
PD-1与ADC之间的较量,并不会因为这一次的对决而一锤定音。随着ADC与PD-1适应症的不断扩张,下一场战争似乎难以避免。
某种程度上,两者之间的竞争,也只是创新药行业的一个缩影:
这些参与者们实力各异,起点不同,路径不同。但他们,都面临着同样巨大的挑战和不确定的未来。没有人会是常胜将军,也没有人知道挑战者会在何时突然出现。
/ 01 / 雄踞霍奇金淋巴瘤适应症
在如今大火的ADC领域,Adcetris堪称元老级药物。
早在2011年,当ADC领域还处于百废待兴之时,Adcetris就在美国获批上市,用于治疗霍奇金淋巴瘤(HL)和系统性间变性大细胞淋巴瘤(sALCL)。
对于这些患者来说,Adcetris堪称救世主。
HL患者虽然对化疗及放疗高度敏感,但仍有约5%-10%的患者对于初始治疗无反应,10%-30% 的患者在一线治疗达到完全缓解后出现进展或复发。
当时,这部分对化疗、放疗耐药的患者,没有其他药物可以选择。Adcetris的问世,改变了这一窘境。
Adcetris由二肽连接子、靶向CD30的单克隆抗体cAC10、MMAE毒素三部分形成。
其中,CD30是肿瘤坏死因子受体超家族成员,大约95%的HL病例中都存在着CD30高表达,但在正常组织中CD30表达相对有限,所以CD30也成为了对抗HL的理想靶点。
在一项单臂二期临床试验中,经过Adcetris治疗的102例自体干细胞移植后复发或难治性cHL患者中,ORR(客观缓解率)达75%,CR(完全缓解)为34%,DCR(疾病控制率)高达96%。
对于无药可治的患者,Adcetris依然能够展现极为突出的疗效。
因此2011年FDA根据这一单臂临床试验结果,批准Adcetris上市用于治疗HL。这是1977年以来,HL领域批准的首个创新药。
此后,围绕着HL领域,Adcetris继续拓展适应症。
2018年3月20日,FDA批准Adcetris联合 AVD方案(阿霉素、长春碱、达卡巴嗪)一线治疗III期或IV期HL成年患者,Adcetris在HL领域的地位一举奠定。
在一线治疗晚期HL领域,除了ABVD方案(阿霉素、博来霉素、长春碱、达卡巴嗪)之外,仅有Adcetris联合 AVD这一种治疗方案可选。
所以,即便患者群体有限,Adcetris商业化数据依然不差。2022年,Seagen与合作伙伴武田制药的Adcetris销售额合计已达14.69亿美元,在全球ADC药物销售额排行榜中位列第二。

未来,随着Adcetris的适应症继续扩张,销售额大概率将随之上升。Clarivate曾预测,2024年Adcetris年销售额将突破20亿美元,成为一款当之无愧的重磅炸弹药物。
然而,O药的突然闯入,击碎了Adcetris的美梦。
/ 02 / PD-1杀入Adcetris主场
虽然Adcetris如日中天,但对于该领域,PD-1抑制剂一直虎视眈眈。
从机制上来说,在HL的细胞系中,PD-1信号通路异常,是肿瘤发生的重要原因:
由于9号染色体特定区域(9p24.1)扩增导致PD-1配体表达增加,EBV+的cHL通过EBV编码基因的异常激活而上调PD-L1表达。
这些因素导致,HL细胞表面具有极高表达的PD-L1受体,可以与T细胞表面的PD-1相互结合,释放出“我是自己人”的假信号,使得肿瘤细胞成功逃脱人体免疫卫士T细胞的追杀。
由于PD-L1受体表达量极高,因此通过PD-1抑制剂阻断该信号通路的效果也会极为突出。所以,HL也成为最有可能获益于PD-1抑制剂治疗的淋巴瘤。
我们也能看到,包括派安普利单抗、卡瑞利珠单抗在内的不少PD-1抑制剂,都成功拿下了后线治疗HL的适应症。但是,在想象空间更大的一线治疗HL领域,暂无挑战成功者。
眼下,这一历史或将被O药改写。
2023年ASCO大会上,百时美施贵宝公布了名为SWOG S1826的三期临床试验结果,这是一项有史以来规模最大的HL研究。
在这项试验中,试验组N-AVD接受了多柔比星(阿霉素)、长春碱和达卡巴嗪 (AVD) 、O药的联合治疗,而在对照组BV-AVD中O药被替换成了Adcetris 。
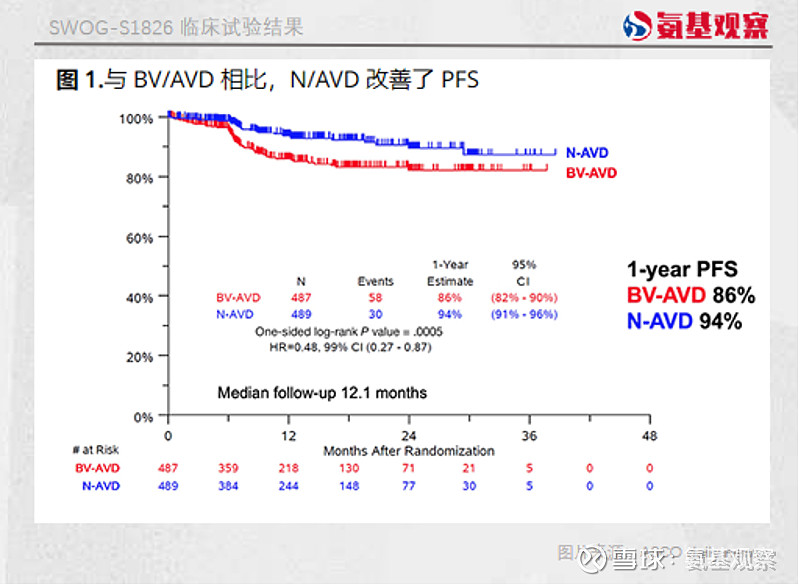
试验结果显示,相比于BV-AVD组合疗法,N-AVD组合疗法能够将HL患者进展或死亡风险降低52%。在治疗1年后,N-AVD组PFS率为94%,而在BV-AVD组中这一数字为84%。
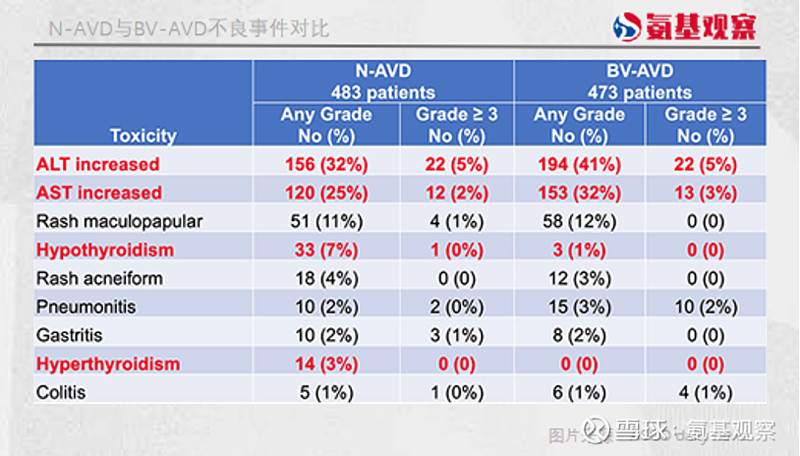
在安全性方面,N-AVD组看起来也更具优势。BV-AVD组中停药率达到22%,但N-AVD组仅为11%;BV-AVD组出现了11例患者死亡事件,其中7例死亡与药物毒性相关,而在N-AVD组患者死亡仅有4例,其中3例与药物毒性相关。
更好的疗效与安全性,都使得O药直攻Adcetris的腹地,跻身一线治疗HL的阵营。
/ 03 / 挑战者与被挑战者
当然了,结局究竟如何,还有待时间揭晓谜底。
如今O药在一线治疗HL的优势还局限于PFS获益,金标准OS(总生存期)的数据尚未出炉。
而在临床试验中,PFS的获益并不总是都能转换为OS优势。所以,O药能否在一线治疗HL领域彻底打败Adcetris,还需要等待更多的数据才能下定论。
但无论如何,对于Adcetris而言,一个不能忽视的对手已然出现,在HL领域建造的壁垒开始出现裂痕。
不过,Adcetris在HL领域的处境,同时在说明,不断上升的ADC药物研发热潮,也会遇到挫折。
过去一段时间里,随着第三代ADC药物DS-8201,在多个领域刷新ADC药物的天花板,使得不少人对于ADC药物的期待极高,不管是Big pharma还是Biotech,都在用ADC武装自己。
ADC药物,开始向多个不同的癌种试探。不少人都抱着这样的希冀,DS-8201在乳腺癌领域的所向无敌之姿,能够被其他ADC重演。
但现实是,ADC并不能在每一个领域都所向披靡。
比如在血液瘤领域,ADC便显得力不从心,先是葛兰素史克的Blenrep因临床失败而退市,接着又是阿斯利康的Lumoxiti因疗效和副作用问题,商业化无解而黯然退出市场。
这一次,ADC在霍奇金淋巴瘤的遭遇,更进一步说明了,ADC药物并不是无往而不胜的。
对于药企来说,当下的ADC赛道越是火爆,就越是要理性,通过理性的判断和足够的耐心,一步一个脚印向前探索,最终找出ADC的最佳作用点。
