
会议报名点击阅读原文
转载请注明作者和来自新康界(XKJ0101)
2018年7月5日,欧洲药品管理局(EMA)发布公告称浙江华海药业生产的缬沙坦原料药检出致癌物质亚硝基二甲胺(NDMA),EMA随即展开相关评估调查,欧盟各国启动召回。
此消息一出,再加上7月5日华海发布公司股东及董监高减持股份的公告,华海于2018年 7月 5日、7月 6日、7月 9日连续三个交易日内收盘价格跌幅偏离值累计超过 20%以上的异常波动。

7月7日,华海药业发布公告称,公司在对缬沙坦原料药生产工艺进行优化评估的过程中,在未知杂质项下,发现并检定其中一未知杂质为亚硝基二甲胺(NDMA)。根据相关科学文献中基于动物实验的数据显示,该杂质含有基因毒性。
缬沙坦对华海影响有多大?2017年华海药业营收50亿元其中缬沙坦原料药销售3.28亿元。华海2017以来连续每个月稳定出口至美国9个产品中其中一个就是缬沙坦。
华海的缬沙坦片和缬沙坦氢氯噻嗪片曾经进入722临床自查核查清单,坎地沙坦酯片不予批准后(公告2015年第229号),华海撤回了缬沙坦片和缬沙坦氢氯噻嗪片(2015年第255号),直到2017年12月华海的缬沙坦片才进入第十一批自查(2017年第149号),缬沙坦氢氯噻嗪片则于2018年6月进入第十四批自查(2018年第30号)。
华海的缬沙坦片以新4类申报并且以“国外已上市同步申请国内上市的仿制药”为由获得优先审评,已于2018年5月正式国内上市,亦进入《中国上市药品目录集》,可视为通过一致性评价。缬沙坦氢氯噻嗪片亦以“同一条生产线生产,2016年美国上市”为由获得优先审评。
国内企业主要通过原料药方式出口欧美

在美国,FDA原料DMF除了华海还有浙江新赛科(华润双鹤(SH:600062))、浙江天宇(天宇股份(SZ:300702))、海正药业(SH:600267)和润都股份(SZ:002923)。欧盟CEP登记除了上述的华海、天宇、海正,还有浙江昌明化学。出口缬沙坦原料药的还是以我国上市公司(包括控股公司)为主。
目前网上针对NDMA的杂质做出反应的生产厂家主要有浙江天宇和新赛科。从浙江天宇和新赛科公布的声明可以看出,欧洲药品管理局(EMA)对N-亚甲基亚硝胺(NDMA)的限度要求为不高于0.3ppm。但从华海的公告中暂未能了解华海的检验限度超标情况。
浙江新赛科属于华润双鹤的控股孙公司,此前华润双鹤的子公司华润赛科药业有限责任公司曾发布拟转让浙江新赛科药业有限公司51%股权的公告,转让底价为13770万元,华润赛科共持有新赛科82.52%股权。预告转让股权与2017年新赛科滥用市场支配地位罚款29万有关。新赛科已经对50多个批次进行检验,暂未超过标准。天宇则选择抽检3批,发现N-亚甲基亚硝胺(NDMA)没有超过限制。
华海为啥NDMA杂质超标,预计是其新工艺采用DMF溶剂,三乙胺-叠氮酸钠做环合剂,亚硝酸钠淬灭做后处理有关,新赛科前期的工艺与华海相同,淬灭选了次硝酸钠。浙江天宇和海正尚未公布工艺,但预计还是和华海有所不同。
最新FDA召回清单:暂无中国其他生产厂家

华海于2018年7月13日发布《关于缬沙坦原料药的未知杂质中发现极微量基因毒性杂质的进展公告》主动召回国内外上市的缬沙坦原料药,华海2017 年度国内缬沙坦原料药销售收入约为 1,396 万元人民币;2018 年1 月至 6 月预计销售收入约为 1,284 万元人民币。
而FDA也在2018年7月13日公布了需要召回的公司清单,暂无中国其它生产厂家。
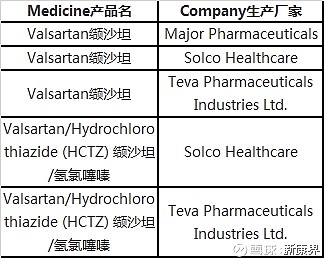
FDA召回缬沙坦生产厂家
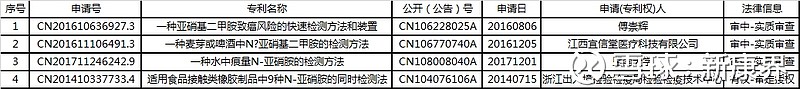
国内目前关于亚硝基二甲胺的检测方法专利主要用在食品分析方面,暂无用在药品检验的专利,暂未看到华海申请专利的信息。
我国亚硝基二甲胺的检测方法专利列表
小结

华海短期内将会面临同类厂家争夺市场的风险,国内该基因毒杂质控制在限度范围之下的生产企业就是主要的竞争对手。在研缬沙坦及缬沙坦复方制剂(缬沙坦/氢氯噻嗪,缬沙坦/氨氯地平,缬沙坦/阿利克仑半富马酸盐,缬沙坦/沙库巴曲)的药品上市许可持有人都需要研究此基因毒杂质的检测标准是否需要进入自己的制剂标准。
此外,NDMA的制剂限度应该如何制定,原料工艺变更了是否需要重做BE等等都有待国家药监部门解答。
—精彩回顾—

资本峰会 | 56个项目路演公示!
点击上图阅读文章