CD47靶点被称为“下一个PD-1”,可研发之路却一波三折、“难倒英雄汉”。
从再鼎到罗氏,再从艾伯维到吉利德,不是对CD47抗体降级开发,就是放弃开发,甚至因疗效不足终止开发。
新药开发的目的在于为患者提供安全、有效的治疗方案。为了达到这两项指标,CD47抗体研发已经走过了一段又一段坎坷的路途。
一、CD47靶点:泛癌药潜力,国内布局药企超30家
与PD-1一样,CD47靶点也能广泛表达在不同的癌细胞,因此成为了后PD-1时代的明星靶点。
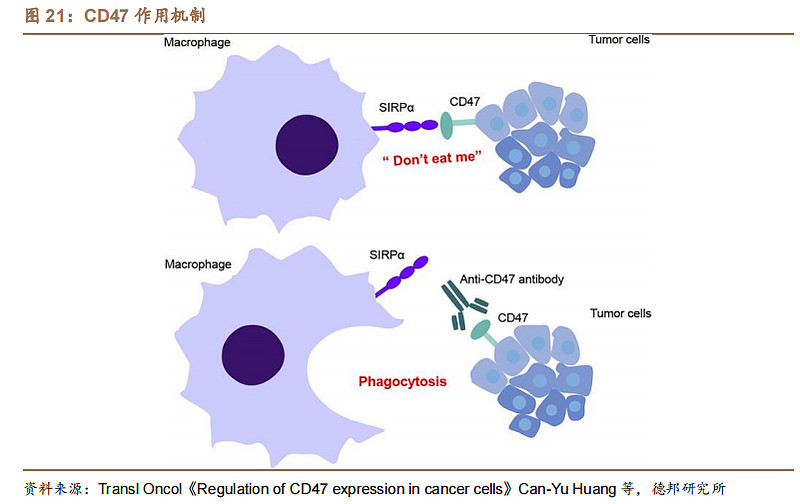
从作用机制看,CD47可以和巨噬细胞表达的SIRPα相结合,释放“别吃我”信号,进而阻断巨噬细胞对肿瘤细胞的吞噬作用。研究者认为抑制癌细胞中CD47信号可能促进巨噬细胞对肿瘤细胞的吞噬,从而限制肿瘤生长。
简而言之,CD47可以阻止巨噬细胞吞噬和破坏肿瘤细胞。
此外,CD47成为新一代免疫疗法热门靶点的另一个重要原因,更在于PD-1的内卷、急需新的前沿靶点替代,以及自身释放出的极大的市场潜力。
正是看中CD47被开发为泛癌药的潜力,财大气粗的国外头部玩家掀起了资本热潮。
例如,吉利德于2020年3月斥资49亿美元收购了Forty Seven,将明星药物IgG4 CD47单抗Hu5F9-G4(Magrolimab)纳入囊中;同年9月,艾伯维与天境生物达成交易总额近30亿美元的license-in交易;辉瑞于2021年8月斥资近23亿美元对价收购了Trillium,并囊获靶向CD47肿瘤免疫在研疗法。
这些巨额交易,不仅将CD47抗体研发推向了最高潮,还吸引了无数后来者前仆后继地涌入这条赛道。
除了上述三家国外头部玩家以外,目前国内CD47抗体药物赛道已遍地开花。据Insight数据库显示,当前已有36款产品进入临床阶段,涵盖单抗、双抗和融合蛋白等药物类型,布局企业涉及天境生物、康方、信达、天广实、百奥泰等超30家企业。

国内进入临床阶段CD47单特异性抗体 来自:Insight 数据库网页版(下文如无特殊标注,为同一来源)
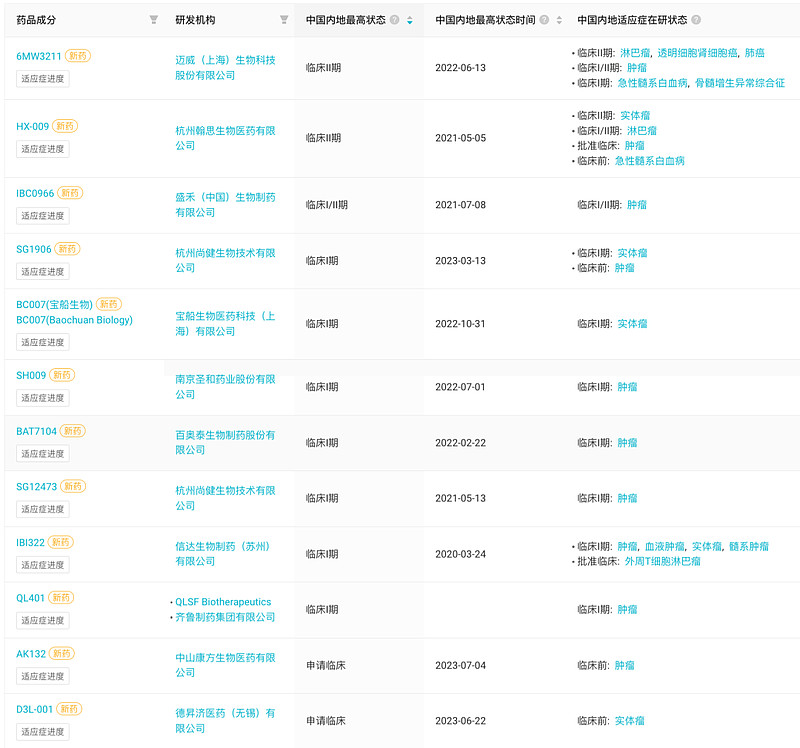
国内进入临床阶段CD47双特异性抗体
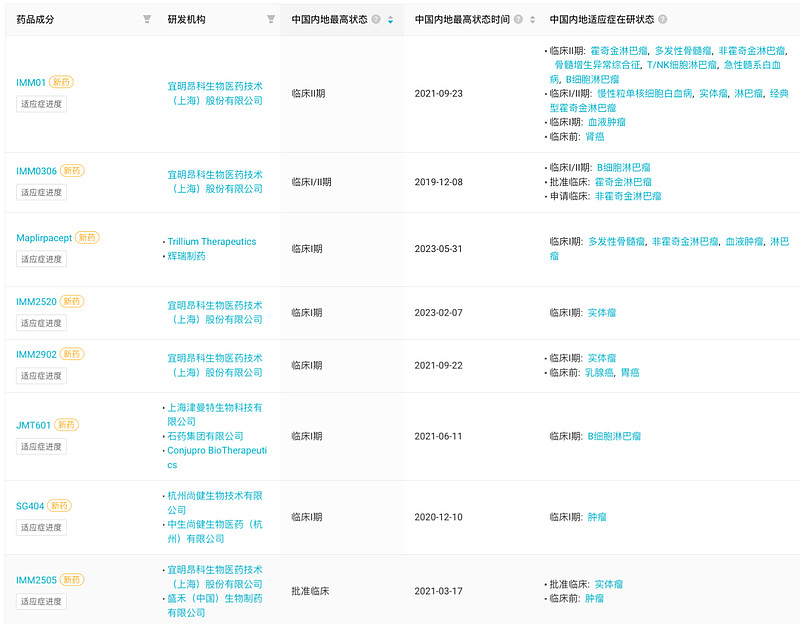
国内进入临床阶段CD47抗体类融合蛋白
实际上,理想很丰满,现实却很骨感。CD47抗体研发,并没有想象中的那般顺利。
二、CD47抗体研发的“拦路虎”:安全性、疗效
布局者众,成功者少,是当下CD47抗体研发的残酷现状。
CD47抗体研发的第一道难关,就在于安全性。
由于CD47在人体内红细胞上广泛表达,靶向CD47药物在杀伤肿瘤时会导致红细胞的吞噬破坏和凝集,误伤红细胞,影响其使用的安全性和耐受性,造成贫血、血小板减少症等血液毒性问题。
例如,Arch Oncdogy的Ti-061、新基公司(Celgene)的CC-90002和Surface Oncology的SFR231,都因发生严重溶血反应导致临床失败。
如何在保护红细胞的同时,最大程度地杀伤肿瘤细胞,成为CD47抗体研发的核心关键。
为了降低药物红细胞毒性并提高疗效,吉利德Magrolimab在Fc端采用了IgG4亚型而非IgG1亚型,由于IgG4亚型不能引发强烈的ADCC和CDC效应,降低了对红细胞、血小板的影响,并且通过预激给药的方式来解决血液毒性的问题。
实际上,这种解决方案的确获得了良好的安全性数据:根据Forty Seven公司在2019年ASH会议上公布的Magrolimab和阿扎胞苷联合治疗高风险AML(急性髓系白血病)和MDS(骨髓增生异常综合征,无法进行诱导化疗的患者)临床Ib期研究结果显示,在62例患者中只有1例(1.6%)因治疗相关不良事件停止治疗。
当时正是基于这项优异的数据,吉利德才斥资49亿美元收购Forty Seven。

之后,吉利德在万众瞩目中开启了Magrolimab联合阿扎胞苷联合治疗MDS的Ⅲ期临床试验。这也是验证CD47靶点成药性最接近成功的一次。
事实上,新药研发总是充满坎坷。
7月21日,吉利德在万众期待下遗憾宣布:因在中期分析中发现联合疗法有效性不足,终止Magrolimab联合阿扎胞苷联合治疗MDS的Ⅲ期临床试验。
好不容易迈过了安全性这道坎,却因疗效不足栽了。这便是CD47抗体研发要跨越的第二道难关:疗效。
虽然Magrolimab在Fc端采用IgG4亚型,确实提高了安全性。但与此同时,由于IgG4 Fc只传递适中的信号,导致CD47单抗对肿瘤细胞的杀伤能力被大幅度削弱。
单药使用效果有限,药效也降低。这也是为何研发靶向CD47药物要采取联合用药,或开发基于CD47的双抗的缘故。
三、“全村的希望”:天境、康方、信达能否逆袭?
穷且益坚,不坠青云之志。
尽管Magrolimab已经在MDS适应症上宣告失败,但吉利德还在开发10多项涵盖血液瘤和实体瘤适应症,其中就包括“硬骨头”AML(急性髓细胞性白血病)。
AML是成人中最常见的急性白血病类型,约占成人白血病的70%。据统计,我国AML的发病率约为2.57/10万人,死亡率约为每年1.57/10万人。现有治疗方案阿糖胞苷化疗和造血干细胞移植治疗,虽然有效延长了患者生存期,但数据都不算惊艳。就看吉利德能否再次创造奇迹了。
虽然罗氏、艾伯维和吉利德等国外头部玩家接连受挫,但CD47抗体研发进展靠前的天境生物、信达生物和康方生物,还有机会成为“全村的希望”。
例如,天境生物的来佐利单抗(lemzoparlimab)虽然也采用了IgG4亚型抗体,但却利用其独有的人源天然噬菌体技术,筛选出了可以结合在稀有表位上的CD47抗体,通过降低与红细胞的结合解决血液毒性的问题。
不过,正如前文所述,这种采取IgG4亚型抗体的解决方案,存在药效降低的缺陷。就看天境生物如何解决这一问题。
值得一提的是,Lemzoparlimab并没有放弃MDS适应症。而且,根据天境生物近期投资者文档,该药与Magrolimab疗效相当的同时安全性可能更优,与红细胞结合更低。

来自:天境生物官网资料
另外,Trillium(被辉瑞收购)的产品TTI-621,也采取了这种降低CD47对红细胞的结合能力的解决方案。
康方生物的AK117(莱法利单抗)也有着独特的结构设计,属于新一代人源化IgG4 mAb,无血凝作用,可诱导巨噬细胞对肿瘤细胞的强大吞噬作用,无需较低的预剂量来预防贫血,且抗肿瘤活性良好。
不仅如此,无论单药或联合化疗、联合双抗±化疗,AK117在血液瘤或实体瘤中总体安全性良好且无种族差异,并且不需要预激给药。
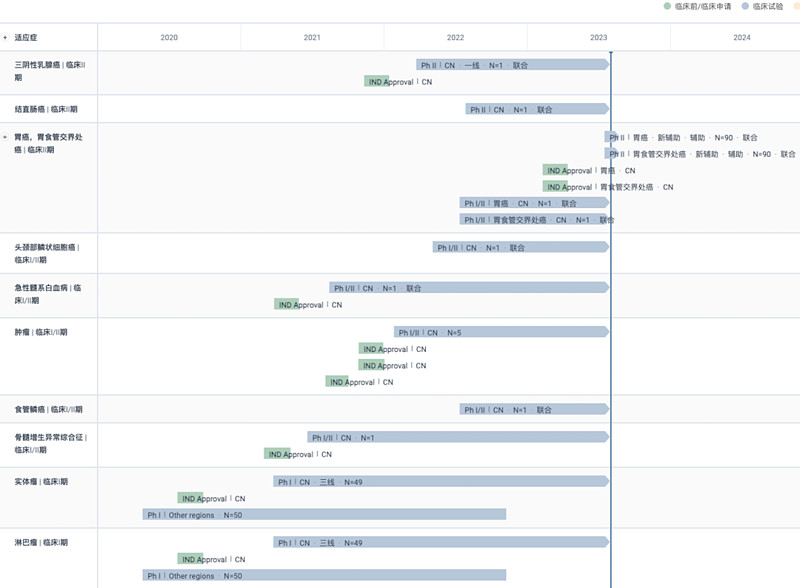
AK117全球项目开发进度甘特图
值得一提的是,目前针对三阴乳腺癌治疗的CD47靶向药物只有AK117,而且联合阿扎胞苷治疗MDS、AML适应症的研究均已进展到临床Ib/II期阶段。

AK117针对 MDS、AML临床试验
综上可见,独特的结构设计,确实呈现出一定的差异化优势。但最终能否成药,仍需时间来检验。
四、尾声
总结来看,CD47抗体研发确实面临诸多坎坷,即便是罗氏、艾伯维、吉利德等头部玩家也接连受挫。当然,即便是过去如日中天的PD-1,研发之路也曾布满荆棘和坎坷。
从现有的解决方案看,独特的结构设计、联合用药或玩法更高级的双抗,期待能走出不一样的风景。
参考资料:
1、《康方生物-B-9926.HK-自主商业化验证+大单品出海,持续进化的新一代创新药龙头》,德邦证券
2、《屡败屡战,CD47靶点是否还有未来?》,同写意,2023-01-28
(完)
本文所写的内容,不同投资者有不同的看法,难念存在争议性。由于粽哥阅历所限,如有不足之处,还请批评指正,多多担待。
本文所提个股,不做投资买卖建议,仅供参考,不喜勿喷