续前两篇:1.恒瑞医药分析之基本面:雪球 网页链接;2.恒瑞医药分析之估值和投资展望: 雪球 网页链接。
截止2020年底,继成为中国沪深A股上市公司医药制造行业的股王之后,恒瑞医药接连入围了“全球药企市值25强”、“亚洲上市公司50强”,市值超过6000亿元,位居医药领域市值第一;尽管仿制药依然占大头,但创新药销售占比稳步增长,预计在未来三年内将达到40%-50%。

一、创新起步
恒瑞医药的前身是始创于1970年的连云港制药厂,隶属于当地的街道办事处,主要生产红药水、紫药水等生产技术含量低的仿制药,利润微薄且市场竞争剧烈,一度陷入倒闭的困境。为解当地医药企业发展的困局,连云港医药管理局批准管辖下的企业可以启用一批
年轻人担任管理者。1990年,32岁的孙飘扬掌权制药厂,当时只有300多名员工,一年利润只有8万元。
作为中国药科大学的毕业生,技术出身的孙飘扬深知研发的重要性,上任之初制定了以高技术仿制药扩大市场的战略。当时他敏锐地捕捉到VP-16抗癌制剂的市场潜力,通过四处借款筹集300万元从一位大学教授手中买下了该专利。次年靠这一新药,连云港制药厂创造了5000万元的销售额,制药厂就此转危为安。 靠着生产VP-16取得的第一桶金,连云港制药厂进一步引进其它专利配方,生产更多的高端仿制药。1992年又斥资120万元购买了中科院药研所的抗癌新药异环磷酰胺的专利权,并通过临床试验,于1995年成功上市获得巨额资金回报。连云港制药厂初次的战略转型大获成功,企业发展也逐渐步入正轨。
1997年,连云港制药厂迎来了国企改制,恒瑞医药正式成立,恒瑞医药从一家国有性质企业变成了一家民营企业。虽然此前的高技术仿制药战略取得了极大成功,但是勇于创新的孙飘扬不满足于此。他认识到仿制药在日益激烈的市场竞争中空间将越来越少,并前瞻性地预测到创新药未来的战略制高点地位,于是果断决定第二次进行战略转型,由高技术仿制药转向创新药,同时放弃了已经取得一定成就的高技术仿制药的研发。恒瑞的首个创新药“艾瑞昔布”从1999年开始研发,于2011年才获批上市,历时12年之久,而“艾瑞昔布”之前的几个项目均已失败告终。2004 年,公司决定第三次转型,制定了创仿结合“两只脚走路”的战略,形成“‘仿制药’+‘创新药’”共同发展的格局。
第三次转型也成为恒瑞医药发展史上的重大转折点。2011年恒瑞首个创新药“艾瑞昔布” 获批上市,2014年第二个创新药阿帕替尼上市,随后又有多个创新药上市。得益于多个创新药相继上市,恒瑞营业收入从2011年的45.50亿元增长到了2019年的232.9亿元,净利润从2011年的 8.77亿元增长到了2019年的53.26亿元。2020年恒瑞医药销售收入达277.35亿元。
二、创新布局
即使与国际巨头相比,恒瑞医药的研发能力毫不逊色。目前,恒瑞医药在美国、日本、澳大利亚、德国等地设有分公司,从事行业研究趋势监控、新药研发、技术项目引进或转让、向当地申报和注册药品等工作。在创新药国际化方面,2018年恒瑞医药有SHR0302 片、INS068注射液、SHR0410注射液3个产品获准在海外开展临床试验。在仿制药国际化方面,恒瑞医药已经有地氟烷、注射用塞替派、磺达肝癸钠注射液等在美国获批;碘克沙醇注射液在英国和荷兰获批;盐酸右美托咪定注射液在日本获批。早在2015年9月,恒瑞医药以7.95亿美元将拥有自主知识产权、用于肿瘤免疫治疗的PD-1抗体国外权益出售给美国INCYTE制药公司,实现中国企业从进口美国生物医药技术向出口创新技术的首次转变。在2018年恒瑞医药海外销售额达20亿元人民币。另外,作为中国第一家通过美国FDA认证的医药企业,恒瑞医药始终以国际标准严格要求自己。
三、研发策略
恒瑞医药对仿制药与创新药分别制定了不同的策略。恒瑞医药尽管以创新药的研发而知名,但高度重视仿制药。公司约将70%的研发费用投入到仿制药。而且对于仿制药的技术秘密更为保护。譬如当恒瑞成为中国巨头之后, 无数学者、专家希望参观恒瑞研发实验室。当访客希望参观仿制药实验室时,需要公司董事会审批。反之,若希望参观创新药实验室,普通项目经理审批就可以了。除此以外,恒瑞对于仿制药的研发策略坚持三大原则:
第一,提前布局,争做首仿。恒瑞仿制药的研发工作并非始于被仿药品专利到期时,而是在被仿药品大致还有5年的专利期时,仿制研发工作便已悄然进行。只要被仿药专利期一过,恒瑞便可以立马将自己的新药打入市场, 快速地占领国内外市场。为此,恒瑞医药在全球各地都设立了研究中心,监控全球医药研究的前沿趋势,调研市场的药品需求变化,收集各种专利药品的相关信息,在信息战上抢占先机,从而在研发上先人一步。第二,选择有技术壁垒的仿制药。被仿药处于专利保护期时,药品的很多相关信息会公开,市场效益也可以由市场调研得知。研发实力强大的研究所、药企甚至可以在核心技术保密的情况下通过实验分析,将药品的合成方法给推测出来。而对于这类被仿药,一旦专利到期,因为技术壁垒不高,将会有大量药企进行仿制药生产。因有强大的研发团队支撑,恒瑞只仿有技术壁垒的药品,专攻仿制药中的尖端领域,避开激烈竞争的低端仿制药领域。第三, Me Too, Me B etter, Me Best!恒瑞在仿制药领域的目标不仅是仿制出药效一致的药品,还要在此基础上有所创新, 实现超越,研发出更有效的新一代产品,逐步取代被仿药品,掠夺被仿药品的市场,做到“Me Too,Me Better, Me Best”!
四、核心竞争
一是完整的研发管线。恒瑞医药项目的研发拥有一条完整、清晰的研发线,从项目立项到临床研究再到获批上市都有一个明确的时间规划,按研发线有序推进。经过多年的创新研发布局,恒瑞医药已形成“上市一批、临床一批、开发一批”的良性研发循环。 目前,恒瑞医药在研项目 70多项,其中已进入临床阶段的项目30余项。与此同时,恒瑞持续追踪国际上医学动态热点和监控市场传递的需求信息,不断寻找新靶点, 推动新的化合物立项研究编入研发线。截至2020年,恒瑞医药产品线聚焦于抗肿瘤药、麻醉制剂、心脑血管常发病药、造影剂等的研发,集中于靶向治疗、免疫疗法、超长效胰岛素等领域。
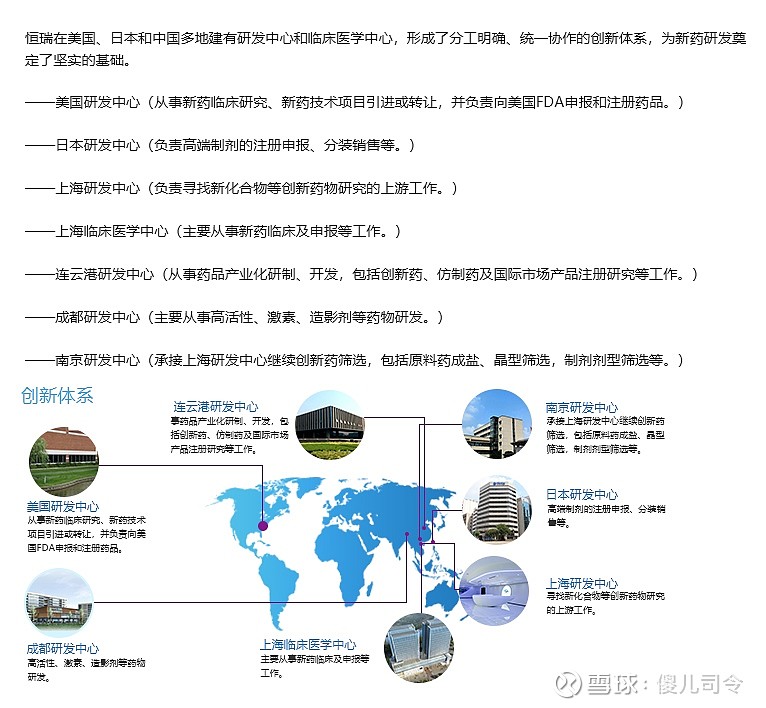
二是研发中心的全球化。为完成全球创新布局,早在2003年恒瑞就投资2亿元在中国上海设立研发中心,其设计、规划、建设等都参照美国第四大生物制药企业Chrion研究中心的标准。在2005 年, 恒瑞投资300万美元成立了恒瑞医药(美国) 创新药物研究公司,主要从事创新药研发和ANDA、API美国市场准入及销售业务。如今,研发中心遍及中国、美国、日本、德国、澳大利亚等地区。在国内,南京、成都、 苏州研发中心相继成立,最终形成了在上海、南京、成都、苏州、连云港等地相互补充、相互促进、相互协作的完整创新体系。这些研发中心承担了包括临床研究、药品产业化、国际市场产品注册、新药技术引进或转让等任务。
三是销售创新,强大的销售分线。恒瑞的产品基本上都属于处方药。处方药无法通过广告形式进行宣传,其使用依赖于医生的选择。因此,对于恒瑞来说,其主要营销对象是医生。主要的营销方式为学术推广: 通过学术研讨会、科室会议等方式,将产品介绍给医生,让医生更清楚地认识和了解产品而达到推广的效果。在过去,恒瑞医药在不同地区设立营销分支机构,统管所有产品的推广与销售。例如A销售机构负责南京地区,那么A销售机构将统管恒瑞旗下所有药品的推广与销售。随着恒瑞医药的不断发展,产品线越来越丰富,分支机构的少数销售人员无法掌握如此庞大的产品信息,医生无法从营销人员口中得到相对专业的信息,只能听营销人员泛泛而谈。为了解决这一困境,恒瑞医药在销售上进行了创新,实施了销售分线制度。销售分线是指将恒瑞医药旗下各种产品根据药品的适用症状进行分线,组成不同的销售团队,统管该类产品在全球的销售。目前,恒瑞产品主要集中在抗肿瘤药、麻醉制剂、心脑血管常发病药以及造影剂四大领域。根据分线的原则,对于不同领域的药品由不同的营销人员负责。而营销人员接受更专业、更具有针对性的培训,充分了解该产品线系列产品的作用机制、效果、副作用、适用情境,从而可以更好地为被营销者—— 医生等人员提供专业化建议。为此,恒瑞医药扩充了其销售队伍,涉及各条产品线,形成了专业、规范、有序的销售体系,为产品销售提供了可靠保障。
四是质量管理创新,强大的质量管理体系。品质是恒瑞的生命。药品关系人的生命健康,任何问题都会让一个医药企业遭受灭顶之灾。国际药品质量规范最高标准是美国FDA 制定的。恒瑞是第一家通过美国FDA认证的中国医药企业。恒瑞的各大生产基地均以美国FDA标准进行设计和建设,以FDA标准来保证生产质量,并引进了一批世界先进水平的生产设备保证生产的精度与纯度,每一个生产步骤都可以追责到个人,从而在制度和硬件上保证药品的高品质。在人员设置上,恒瑞在品质控制(QC)和品质保证(QA) 上的人员投入占公司总人数的27%,远远超过国内业内 20%的平均水平。在药品质量管理方面,恒瑞除了采用美国FDA标准,在产品售后上也建立了一套称为“上下可追溯”的质量追踪机制:通过这个机制,恒瑞可以快速对出现质量问题的产品进行排查。对于药品来说,存在不良反应是常见的事,但弄清楚不良反应究竟是药品成分所致, 还是药品在生产中存在的质量问题所致,亦或是个例患者出现的个别现象,这都需要公司的质量管理人员加以甄别。若因为药品成分或者生产质量失控出现问题,对于医药企业来说将会是致命打击。即使不良反应不是药品成分和质量的问题,若无法快速排查不良反应产生的原因,在此情况下医生不敢用药,药品的推广销售则会受到极大的阻碍。同时,公众舆论也会对产品质量产生怀疑,莫须有的揣测将严重损坏企业声誉形象。
阿帕替尼是恒瑞医药第二个获批上市的I类创新药,但患者在使用过程中曾出现过不良反应,而恒瑞的“上下可追溯”的质量追踪体系在一系列危机事件中发挥了至关重要的作用。恒瑞医药研发部总监骆梅曾回忆说:“当阿帕替尼刚打入市场时,河南省曾发生患者服用阿帕替尼后产生头疼的不良反应等问题。恒瑞接到反馈后,便立即通过质量追踪体系排查服药后出现副作用的原因。通过对全国各地患者服药后不良反应的总体调查,发现仅仅在河南极少部分地区有出现头疼反应的症状,从而排除了药品本身成分上对人体有害的可能性。再通过对生产批次的排查,恒瑞发现销往全国各地的同一批阿帕替尼仅在河南出现头疼症状,从而排除了生产上出现质量失控的可能性。通过两次质量追踪,恒瑞快速排除了产品本身存在质量问题的可能性,把不良反应定性为由于个人体质差异所引起,从而打消了医生与患者的顾虑,使药品的销售继续顺利进行下去。”
路当平处经行稳,创新腾飞乃久致远。多年来恒瑞始终坚守着初心,无论是创新药还是仿制药的研发都取得了很大进展。通过一系列的战略转型,恒瑞从一个生产红药水、紫药水的低端制药厂,通过仿制药与创新药“两只脚走路”的战略,目前已经成长为我国医药行业的领头羊。在恒瑞2019年232.89亿元营业收入中,已经上市的创新药占比近21%,其中阿帕替尼约营收23亿元,艾瑞昔布约3亿元,吡咯替尼约8亿元, 卡瑞丽珠单抗约10亿元,硫培非格司亭约5亿元,其余收入来自于仿制药。随着已经获批上市的5类创新药于2019年全面进入市场,并且今后逐年新增获批2-3种创新药,到2021年将有10种创新药,恒瑞创新药销售占比将逐年上升,在未来的4-5年内甚至可能超过仿制药,从而真正形成优质低价的“仿制药”+具备核心优势的“创新药”共同发展的布局。
未完待续.....
@今日话题 $恒瑞医药(SH600276)$ $爱尔眼科(SZ300015)$