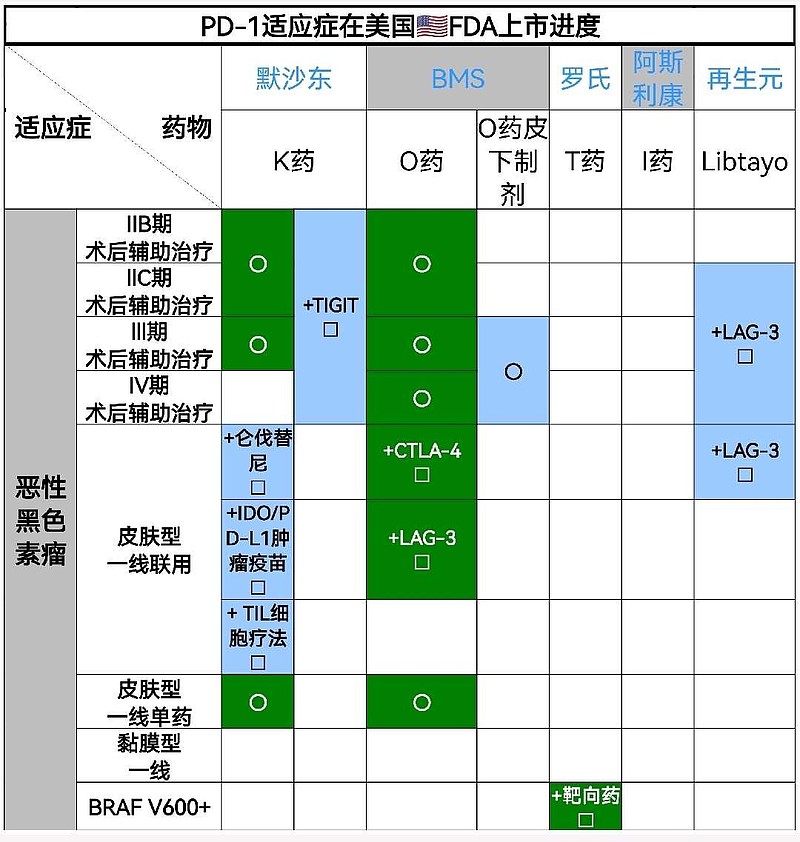
(一)LAG-3单抗2/3期临床历时5年时间,PFS数据读出获FDA批准上市,美国价格出炉,>18万元/月
百时美施贵宝,将O药(Nivolumab 480 mg)和Relatlimab (LAG-3单抗)160mg固定剂量抗体组合,以Opdualag这一名称进入美国🇺🇸市场,售价为27389美元/针。
由于黑色素瘤一线治疗国际多中心3期临床,每4周一次使用Opdualag,无进展生存期PFS=10.1个月。
Opdualag每年(10个月)费用高达188万元RMB,远远高于O药单药100万元RMB的美国🇺🇸年费用水平,60万元RMB的中国🇨🇳HK年费用水平。
百时美施贵宝预计Opdualag到2030年销售额可以高达40亿美元(275亿元RMB)。
(二)美国也有药价谈判,LAG-3单抗从2034年降价
2022年8月,美国通过了《降低通胀法案》(IRA)。该法案旨在通过减少联邦赤字,其中也涉及处方药的降价。
具体来说,该法案赋予Medicare对某些缺乏竞争药物价格的进行谈判权力,同时约束那些Medicare名单内提高产品价格快于通货膨胀率的制药商。
从2023年开始,Medicare可每年针对上市9年(小分子药物)或12年(生物药)以上、且不存在仿制药或生物类似药的原研药,与药企展开药价谈判。
意味着,从2034年开始,LAG-3单抗(Opdualag)就可能会在美国🇺🇸市场大幅降价。
(三)需要OS数据读出,也需要避开美国药价谈判,百济神州LAG-3单抗在美国自主定价生命周期可能只有4年?
2021年5月19日,CheckMate-067试验的6.5年数据公布,该研究在先前没有接受过治疗的晚期黑色素瘤患者中开展,评估了抗PD-1疗法Opdivo(nivolumab,纳武利尤单抗)联合抗CTLA-4疗法Yervoy(ipilimumab)、Opdivo单药疗法、Yervoy单药疗法用于一线治疗的疗效和安全性。
随访结果为,Opdivo+Yervoy双重免疫疗法在黑色素瘤治疗中具有长期生存益处,6.5年的生存率为49%,中位总生存期达到了72.1个月(Opdivo单药仅为36.9个月;Yervoy单药仅为19.9个月),是3期黑色素瘤临床试验中最长的总生存期。
如果OS数据读出,才能获得美国FDA批准上市,$百济神州-U(SH688235)$ 从去年才开展(维立志博)LAG-3单抗的1期临床试验,上市时间可能要到2030年了,百济神州的#LAG-3生命周期太短了#。 。
(四)再生元制药LAG-3单抗,黑色素瘤3期临床直接头对头对照默沙东K药,通过适应症差异化竞争,避开Opdualag。
而对于$再生元制药(REGN)$ 的LAG-3单抗Fianlimab,已完成的一项1期临床试验可以看出,其联合自家PD-1西米普利单抗在既往未接受PD-1/PD-L1抗体治疗的黑色素瘤患者中,ORR达到62.5%,mPFS可达到14.2个月。目前,两项在进行的3期临床,对照组均设置了默沙东K药,直接选择挑战一线和辅助的黑素瘤标准治疗方案。
(五)君实生物打算在美国🇺🇸开展BTLA单抗3期临床,二线治疗复发/难治性淋巴瘤
$君实生物-U(SH688180)$ 已经说了,打算在2023年6月在中国🇨🇳美国🇺🇸,开展#国际多中心3期临床# ,PD-1单抗联合BTLA单抗,二线治疗复发/难治性淋巴瘤。
美国癌症学会、美国国家癌症研究所每三年一次,使用来自SEER的肿瘤登记数据来统计估算美国的癌症患病率。美国当地时间2022年6月23日(即中国时间24日),这一估算结论形成了一篇论文,发表在CA Cancer J Clin上。与诸位分享。
淋巴瘤,估计美国🇺🇸现有22.904万霍奇金淋巴瘤及84.555万非霍奇金淋巴瘤存活患者,预计2022年新诊断的患者分别为0.854万和8.047万,近一半发生在40岁之下,可谓是年轻癌。
BTLA单抗,只有君实生物首先研发,first-in-class,这个市场潜力很大很大。
推算过程很简单,每年1万例淋巴瘤患者使用BTLA单抗,BTLA单抗假设定价20万美元/年,每年新增20亿美元销售额。
尽管BTLA显示出不俗的潜力,但目前靶向BTLA的在研药物很少,中国🇨🇳创新药企仅仅君实生物迈入临床试验。靶向BTLA的药物进展如下:
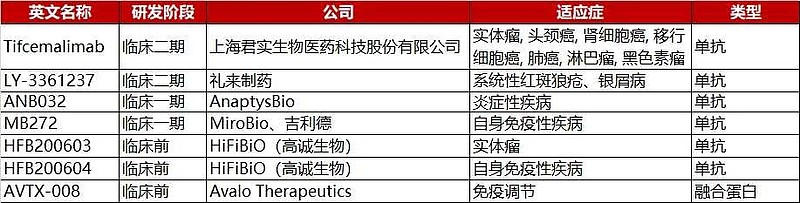
@今日话题 @招财小黄鸭 @Rich_唐 @实干兴国 @生煎只爱大壶春