(一)君实生物VV116
该项3期临床研究,采取的是800例大样本、单盲、随机、与辉瑞特效药Paxlovid头对头对照试验。
从临床数据看,$君实生物-U(SH688180)$ VV116比辉瑞Paxlovid的优势非常明显。
VV116(JT001)组,对比paxlovid,中位至持续临床恢复时间更短,达到统计学优效,为该疗法可加速COVID-19症状缓解提供了有力的证据。
目前为止,上海多中心3期临床已经完成7个月时间了,CDE仍然没有批准VV116上市。
(二)默沙东莫努匹韦Molnupiravir
Molnupiravir是全球首款口服抗新冠病毒药物,由默沙东与Ridgeback生物治疗公司共同开发。该药最初并非针对新冠而研发,其本身是一款广谱抗病毒药物。刚开始是针对委内瑞拉马脑炎病毒(VEEV)而开发,后来被用于流感病毒、呼吸道轮状病毒等多种病毒的治疗。
药物作用机制,作为一种核糖核苷类似物的前药,Molnupiravir的作用机制不是直接消灭或抑制病毒,而是“诱骗”病毒,通俗地说,就是药物会诱导病毒RNA聚合酶和自己结合,进行错误复制(突变),最终合成没有感染性的假病毒。
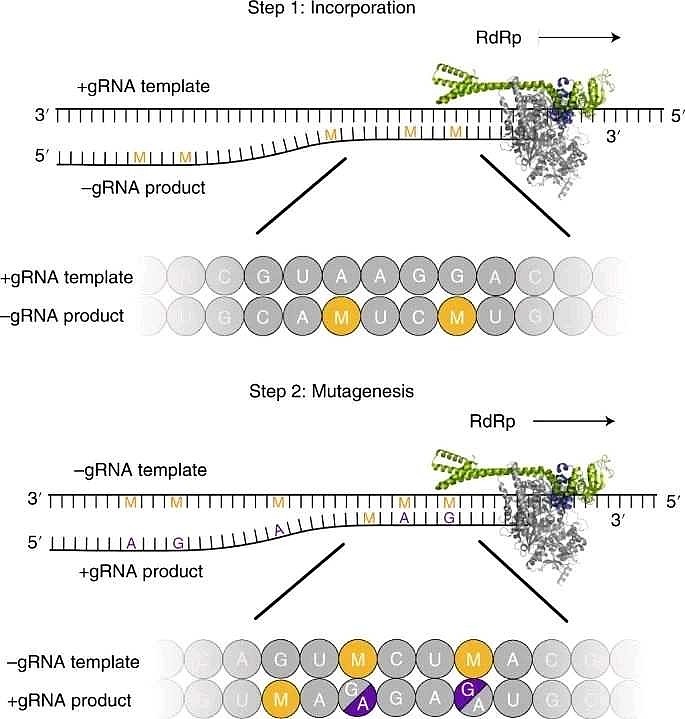
该药物的作用机制决定了,需要在感染早期服用,才能取得较好的效果。
根据默沙东于2021年10月1日发布的新闻稿,在3期临床研究的积极中期分析中,与安慰剂相比,Molnupiravir将轻度或中度新冠患者的住院或死亡风险降低了大约 50%。
使用Molnupiravir进行早期治疗可降低未接种新冠疫苗的高危成人住院或死亡的风险。[4]
不过,根据2021年11月30日FDA药物咨询委员会会议上披露的数据,Molnupiravir的有效性出现了不小的下滑:从中期的50%下降到了30%。
Molnupiravir在安全性上最大的争议,不是来自服药后的腹泻、恶心、头晕等不良反应,而是来自药物的根源:作用机制。
前面说过,Molnupiravir的作用机制在于诱导病毒的RNA进行错误复制(突变),因而随之带来的风险是:人体细胞的突变风险。
由于胎儿和未成年人体内的大量细胞处于分裂中,所以Molnupiravir应被限制在孕妇和未成年人人群使用。
(三)辉瑞帕洛韦德Paxlovid
Paxlovid由大名鼎鼎的辉瑞制药生产,风头完全盖过了比它更早上市的Molnupiravir,甚至在一段时间成了“新冠特效药”的代名词。
和Molnupiravir的“诱导突变”不同,Paxlovid的作用机制简单直接。
我们知道,Paxlovid是由利托那韦和奈玛特韦组成的复合药。
利托那韦并不是一种新药物,早就以抗艾滋病药物的身份享誉十数载,利托那韦能够破坏病毒中酶的正常功能,使病毒无法完成组装和释放。
而奈玛特韦则是新冠病毒主要蛋白酶Mpro的拟肽类抑制剂,能够让Mpro无法处理多蛋白前体,从而抑制新冠病毒在人体内的增殖。
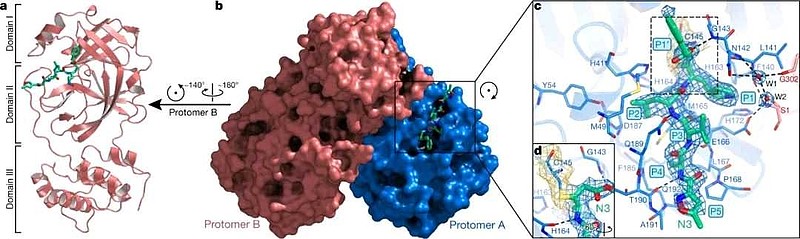
2021年11月5日,辉瑞发布了一项研究,宣称在第二和第三期EPIC-HR(指对高危患者的新冠肺炎的蛋白酶抑制进行评估)临床试验的中期分析中,新型抗新冠口服药Paxlovid将住院或死亡风险降低了 89%。
该项研究同样采取的是大样本、双盲、随机、安慰剂对照试验。
从临床数据看,Paxlovid比Molnupiravir的优势非常明显。
那么,在真实世界中,二者的表现如何呢?
今年10月8日,《柳叶刀》发布了一项中国香港关于两款新冠口服药Molnupiravir和Paxlovid对治疗奥密克戎感染有效性的真实世界研究。

在研究中,研究者分析了2022年2月26日至6月26日期间,11847名服用过Molnupiravir或Paxlovid患者的记录,他们大多都属于新冠感染的高危人群——年龄超过60岁,且未完成疫苗接种。
研究发现,Molnupiravir治疗组的全因死亡率为17.9/100000人日,相比对照组降低了24%;Paxlovid治疗组则为4.2/100000人日,相比对照组降低66%。
Paxlovid完胜Molnupiravir,
反而可以间接证明$君实生物-U(SH688180)$ VV116的优秀。
(四)真实生物阿兹夫定
与Molnupiravir和Paxlovid一样,阿兹夫定也是“老药新用”。
阿兹夫定是由郑州大学常俊标教授作为发明人研发的抗HIV病毒药物,于2013年获批开始进入临床试验。2021年,阿兹夫定作为抗艾滋病药物获批上市。
2022年7月,阿兹夫定获得国家药监局紧急附加条件批准,成为中国紧急批准授权使用的唯一一款国产新冠肺炎(普通型)口服药。
阿兹夫定的作用机制和Molnupiravir相似,都是通过“诱骗”RNA病毒与自己结合来抑制病毒的复制。
阿兹夫定的发明者常俊标教授说:“如果把RNA病毒复制比作盖房子,核苷酸是原材料。阿兹夫定就是一种劣质的原材料,可以诱骗RNA病毒用来盖房子,劣质原材料盖起来的房子会倒塌,这样也就使得RNA病毒无法复制。”
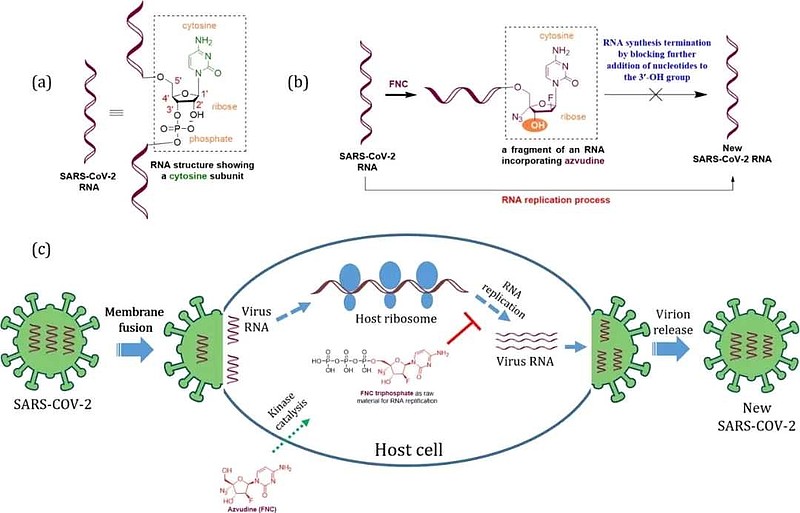
作为首款被批准的国产抗新冠口服药,阿兹夫定目前尚未在学术期刊上公开关于新冠治疗的研究数据,我们只能从其生产厂家真实生物的IPO申请文件和药物试验登记网站获得其三期临床试验部分信息。
从真实生物的IPO申请资料,我们了解到:
在俄罗斯开展的314名中症新冠患者研究中,在第7天时,用药组40.43%的患者症状有改善,而安慰剂组只有10.87%,显示了阿兹夫定的疗效。
不过,阿兹夫定的疗效也受到学术界和医药圈的疑问,包括:
数据主要来自商业属性浓厚IPO文件,缺乏来自学术期刊的研究,导致不但试验数据不足,且有部分数据存疑。试验样本太少,例如,俄罗斯的试验只招募了314人,巴西的试验只招募了180人。作为对比,Paxlovid的三期临床试验招募了2246名受试者,Molnupiravir的三期临床试验也招募了超过1400人。
不过,相比疗效,最大的疑问来自阿兹夫定的安全性和不良反应。
根据阿兹夫定的上市审评报告,其遗传毒性和生殖毒性不容忽视。
(五)以岭药业连花清瘟胶囊
连花清瘟胶囊同样是“老药新用”。
近期,一则《中医药治疗新冠肺炎无症状感染成果登上国际期刊》的新闻被国内各大媒体竞相转载,文章表示:
一项题为《连花清瘟胶囊治疗新型冠状病毒肺炎无症状感染者的有效性:一项随机、对照多中心试验》的临床研究成果在国际医学期刊《结合医学与补充医学杂志》(《JOURNAL OF INTEGRATIVE AND COMPLEMENTARY MEDICINE》)发表。
研究结果显示:治疗组在14天的隔离观察期间核酸转阴率较对照组提高了81.21%。患者核酸转阴时间较对照组缩短接近一半。此外,治疗组临床症状出现率较对照组下降了47.5%。治疗组转为普通病例的比例也较对照组下降了51.4%。且无记录严重不良事件。揭示了连花清瘟对无症状新冠病毒感染患者的有益作用。
这是这本叫做Journal of Integrative and Complementary Medicine的国际期刊,影响因子是2.381。
目前国内比较优秀的科研工作者,通常会寻求在影响因子5-10甚至更高的期刊上发表论文。例如今年年底,$君实生物-U(SH688180)$ VV116头对头对照Paxlovid的3期临床的论文即将在《新英格兰医学杂志》发表。
可以说,期刊在国际上的影响力很重要。
再看具体内容:
现代医学的临床试验,通常要遵循大样本、双盲、随机、安慰剂对照等原则。为了避免因样本过小导致的误差,大样本是最基础的要求。
而连花清瘟的这次试验有多少受试者呢?

总计120人,服药组和安慰剂对照组各只有60人。
如前所述,阿兹夫定就因为样本过少而遭业界质疑,但好歹也有300多人,而连花清瘟这次试验居然只有120人。
我们知道,按照国际惯例,三期临床试验通常需要招募500-1000名受试者,120名受试者只能达到二期临床试验的规格。
结论
笔者客观陈述,没有结论。