真实生物的新冠药还有悬念,至今没有3期临床数据读出。$新华制药(SZ000756)$ 和$华润双鹤(SH600062)$ 近期不可能有上市利好发生。
根据clinicaltrials.gov官网的公示信息,
(一)新冠重症3期临床
真实生物的阿兹夫定目前已经完成了一项随机、双盲、对照III期临床(NCT04668235),主要评估在中度至重度感染SARS-COV-2的患者中评估阿兹夫定相对于安慰剂的疗效和安全性。

阿兹夫定这项研究只在巴西招募了342例重症患者,远远少于$君实生物-U(SH688180)$ VV116在乌兹别克斯坦招募入组600+例重症患者。

君实生物VV116今年3月启动了治疗中重度COVID19的国际多中心、随机、双盲、对照III期临床研究,目的是在国际多中心的中重度COVID-19受试者中确证性评价VV116对比标准治疗(法匹拉韦)的有效性和安全性,主要终点为截至第29天进展为(危)重型COVID-19或全因死亡的受试者百分比。
(二)新冠轻症3期临床,预计今年7月完成
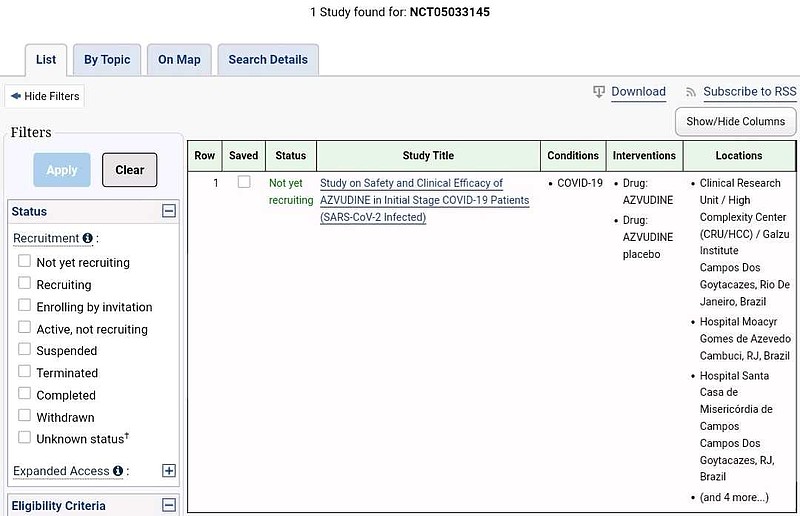
另一项评估阿兹夫定片剂在初始阶段和轻度症状期间治疗COVID-19的有效性和安全性的III临床试验(NCT05033145)预计于今年7月完成。
在巴西开展,#尚未招募入组患者# 。
阿兹夫定的轻症临床试验进度,落后于君实生物VV116中国多中心III期临床试验(VV116已经达到主要临床终点,疗效优于辉瑞Paxlovid)。
阿兹夫定计划招募312例轻症患者,也少于君实生物中国多中心的822例轻症患者。

NCT05341609 研究是一项中国多中心、单盲、随机、对照 III 期临床研究,旨在评价君实生物VV116 对比辉瑞口服药奈玛特韦片/利托那韦片( Paxlovid)用于轻中度 COVID19 患者早期治疗的有效性和安全性。
(三)新冠轻症治疗,才是最大适应症
假设,即使,阿兹夫定依据巴西3期临床试验NCT04668235数据,获批上市的适应症也只是——新冠重症。
新冠重症患者发生率只有0.1%。
#新冠口服药最大市场在新冠轻症治疗# ,预防重症,预防死亡。
君实生物VV116,今年6月1日即将获批的适应症是——新冠轻症。
新冠轻症患者发生率是99.9%。