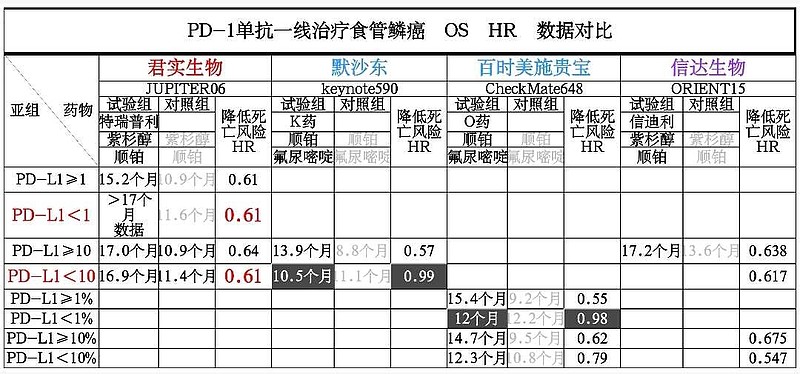
2021年5月,欧洲药品管理局EMA批准——$默沙东(MRK)$ K药+化疗一线治疗 PD-L1 CPS≥10的局部晚期不可切除性或转移性食管癌和胃食管连接部腺癌。
2022年4月,欧洲药品管理局EMA批准——$百时美施贵宝(BMY)$ O药+化疗一线治疗 PD-L1 TPS≥ 1% 无法切除的晚期、复发性或转移性食管鳞癌。
最新,Coherus宣传,特瑞普利单抗+化疗一线治疗PD-L1 CPS<10晚期或者转移性食管鳞癌,是潜在的未满足需求(Potential unmet need)。
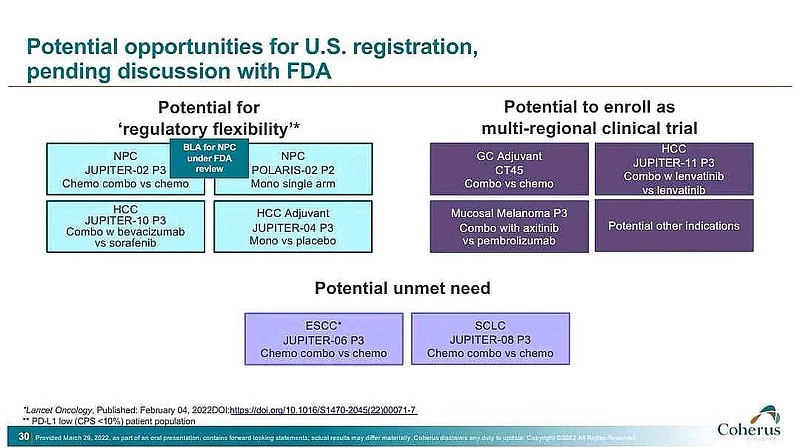
从JUPITER-6研究来看,
PD-L1 CPS<10 亚组,或者PD-L1 CPS≥1亚组,$君实生物-U(SH688180)$ 特瑞普利单抗一线治疗食管鳞癌都取得了OS显著延长的疗效。
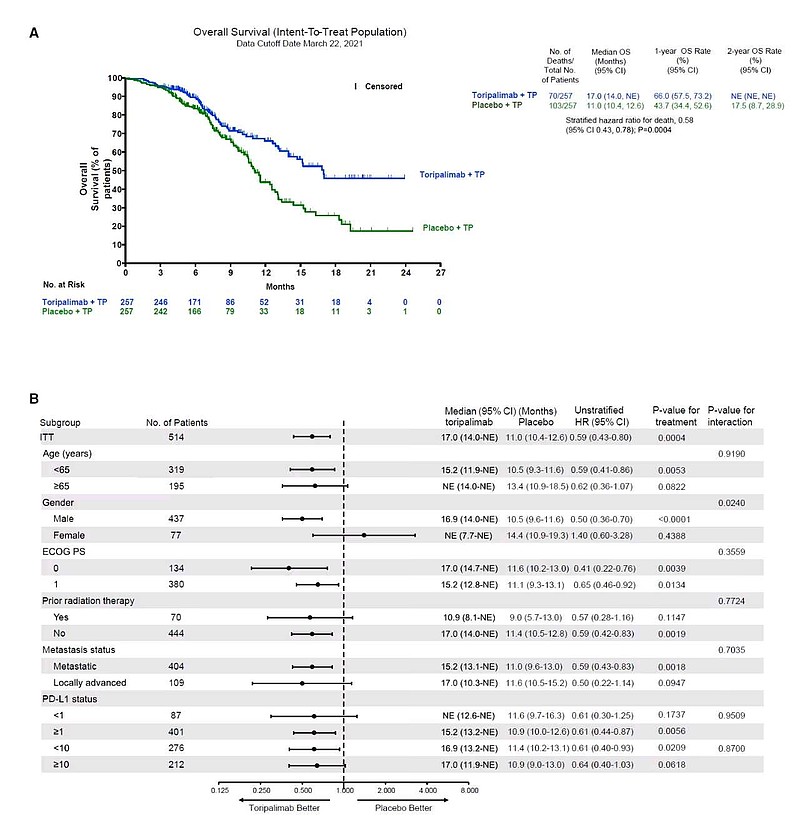
PD-L1 CPS<10 亚组,OS HR=0.61(0.40-0.93),P值=0.0209。
PD-L1 CPS ≥ 1 亚组,OS HR=0.61(0.44-0.0.87),P值=0.0056。