$信达生物(01801)$ PD-1单药二线治疗晚期鳞状非小细胞肺癌适应症,在中国🇨🇳上市申请被NMPA否决,上市失败。
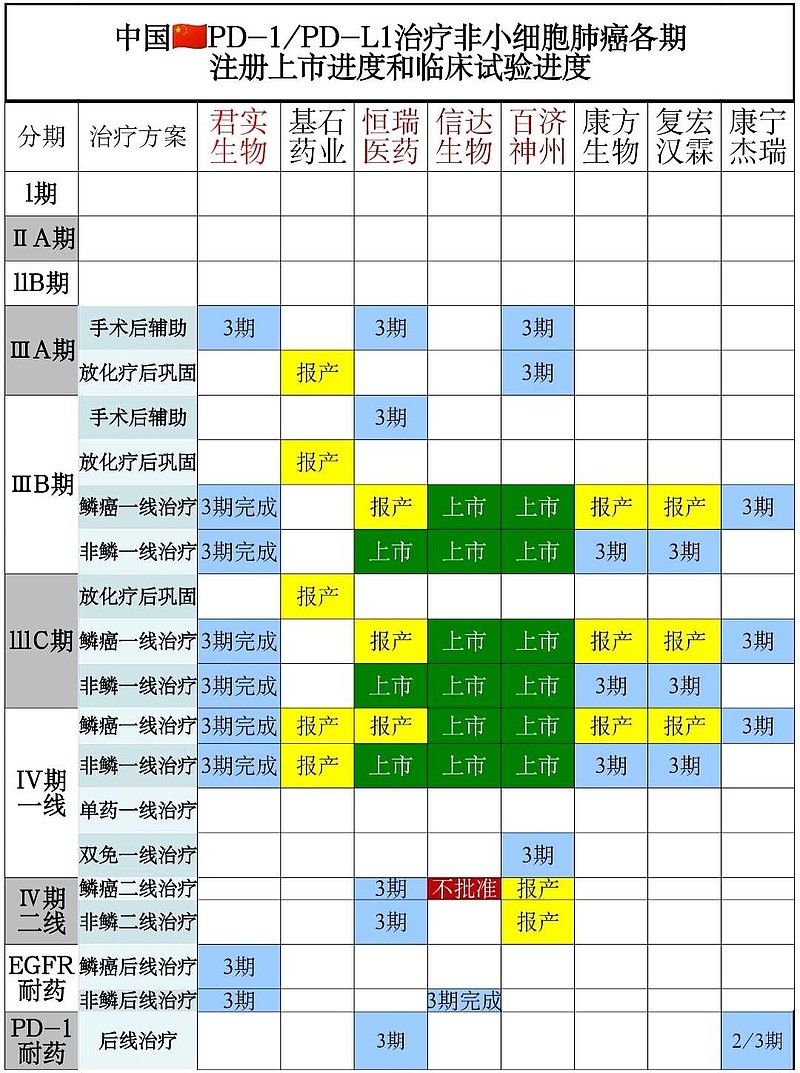
(一)这项上市申请,依据的是ORIENT-3研究(3期临床双臂试验,开放性标签,不是双盲对照试验),临床数据证据不足。
在已经有了每年3万元RMB的PD-1单抗一线治疗方案,显然#不属于未满足的临床需求# 。
(二)信达生物PD-1的鳞状非小细胞肺癌一线治疗,#3期临床数据垫底# 。
非头对头其他药企的临床试验数据,信达生物PD-1的ORR和PFS最低。
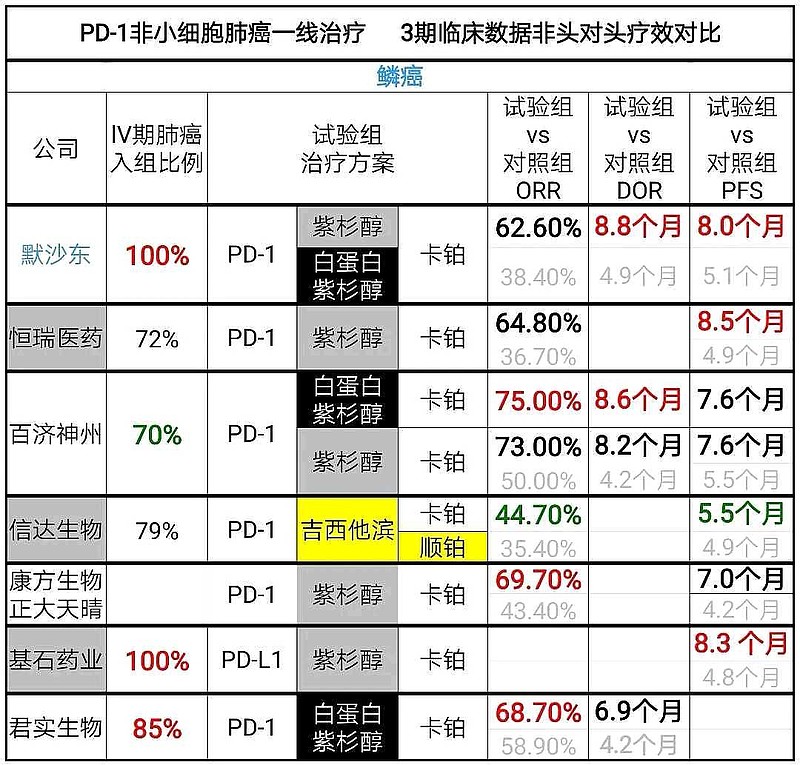
所以,CDE要求信达生物——补充临床试验数据,需要再次招募患者入组。
(三)间接利好,已经开展二线治疗3期临床的$恒瑞医药(SH600276)$ ,$百济神州(06160)$ 。