——加速剥离非核心资产的企业们——
天境生物
2024年2月7日,天境生物(I-Mab)官宣了重大战略调整:中国子公司已与天境生物制药杭州公司达成协议,剥离中国的资产和业务给后者。根据最终协议,天境生物将以无现金和无债务的方式将公司在中国经营业务的全资子公司天境生物医药有限公司的100%已发行股权转让给天境杭州,总对价为人民币等值不超过8000万美元。与此同时,天境生物科技(杭州)有限公司还宣布完成超5亿元人民币C1轮融资。本轮融资由泰珑投资、和达大健康基金、I-Mab、杭州钱塘城发科技服务有限公司、Bruggemoon Limited、宁波开投瀚润资本共同投资。交易完成后,天境杭州将收购天境生物在中国的多款药品资产,承担这些资产所有未来开发成本。截至2月8日收盘,天境生物大跌10%。
对于上述的资本操作,相信即使不炒股的你都能够明白其着实有些大不韪,在经济寒冬期,尤其是在更加凄苦的生物创新药领域,让不少投资机构唾弃。相关的文章已经有很多,本文不想落窠臼,更为关注的是I-Mab保留了哪些资产?I-Mab将保留手头现金,保留包括givastomig(CLDN18.2/4-1BB)、uliledlimab(CD73单抗)和TJ-L14B(PD-L1/4-1BB)在内的所有临床阶段资产的非中国权利,以及保留候选新药相关的大中华区以外的优先谈判权,并继续在纳斯达克上市。
关注天境生物,一定是源自于C47靶点药物研发处在前列,但CD47丨吉利德终止三项III期,亚力兄转战实体瘤,宜明昂科和天境生物悲喜不同一文已经提到过:
天境生物丨Lemzoparlimab(CD47抗体)
2023年9月22日,天境生物宣布艾伯维终止CD47抗体的合作协议,该决定由艾伯维基于此前的项目终止和策略调整所作出。协议终止从11月20日起效,天境生物重获CD47抗体的全球权益,协议终止不影响天境生物已经获得的2亿美元预付款+里程碑金额。Lemzoparlimab目前处于三期临床阶段,与阿扎胞苷联合一线治疗高危MDS。由此,CD47抗体将不再是天境生物的核心资产。
天境生物丨uliledlimab(CD73抗体)
对于CD73靶点药物的关注,源自于疫情期间的相关药物的研发,但在现在,更为关注的是该靶点药物与ICIs的连用探索:
ASCO靶点追踪丨CD73单抗±度伐利尤单抗+化疗治疗胰腺癌
本身也通过搜集天境生物的uliledlimab(CD73抗体),发现其在联合ICIs进行肺癌领域的探索。但鉴于既往的种种表现,在此不表,等具体III期结果。由此,该产品目前的估值只能放低。本人更为关注的是双抗产品是否能够实现双效协同:
天境生物丨givastomig(CLDN18.2/4-1BB)
对于当下的明星靶点,CLDN18.2毫无疑问是必须要布局的,但安斯泰来的单抗已经遭受重挫,进行双抗、CAR-T等技术的迭代,还能把故事继续讲下去。
CLDN18.2双抗丨凡恩世、康方选CD47、信达选CD3,差异分析
CLDN18.2丨信达聚焦ADC,率先申报III期,逆袭单抗
CLDN18.2丨安斯泰来被拒上市,奥赛康、创胜硬上III期
网页链接{GI24丨科济CLDN18.2 CAR-T胃癌/胰腺癌数据解读}
对于该靶点,多篇文章已经表明各个企业都希望能够有所突破。但对于当下阶段的资本市场,更为关注的是成药可能性,厌恶风险。所以,做成4-1BB进行双抗,有些风险性。
免疫激动剂丨4-1BB单/双抗项目进展 一文有汇总过,不再解释。
天境生物丨TJ-L14B(PD-L1/4-1BB)
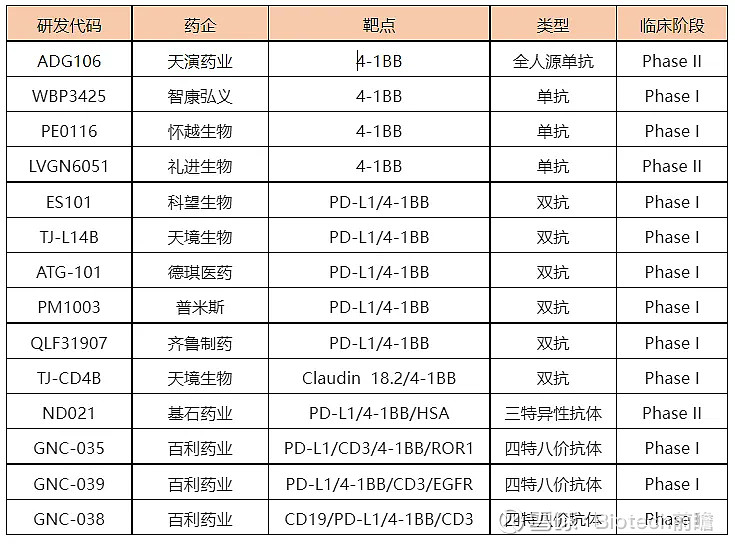
国内部分临床阶段4-1BB在研产品
汇总下来,额,好吧,天境生物的未来,大体确定了。
2024年2月6日,中国生物制药发布公告称,中国生物制药将出售正大青岛67%股权给两位买方,交易总对价约为人民币18.2亿元。这是中国生物制药近半年第二次出售下属公司股份。查询资料发现,对于既往粗犷发展时代积累起来的商业流通分公司及经过多轮杀价导致利润下滑的普药分公司等资产,在加速剥离,回笼资金。但纵观中国生物制药的股价走势,必须得有足够强有力的核心创新药物管线加持,才能获得投资者的信赖。
中国生物制药丨贝莫苏单抗(PD-L1抗体)
2024年2月7日,中国生物制药宣布,集团附属公司正大天晴药业集团股份有限公司开发的「贝莫苏拜单抗 (TQB2450注射液)」已被中国国家药品监督管理局药品审评中心 (CDE) 纳入优先审评审批程序,用于联合盐酸安罗替尼胶囊治疗复发性或转移性子宫内膜癌。贝莫苏拜单抗是本集团自主研发的一款全新序列的创新全人源化抗PD-L1单克隆抗体。
2022年4月,贝莫苏拜单抗联合安罗替尼治疗复发性或转移性子宫内膜癌被CDE纳入突破性治疗品种。2023年1月,贝莫苏拜单抗的新药上市申请获CDE正式受理,用于联合安罗替尼一线治疗小细胞肺癌。
2023年8 月 3 日,中国生物制药与益方生物共同宣布,两家公司就 KRAS G12C 靶向药物 D-1553 达成合作。根据公告,中国生物制药集团下属正大天晴药业集团与益方生物签订许可与合作协议,获得后者 KRAS G12C 靶向药物 D-1553 产品在中国大陆地区开发、注册、生产和商业化的独家许可权。同时,基于未来潜在的数据分享合作,正大天晴还将有权获取一定比例的中国大陆以外地区收益。
而正大天晴将向益方生物支付最高不超过人民币 5.5 亿元的首付款及里程碑款;并按年净销售额向公司分层支付特许权使用费。D-1553(Garsorasib) 拟用于治疗带有 KRAS G12C 突变的非小细胞肺癌、结直肠癌等多种癌症,是国内首个自主研发并进入临床试验阶段的 KRAS G12C 抑制剂,也是首个获得 CDE 突破性治疗品种的国产 KRAS G12C 抑制剂。
但网页链接{FDA拒绝完全批准安进KRAS G12C抑制剂,国内多家企业布局}一文有提到该靶点研发阴影问题。
网页链接{阿斯利康押注KRAS G12D抑制剂,汇总该赛道研究进展} 有企业,不仅是阿斯利康,恒瑞等也在开始尝试新靶点的药物迭代。风险性较高。
21世纪是生物的世纪,曾经以为戏谑的段子却无疑成为当下时代竞逐的主战场之一。既往的宽松时代,有诸多国内学子远渡重洋,选择了生物专业,11年左右兴起的归国热潮,有些人进入大学,有些人进入工业界,借助全球化合作模式的蜜月期,在新兴的肿瘤治疗药物研发领域,与国际竞争中尚可一战。但也是鉴于异军突起导致的王座不稳,拜登政府也开始进行生物技术领域的再审视,既芯片之后的第二个主要封锁的领域。近期发生的几起事件,无疑也验证了看不见却实在存在的铁幕。国内的医疗体系已然重荷超载状态下,如何有效支撑不断涌现的创新药的支付体系,增加企业创新的积极性,无疑是Biotech企业下半场应该考量的重要命题,近期的几家企业的资本操作,毫无疑问是期望能够加速资金回笼,应对危机。
基石药业丨抗PD-L1单抗
2024年3月15日,基石药业宣布舒格利单抗(抗PD-L1单抗)的新适应症上市申请已获得NMPA批准,用于联合化疗治疗PD-L1(CPS≥5)的不可手术切除的局部晚期或转移性胃及胃食管结合部腺癌的一线治疗。该适应症的申请基于GEMSTONE-303研究结果,研究结果显示,GEMSTONE-303研究已达到预设协同主要终点。在PD-L1表达≥5%患者中,与安慰剂联合化疗相比,舒格利单抗联合化疗明显改善了PFS(7.6个月 vs 6.1个月)和OS(15.6个月 vs 12.6个月),且差异具有统计学显著性与临床意义。

此前,舒格利单抗已有4项适应症获得NMPA批准,分别为:
联合化疗一线治疗转移性鳞状和非鳞状非小细胞肺癌患者;
治疗同步或序贯放化疗后未出现疾病进展的、不可切除、III期非小细胞肺癌患者;
治疗复发或难治性结外NK/T细胞淋巴瘤患者;
联合氟尿嘧啶类和铂类化疗药物一线治疗不可切除的局部晚期,复发或转移性食管鳞癌患者。
一直追踪创新药企的商业运营模式,尤其是在日渐合规的环境下,创新产品的适应症内销售显得尤为重要。而基石药业也在经历一系列人事变动之后,在逐步找寻适合自己的商业合作模式。值得一提的是,基石药业已与辉瑞(Pfizer)达成战略合作,其中包括基石药业与辉瑞投资就舒格利单抗在中国大陆地区的开发和商业化等。继KRAS抑制剂、宫颈癌ADC后,再鼎再获O药10省销售权 一文所述,而施贵宝却将旗下核心产品O药的10省销售权转让给再鼎,再回溯君实与阿斯利康就特瑞普利单抗的销售合作,成熟已上市产品的商业合作日渐丰富起来。在2023年3月15日,港股创新药企基石药业(02616.HK)公布了2022年财报数据:基石药业 2022年营收实现翻倍,为4.814亿人民币;商业化收入同比增长142%,达到3.941亿人民币;其中,精准治疗药物销售额为3.64亿元,来自于销售药品阿伐替尼、普拉替尼及艾伏尼布;另外,舒格利单抗特许权使用费收入为2980万元;截至2022年12月31日现金储备为10.42亿人民币。期望能够在有充足循证依据前提下在适合患者人群中展示出创新药的优异疗效,并能在未来出海国外市场奠定扎实基础。百济PD1出海欧盟后再获FDA批准,第二款国产PD1登陆美国。