9 月 20 日,Seagen 和 Genmab 宣布其共同研发的 First-in-class 组织因子(TF)靶向 ADC 产品 TIVDAK™(tisotumab vedotin-tftv)获批上市,用于复发/转移性宫颈癌。这是针对宫颈癌人群首款获批的 ADC 疗法,也是 ADC 巨头 Seagen 获批的第 4 款 ADC 疗法。
本次获批是基于开放标签、多中心、单臂 2 期临床 innovaTV 204 研究的数据(NCT03438396/GOG-3023/ENGOT-cx6) 。这项临床试验在 101 名此前接受过不超过 2 种前线系统疗法、包括至少一种既往含铂化疗方案治疗的复发或转移性宫颈癌患者中评估了 tisotumab vedotin 的疗效。主要疗效指标为 IRC 评估的根据 RECIST v1.1 确认的 ORR 以及 DOR。
结果显示,根据独立审查委员会 (IRC) 使用实体瘤疗效评估标准 (RECIST) v1.1 标准进行的评估,客观缓解率(ORR)为 24%(95% CI;15.9-33.3),中位缓解持续时间(DOR)为 8.3 个月(95% CI;4.2 至未达到)。
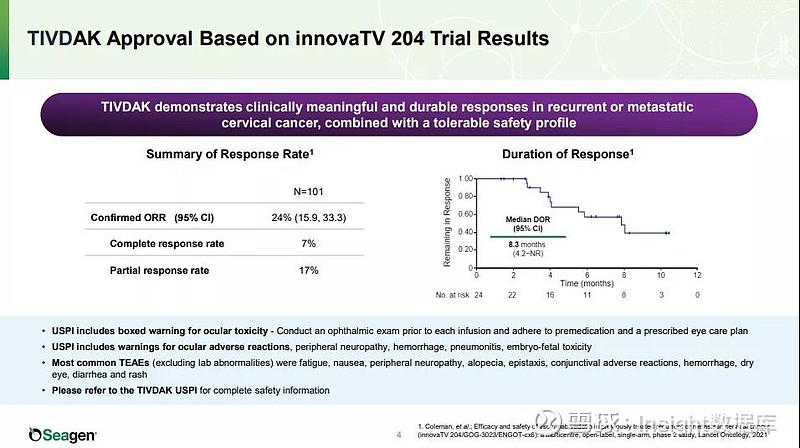
这项批准还包括一项涉及眼部毒性的黑框警告。
TIVDAK 的生物制剂许可申请(BLA)于 2021 年 2 月提交,并于 2021 年 4 月获得优先审评资格。审评历时仅半年多。
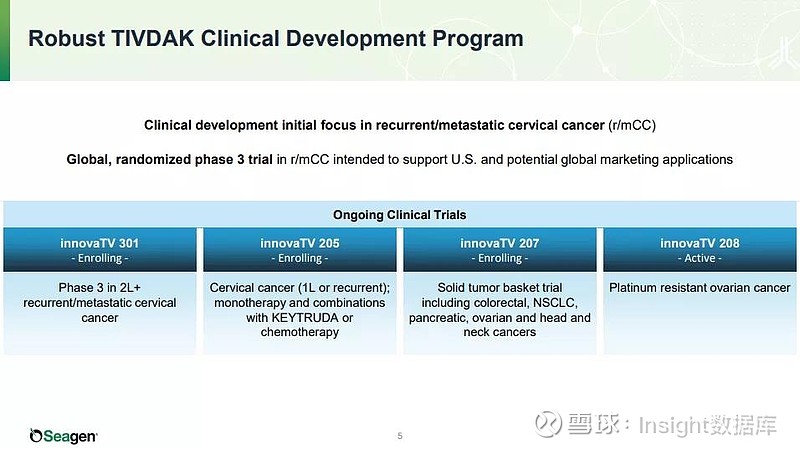
TIVDAK 的临床开发聚焦于宫颈癌。根据 Seagen 官网,目前 TIVDAK 还有针对 2 线以上晚期/转移性宫颈癌的 3 期临床 innovaTV 301 研究、单药或联合 K 药/化疗 1 线治疗宫颈癌的 innovaTV205 研究在进行中,后续还可能针对胆管癌、NSCLC、胰腺癌、卵巢癌、头颈癌进行临床开发。
在 2021 ESMO 上,Seagen 公布了 innovaTV 205 研究中的联合用药疗效数据,详见下图:

在国内,仅乐普生物/美雅珂有同靶点 ADC 产品在研。MRG004A 引进自 Synaffix 公司,已于今年 8 月获批临床。

来源:CDE官网