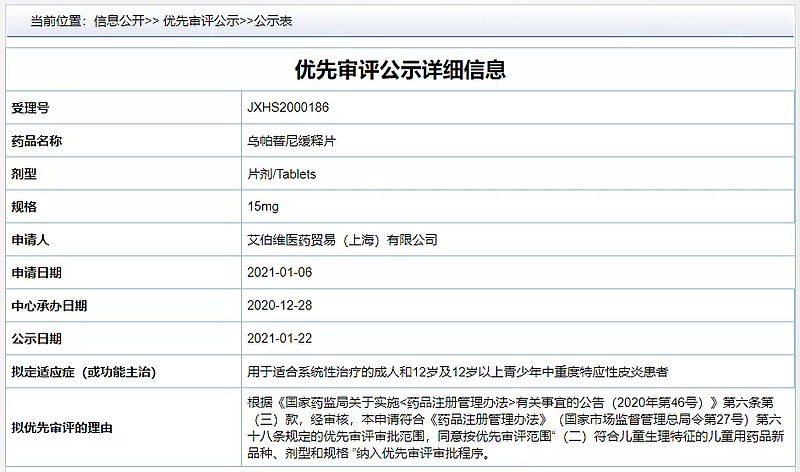
1 月 22 日,CDE 官网显示,艾伯维的 JAK1 抑制剂「乌帕替尼缓释片」拟优先审评,用于 12 岁及以上青少年或成人中重度特应性皮炎。
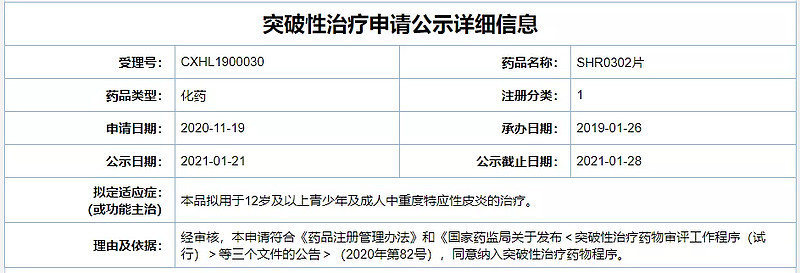
同日,恒瑞子公司瑞石生物的 JAK1 抑制剂 SHR0302 也被纳入拟突破性疗法认证,其适应症同样为:12 岁及以上患者中重度特应性皮炎的治疗。
JAK 是细胞质酪氨酸激酶家族的一员,包含 JAK1、JAK2、JAK3、TYK2 这 4 种亚型。其中,JAK1 在免疫介导的疾病的病理生理过程中发挥重要作用。
艾伯维的乌帕替尼是一种每日口服一次,选择性和可逆性 JAK1 抑制剂。2019 年 8 月,该药首次获美国 FDA 批准,治疗对甲氨蝶呤反应不足或不耐受的中重度活动性类风湿关节炎成人患者。2020 年 10 月,其已向 FDA 和 EMA 递交针对特应性皮炎的上市申请;同年 12 月,艾伯维向 NMPA 递交上市申请并获受理,今日拟纳入优先审评审批。
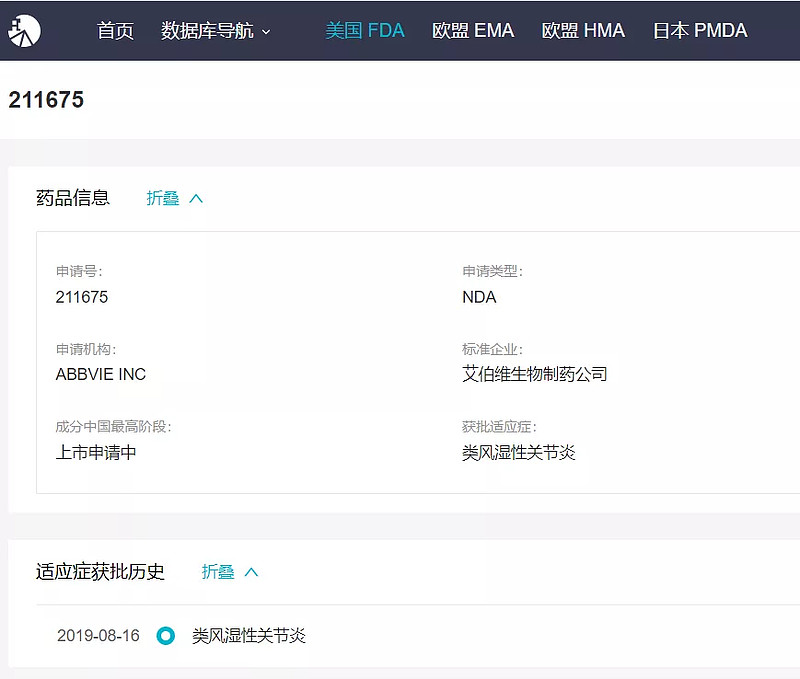
来自 Insight 数据库(网页链接)
乌帕替尼在国外递交的中重度特应性皮炎适应症上市申请是基于 3 项关键性 III 期临床研究 Measure Up 1(单药)、Measure Up 2(单药)和AD Up(联合TCS)的结果。三项临床结果都显示,治疗 16 周后 30mg 和 15mg 的乌帕替尼组在改善皮损状态和减轻瘙痒方面均显著优于安慰剂组,达到双重主要临床终点及次要临床终点。
SHR0302 是瑞石生物自主研发的一款高选择性 JAK1 抑制剂,可通过抑制 JAK1 信号传导发挥抗炎和抑制免疫的生物学效应。此前,其针对特应性皮炎的 II 期临床研究已达到主要终点及次要终点。
(Insight 往期报道:恒瑞 JAK1 抑制剂 II 期临床达到主要研究终点,将启动 III 期临床)
根据 Insight 数据库,SHR0302 共有 2 种剂型处于临床研发中,分别是片剂和软膏剂,均进展至 III 期临床,不过在研适应症各有不同。片剂(即本次拟突破性治疗的剂型)在研适应症较多,包括类风湿性关节炎、强直性脊柱炎两项已进入 III 期临床的适应症,以及斑秃、克罗恩病、溃疡性结肠炎、特应性皮炎 4 项最高处于 II 期临床。
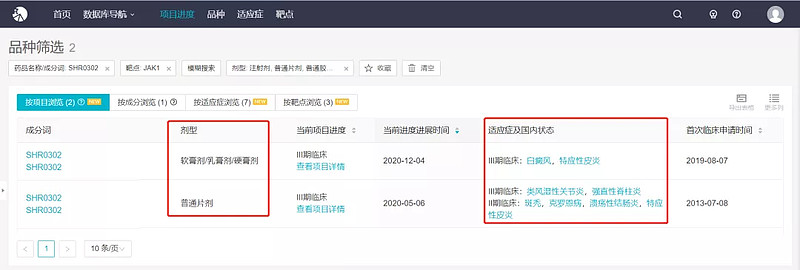
来自 Insight 数据库(网页链接)
目前,国内尚无 JAK1 抑制剂获批用于特异性皮炎。恒瑞和艾伯维的 JAK1 抑制剂在获 CDE 认可后,将加速开发/审评,为相关患者提供更好的治疗选择。
Insight数据库新功能上线,轻松了解目标项目竞争详情。点此免费试用→网页链接