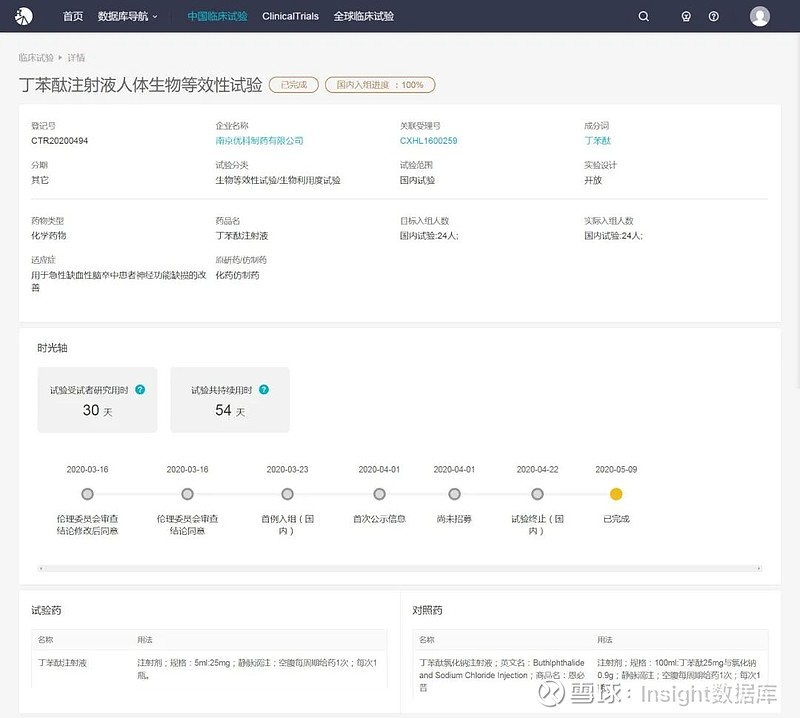
6 月 2 日,CDE 官网显示,南京优科丁苯酞注射液以注册分类 2.2 类递交上市申请获 CDE 承办,用于急性缺血性脑卒中患者神经功能缺损的改善。

早在今年 4 月份,Insight 数据库显示,南京优科启动了丁苯酞注射液的人体生物等效性试验,对照药就是石药的恩必普(丁苯酞氯化钠注射液),目前显示已完成状态。
图片来源:Insight 数据库(网页链接)
丁苯酞,是在 1978 年由中国医学科学院药物研究所首次从水芹籽中分离得到,1980 年首次化学合成了丁苯酞。分为左旋丁基苯酞、右旋丁基苯酞以及消旋丁基苯酞三种主要结构。
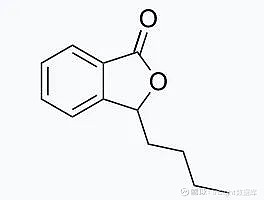
丁苯酞化合物结构(来源:维基百科)
2002 年 9 月,石药集团丁苯酞软胶囊(商品名:恩必普)取得新药证书及试生产批件,2005 年正式上市,成为继青蒿素和双环醇之后中国第三个拥有自主知识产权的创新药物,主要用于治疗用于治疗轻、中度急性缺血性脑卒中。
丁苯酞口服常释剂型在 2009 成功纳入年版国家医保目录,2010 年销量实现大幅增长;同时 2010 年 4 月,石药丁苯酞氯化钠注射液获批上市,用于急性缺血性脑卒中患者神经功能缺损的改善,极大丰富了产品管线。
2017 年,丁苯酞氯化钠注射液成功纳入国家医保目录,为注射液抢占脑卒中治疗的急救期用药和软胶囊恢复期用药的序贯治疗推广起到了积极的拉动作用。据 IVQIA 数据显示,恩必普两个剂型 2017 年共实现销售额 29 亿,其中软胶囊 14 亿,注射液 12.8 亿,注射液成为恩必普市场放量的强劲动力。
石药集团正在拓展恩必普的新适应症,企业公开数据表示丁苯酞正在进行的研究项目共 134 项(基础 69 项及临床 65 项);Insight 数据库显示,丁苯酞软胶囊用于治疗血管性痴呆的 Ⅲ 期临床研究在 2019 年 12 月首次公示信息,目前正在患者招募中,拟入组国内患者 700 人。
图片来源:Insight 数据库(网页链接)

此外,石药的丁苯酞注射液在 2014 年报上市,至今并未获批。Insight 数据库显示,南京优科和珠海保税区丽珠合成制药公司在 2017 年申报了丁苯酞原料药上市申请,目前正在补充资料审评中,预计今年有望获批。
图片来源:Insight 数据库(网页链接)

南京优科申报的 2.2 类丁苯酞注射液在 2019 年 10 月获批临床,2.2 类是指含有已知活性成份的新剂型(包括新的给药系统)、新处方工艺、新给药途径,且具有明显临床优势的制剂。本次南京优科首家以恩必普(丁苯酞氯化钠注射液)为对照药开展生物等效性研究,且首家报上市,对于石药恩必普来说是个潜在的危险。
据公开数据显示,恩必普是石药集团的拳头产品,2019 年销售额达到 56 亿元,同比增长 35.8%,占集团总营收的 25% 左右。据了解,石药集团没有丁苯酞的化合物专利,该化合物用于急性缺血性脑卒中的专利已于 2019 年到期。为了保住恩必普的市场地位,石药还开发了丁苯酞片、左旋丁苯酞片、左旋丁苯酞注射液,目前均已获批临床;此外,丁苯酞软胶囊在美国的 II 期临床试验已入组 112 例。
新适应症及新市场的不断开发将为恩必普带来新的增长机会,目测短期内其他企业难以撼动其市场地位;但是独家大品种总是会面临仿制药的冲击,如何通过适应症拓展、推出改良新品等方式维持专利药的利润将是企业面临的另一巨大挑战。

点击阅读原文
微信申请试用 30 天
