编译丨Jim
编辑丨于靖
过去的两个月里,医生们一直在争论一种备受关注的阿尔茨海默病药物临床试验结果出人意料的积极意义。但他们几乎没有什么进展,只知道叫做lecanemab的药物对接受治疗的患者有多大的好处。
Lecanemab的开发公司卫材和渤健,在9月下旬发布的一份新闻稿中透露,与安慰剂相比,这种药物可以将患者智力和身体衰退减缓27%,不过几乎没有分享其他更详细的数据。
11月30日晚上,负责这项临床的研究人员拉开遮挡的帷幕,在《新英格兰医学杂志》(The New England Journal of Medicine)上发表了完整的研究结果,并在旧金山举行的年度阿尔茨海默病临床试验大会(CTAD)上公布他们的研究结果。
新的数据证实两家公司9月份的声明,确认lecanemab是同类药物中第一个在后期临床中明显获得成功的药物。然而,对于lecanemab的副作用,以及它们是否值得迄今为止看到的获益,仍然存在疑问。
如果FDA像目前预期的那样,在明年初批准lecanemab的使用,那么阿尔茨海默病领域的医生和专家们如何看待这些数据,将大大有助于确定该药是否最终被应用到实际治疗中。
三年前,在CTAD,渤健未能消除医生对其早期阿尔茨海默病药物aducanumab的许多疑虑,导致2021年6月FDA备受争议地批准其以Aduhelm的商品名上市时,对医疗机构对开具它的处方的兴趣不温不火。此后,渤健放弃了在美国销售这种药物的努力。
“在2019年举行的CTAD会议上,我对aducanumab感到非常沮丧和怀疑。”西奈山医学院阿尔茨海默病研究中心主任玛丽·萨诺(Mary Sano)说,“我确实希望人们明白,尽管lecanemab不是万能药,但它有着显著的不同。”
与渤健合作研究Aduhelm的卫材认为,lecanemab是治疗许多早期阿尔茨海默病患者的一种有效方法,也是一种潜在的重磅产品。CTAD上的展示和NEJM上的发表都是向医学界证明这款新药的主要证据。
01 卫材/渤健更新了哪些信息?
卫材和渤健在9月份的新闻发布会上,描述了所谓的顶线结果,透露该试验达到其主要和次要终点,并总结报告的副作用。
这些信息足以使lecanemab成为几十年来临床试验中出现的最有前途的阿尔茨海默病药物,并为卫材和渤健的市值分别增加了数十亿美元。
《新英格兰医学杂志》的论文,详细列出全部数据结果,它们是FDA在做出批准决定时将仔细研究的内容,以及医生开局相关处方的依据。根据这些结果,在研究人员用于评估患者认知能力和功能能力的四个评分量表上,给予lecanemab的患者经历明显较慢的下降。值得注意的是,用于计算组间差异的统计方法在每项测量中都强烈倾向于lecanemab。
该数据还显示,在研究的主要指标——18分的临床痴呆评分量表(CDR-SB)中,接受lecanemab的患者与接受安慰剂的患者间的差异,随着时间的推移而扩大。由于lecanemab是一种长期服用的药物,因此在为期18个月的随访试验中,越来越多的益处,可能表明疾病的进程可能发生更实质性的变化。
此外,研究作者写道,用于衡量数据对其他变量的敏感性的分析,与主要终点的主要发现基本一致。进一步的亚组数据显示,在用于在药物和安慰剂之间随机分配参与者的各种标准中,如通过使用其他阿尔茨海默病药物、遗传风险因素和所在地区,都一致倾向于lecanemab。
CTAD的报告结果同时发表在NEJM上,这让lecanemab与渤健处理Aduhelm数据的方式形成对比——该研究直到药物批准后的2022年3月,才发表在同行评审的医学杂志上,距离该数据在CTAD上首次报告已有两年多。
今年的CTAD上,lecanemab的研究者在五个系列报告中展示他们的发现。
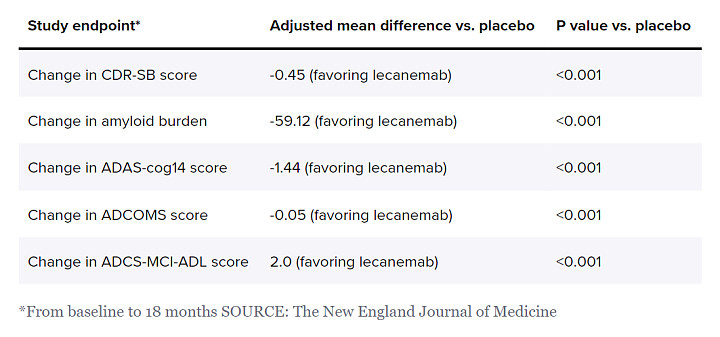
来自卫材、渤健lecanemab三期研究的主要和次要终点结果
02 Aβ蛋白数据能否支持获益?
就像Aduhelm和许多其他实验性阿尔茨海默病药物一样,lecanemab被设计成与一种叫做β淀粉样(Aβ)蛋白的蛋白质结合。
研究表明,这些蛋白质通常在大脑中提供有益的功能。但有时候,它们会错误地折叠,随着时间的推移,它们聚集在一起,形成一种粘性的、有毒的斑块。长期以来,人们一直相信这种斑块在阿尔茨海默病的发展过程中起着关键作用。
渤健和卫材注意到,lecanemab似乎对β淀粉样蛋白的一种形式,即“可溶性原纤维”,具有特定的亲和力。一些人认为,这种形式对神经元的毒性比其他形式更大。
Lecanemab已经被视为β淀粉样蛋白的有效清除剂,11月30日披露的完整数据有助于证实这一点。来自一个由近700名患者组成的亚组的结果显示,在18个月的研究期间接受该药物治疗的患者,其β淀粉样蛋白的平均水平,低于决定其蛋白质是否“阳性”的阈值。
该研究的作者还写道,lecanemab治疗组在神经细胞降解和炎症的其他标志物上有更大的降低。
Aduhelm的案例中,FDA基于该药物清除大脑中β淀粉样蛋白斑块的能力,给予所谓的加速批准。FDA认为这种效果“可以合理地预测对患者的临床益处”。
03 0.5分的下降会有多大价值?
当卫材和渤健首次公布lecanemab的研究结果时,专家们对于这些结果是否代表了对阿尔茨海默病进展的有意义的影响感到不解。即使医生们看到完整的结果,这种争论还会继续。
临床医生使用CDR-SB来评估大脑和身体功能。在试验中,18个月后,接受lecanemab治疗的患者的CDR-SB评分比接受安慰剂治疗的患者平均下降了约0.5分。
对一些人来说,这是一个显著的获益,特别是考虑到该试验允许服用Aricept等其他阿尔茨海默病药物的患者参与。
“这是一个小的效应规模。但我想说的是,这比我们所看到的要多,而且是在我们全力以赴的基础上。”萨诺说。
“所以它是渐进式的,但很强大。”萨诺曾为卫材、渤健等阿尔茨海默症药物开发公司提供咨询,在审阅了试验结果后说,“我认为这是一件非常了不起的事情。”
但是,约翰霍普金斯医学院记忆和老年痴呆症治疗中心主任康斯坦丁·莱克索斯(Constantine Lyketsos)指出,阿尔茨海默病专家认为,一种药物需要提供至少1-2分的效果,才能被认为具有临床意义。
“我觉得这个领域是不言自明的。”莱克索斯此前也为卫材和其他制药公司提供咨询,同样审阅了lecanemab的数据。他说:“归根结底,我们在临床上是否存在最小的重要差异?答案是,我仍然不认为我们(用lecanemab)做到了这一点。”
在《新英格兰医学杂志》论文中,作者们提出一些谨慎的做法,他们写道:“需要进行更长时间的试验来确定lecanemab对早期阿尔茨海默病的有效性和安全性。”
04 Lecanemab治疗风险几何?
人们对lecanemab和其他类似淀粉样靶向药物的主要担忧,是一种被称为淀粉样相关成像异常(ARIA)的副作用。这是服用消除大脑中β淀粉样蛋白的药物的一个众所周知的后果,在其他阿尔茨海默病研究中也出现过。
在卫材的试验中,约22%接受lecanemab治疗的患者经历了与脑肿胀或出血相关的ARIA,而安慰剂组的这一比例不到10%。在大多数情况下,副作用是无症状的,而少数有症状的人通常会经历头痛、视力障碍和意识混乱。
接受lecanemab治疗的17%伴有出血的ARIA患者中,只有6人出现症状。
并且,6名服用lecanemab的患者在研究中出现死亡,而服用安慰剂的有7人死亡。美国健康新闻网站STAT和《科学》(Science)最近的报道称,lecanemab的三期试验中,有2例死亡病例被认为可能与该药物有关。二者都与脑出血有关,尽管还有其他因素,如使用血液稀释剂,也可能起了作用。
“脑溢血是不好的,”莱克索斯说,“当我们谈论FDA批准一种药物时,如果它可能会给成千上万的患者使用,那么出现这些出血的风险和人数规模就会变得非常大。”
来自西奈山医学院的萨诺同意,研究中报道的微出血是令人担忧的。尽管如此,她补充说,lecanemab的风险应该与其报告的益处进行权衡。
“那些能治疗很多严重疾病,同时不具有高风险的药物少之又少。认知方面的好处,是否重要到足以让你承担一些这样的风险?”萨诺说。
05 会像Aduhelm一样惨淡吗?
卫材已经根据早期的研究数据,向美国申请加速批准lecanemab。该公司预计,FDA将于2023年1月6日之前对其申请作出裁决。此外,根据新的后期试验结果,卫材计划在明年晚些时候申请lecanemab的完全批准。
华尔街的普遍预期是,lecanemab很有可能获得FDA批准。投资公司加拿大皇家银行资本市场(RBC Capital Markets)的分析师布赖恩·亚伯拉罕斯(Brian Abrahams),在11月中旬给客户的报告中称,批准的可能性为95%。RBC和雷蒙德·詹姆斯(Raymond James)的分析师团队估计,该药的年销售额峰值最终可能超过90亿美元。
2021年6月,当Aduhelm获得批准时,也曾有过类似的天价预测。但是,由于保险公司的抵制,以及医生对这种药物有效性的严重怀疑,导致该药在上市第一年的销量低迷。
如果lecanemab进入市场,卫材和渤健将有第二次机会来打造治疗阿尔兹海默病的“重磅炸弹”。
然而,这些公司可能会面临来自Aduhelm之后更困难的挑战。例如,联邦医疗保险(Medicare)在今年早些时候对于那些抗淀粉样蛋白的阿尔茨海默病药物实行限制性的覆盖政策,这也将影响lecanemab。分析师预计,卫材的积极后期结果将有助于扩大报销范围,但这需要更多的时间。
参考资料:
1.What to make of Eisai and Biogen’s latest Alzheimer’s drug data;BioPharma Dive