$君实生物-U(SH688180)$ $九安医疗(SZ002432)$ $雅本化学(SZ300261)$
德国实验室对于德国市场抗原检测试剂盒的评测结果(截至20220131),都是干货,链接都给你们,大家自己理解。
1、老规矩先上图:
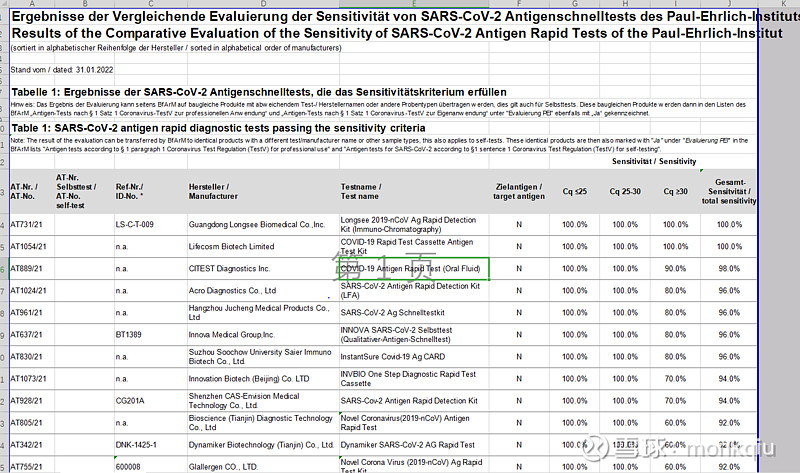
2、为什么找这个数据:
今天上午刚写了个帖子网页链接,做了个小目标研究研究一些感兴趣的内容。于是晚上带着辩证的思维,听了某专家对抗原检测的点评,说实在话,这专家不像老油条,问啥说啥,政治敏感性太差,但是她说的内容除了某些未经证实的内容,基本是符合逻辑的。
我完整的听了一遍,其中提到一点,“对抗原检测试剂盒的效果,建议参考德国PEI实验室的测试结果”,说的比较模糊,我一开始听成BEI 、BEV,但总算是找到了。
德国实验室检测了所有的抗原测试盒并把结果都公示出来了,不管股民怎么看,人家事情做的敞亮,这算不算新冠检测产品质量排行手册?
3、废话不多说,干货:
PEI实验室关于新冠试剂盒官网网页:网页链接
PEI实验室所有检测结果EXCEL下载链接,记得下载后看看中国哪些厂家的质量比较好。
网页链接
很奇怪,我没看到九安医疗的产品,当然之前我主要研究国产特效药,没太注意这一块,大家自己理解了。
另外,关于这个实验室的定位,人家基本就是官方合作实验室了,请参考人家官网说明:
The Federal Institute for Drugs and Medical Devices (Bundesinstitut für Arzneimittel und Medizinprodukte, BfArM) and the Paul-Ehrlich-Institut are the authorities that provide information on SARS-CoV-2 test systems. The information materials complement each other. The legal framework for this, among other things, is the Coronavirus Test Regulation (Coronavirus-Testverordnung, TestV).
全部讨论
具体到九安,大家可以先思考一下:
1. 九安的产品是不是最好的?
2.这个市场是不是充分竞争的红海?
3.目前的竞争格局下,九安的收入和增长预期能否保持?
4.它的估值是否合理?
个人点评一下,这个专家缺心眼,别人问啥就回答啥,没考虑到合规问题。 适合做内部研究,不适合当发言人,都不知道哪些该说,哪些不该说
提这些问题,主要是在雅本 评论价格太贵时,好多人拿九安医疗来做比较,于是我留了个心眼,听了听专家,随便搜索了一下,。
也请$雅本化学(SZ300261)$ $九安医疗(SZ002432)$ 的兄弟独立思考一下
继续回答某人强调的美国EUA唯一性的问题,临时的哦。
如果你看过信达创新药出海被否时FDA的点评,你会理解如果有有力的证据能够证明新的药物比现有的标准疗法好,它会毫不犹豫的推动新的药物,这是政治正确。
如果专家对试剂盒有效性的点评足够客观的话,对比100分和65分,你们觉得FDA会怎么做?
PEI实验结果 也没什么花头,百家之上的中国IVD公司都做了 花钱走流程寄样品就行了 那又如何?唯独美国只此一家。Bfarm权威还是US FDA权威 可以找你的欧美专家朋友了解一下
厂家太多,我只整理了一下准确率>90%的十来家企业,找出了对应的中国厂家名字,只有一家是加拿大企业,中国制造牛AC。另测试的厂家一共有200家。(这个准确率到底啥意思我也不太确认,不够专业,但是的确是优中选优)
至少,这个表格可以看出,抗原检测试剂盒应该是一个充分竞争的市场,对不对?
至于专家嘴中提到的有效率只有60-70%,人家都做到高中大学,某些人还在小学生水平不思进取之类的评价,到底有没有依据,这就没法置评了。
随便搜索了一下这个实验室,辉瑞的疫苗要进欧洲都得这个实验室监管批准呢,你们怎么能贬低它的地位?给你们链接
网页链接
BioNTech和辉瑞宣布获得德国权威Paul-Ehrlich-Institut的监管批准,开始进行COVID-19候选疫苗的首次临床试验
2020年04月23日 阅读量:285 新闻来源:中国化工网 okmart.com | 投稿
第一项与COVID-19相关的临床试验在德国启动
初始剂量递增阶段,目标剂量范围为1µg至100µg
来自BioNTech的GMP认证的欧洲mRNA生产设施的临床供应
四名候选疫苗进入临床研究
柏林,德国和纽约,2020年4月22日(全球新闻)-BioNTech SE(纳斯达克股票代码:BNTX,“ BioNTech”或“公司”)和辉瑞公司(纽约证券交易所:PFE)今天宣布,德国监管机构主管机构Paul-Ehrlich-Institut已批准BioNTech的BNT162疫苗计划预防COVID-19感染的1/2期临床试验。BioNTech和辉瑞公司正在共同开发BNT162。该试验是首次在德国开始的COVID-19候选疫苗的临床试验,并且是全球开发计划的一部分中国化工网okmart.com。辉瑞和BioNTech还将在获得监管机构批准后在美国进行BNT162的试验,预计不久后将进行试验。
这四种疫苗是BioNTech针对COVID-19的项目“ Lightspeed”的首批候选疫苗,每种疫苗分别代表不同的mRNA格式和靶抗原。四种候选疫苗中的两种包括核苷修饰的mRNA(modRNA),一种包括含有尿苷的mRNA(uRNA),第四种候选疫苗利用自扩增mRNA(saRNA)。每种mRNA形式均与脂质纳米颗粒(LNP)制剂结合。两个候选疫苗中包含较大的刺突序列,而另外两个候选物中则包含来自刺突蛋白的较小的优化受体结合结构域(RBD)。基于RBD的候选物包含那部分尖峰,被认为对于引发可以使病毒灭活的抗体最重要。
德国这个测评机构,就和做钻石证书一样 寄样板 花钱就行
