2022年2月28日,FDA正式批准传奇生物/强生的BCMA CAR-T疗法Carvykti上市,用于治疗复发性/难治性多发性骨髓瘤,商品名为Carvykti。成为中国首个进入美国的细胞治疗产品。
多发性骨髓瘤(MM):第二大血液恶性肿瘤,之前的治疗药物主要是蛋白酶抑制剂(PI),免疫调节剂(iMiDs)和单抗(mAb)
竞品:BMS/蓝鸟生物合作开发而Abecma【2021年获批,首款治疗(MM)的CAR-T疗法】
价格比较:Carvykti的定价为46.5万美金,Abecma为41.95万美金
临床数据比较:
有效性:
cilta-cel治疗末线ORR/(s)CR达98%/83%
Abecma治疗末线ORR/(s)CR72%/39%
中位(数)无进展生存期mPFS超过2年,高于同类疗法平均8-12个月;
安全性:
cilta-cel在3级以上细胞因子风暴/神经毒性发生率5%/10%,对比Abecma(ide-cel)9%/4%;即耐受性较好,3/4级CRS和神经毒性的发生率较低。
商业合作:
首付款:3.5亿美元预付款
权益比例:中国权益两家按70:30分成,海外权益按50:50分成
市场空间:MM单病种主流药物规模在欧美等主要国家合计超过120亿美元,未来三年将保持5-8%的增长。作为此前这一市场唯一的CAR-T药物Abecma2021年营收1.64亿美元。
市场竞争格局:
2021是CAR-T元年,除了FDA和NMPA各有两款CAR-T新产品获批上市。在cilta-cel获批前,FDA已有五款CAR-T疗法获批上市,均用于治疗血液瘤。分别是:
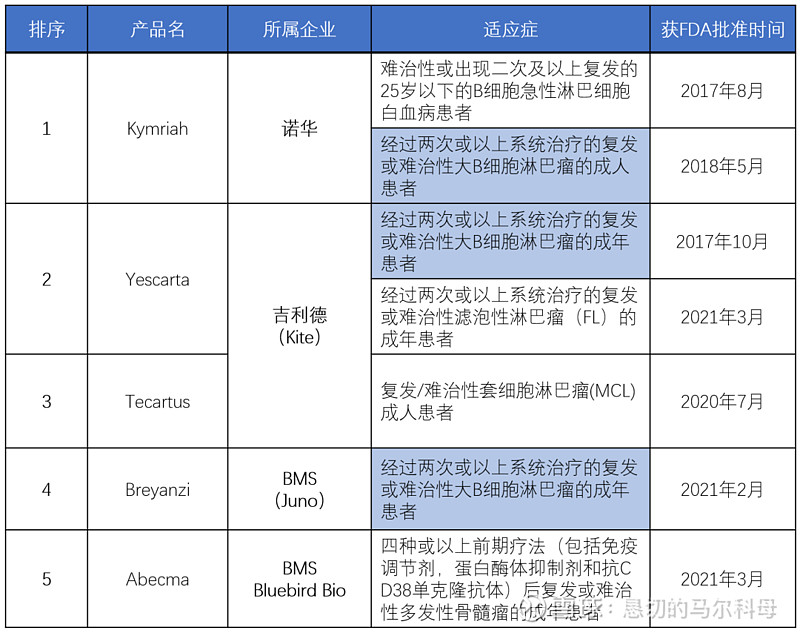
FDA目前获批的5款CAR-T产品
中国也已有两款CAR-T产品获批上市,用于治疗淋巴瘤:
2021年6月,复星凯特阿基仑赛注射液(引进Yescarta技术,商品名:奕凯达)。
2021年9月,药明巨诺瑞基奥仑赛注射液(商品名:倍诺达)。
在全球已获批的CAR-T疗法里,除了百时美施贵宝/蓝鸟生物Abecma(ide-cel)和传奇生物/杨森制药cilta-cel是靶向BCMA,其余四款都是靶向CD19。
截至2020年6月,全球已有超600项CAR-T临床试验进行中,中国以超过357项位居全球首位,而其中靶向CD19近50%,同质化程度已超越了PD-(L)1。
创新药出海的先驱,其探索都值得尊敬,不必以成败论英雄。#传奇生物# #金斯瑞生物科技# #复星医药@雪球创作者中心 @今日话题