12月1日,药物临床试验登记与信息公示平台官网显示,信达生物的GLP-1R/GCGR激动剂玛仕度肽(IBI362)启动III期临床试验。
点击下载:信达生物玛仕度肽高剂量9mg治疗肥胖临床II期48周研究数据更新
该研究是一项随机、双盲、安慰剂对照临床试验,拟纳入450例体重指数(BMI)≥30kg/m2的肥胖受试者,旨在评估玛仕度肽(3、6、9mg,每周1次)对比安慰剂的减重疗效和安全性。研究的主要终点为第60周受试者体重较基线的百分比变化以及体重下降≥5%的受试者比例。
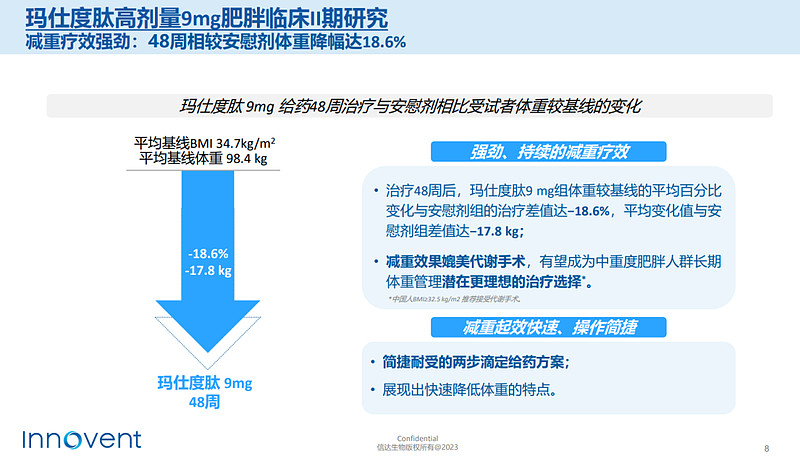
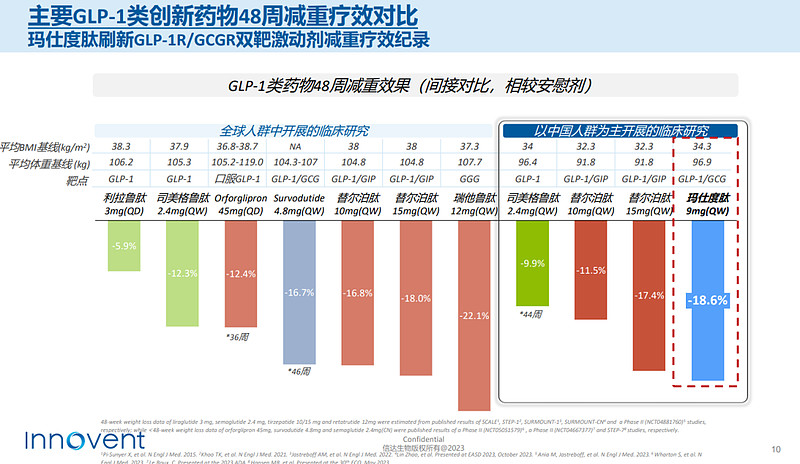
今年10月,信达生物公布了9mg玛仕度肽治疗肥胖的48周II期研究数据。结果显示,9mg玛仕度肽组相较安慰剂组体重降幅达18.6%,高于24周的数据(-15.4%);体重下降超过15%或20%的受试者占比为51.2%和34.9%,相较于24周(31.7%和21.7%)显著增加。
点击下载:玛仕度肽-ibi362-高剂量-9mg减重ii期临床研究48周数据更新_20231030_挂网版
(来源:信达生物官网)
治疗24周后,玛仕度肽降低肝脏脂肪含量达73.3%,显著改善了一系列代谢指标(TG、TC、LDL-C、sUA),且该临床获益在48周继续维持。
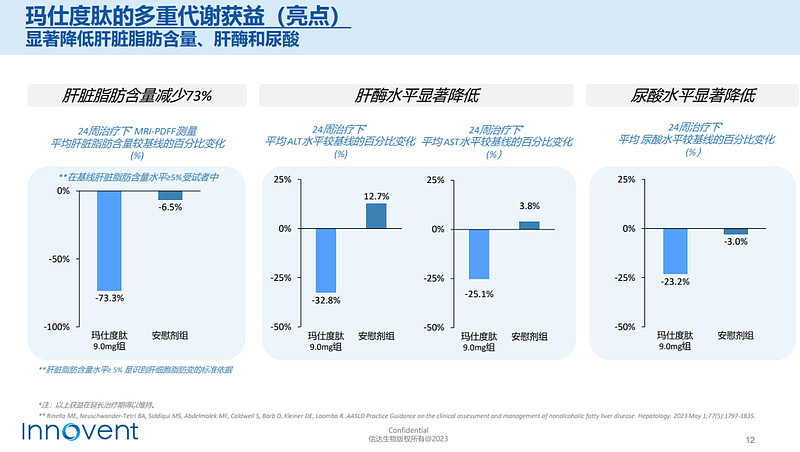
(来源:信达生物官网)
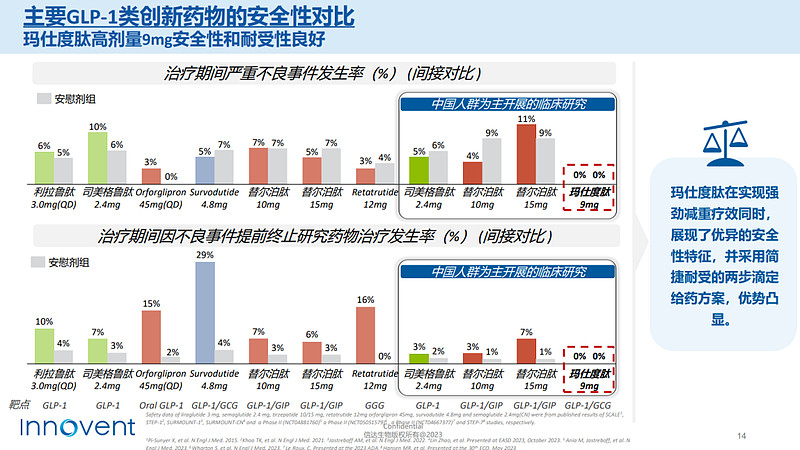
安全性方面,胃肠道不良反应(恶心、呕吐和腹泻)是最常发生的不良事件,绝大多数为轻度或中度。无受试者因不良事件提前终止研究药物治疗,未发生严重不良事件,未见心血管风险增加的安全性信号。
(来源:信达生物官网)
信达生物预计在今年年底至2024年年初递交玛仕度肽用于减肥的上市申请,并计划于2024年递交玛仕度肽用于治疗2型糖尿病的上市申请。