2023年5月12日,礼新医药宣布与阿斯利康就靶向GPRC5D抗体偶联药物LM-305的全球开发和商业化权益达成独家许可协议。该项目为潜在同类首创新型ADC分子,目前处于临床前阶段。本次交易总价值为6亿美元,礼新医药可获得5500万美元首付款和近期里程碑付款、另加高达5.45亿美元的开发和商业化里程碑付款,以及基于全球净销售额的梯度销售分成。
这也是礼新医药在一年内完成的第二笔创新药海外license out交易。随着LM-305的授权交易完成,礼新医药在成立后仅3年半的时间内,连续两款产品授权给大型跨国药企,成为业内非常少见的所有出海产品均与跨国制药巨头进行合作的中国生物科技公司之一。
礼新医药曾在去年5月与美国Turning Point公司就CLDN 18.2 ADC药物LM-302达成总价值11亿美元的license out交易,拉开了中国CLDN 18.2相关新药资产出海的大幕。值得一提的是,在与礼新完成交易仅一个月后,Turning Point即被BMS收购,LM-302也因此被BMS以代号BMS-986476纳入管线。此次梅开二度,与全球MNC巨头达成潜在first in class(FIC)新药的海外授权交易,也让礼新医药再次成为业界关注的焦点。
中国创新药项目“出海”自2007年有记录以来,至今已发生百余起,尤其近两年更加频繁。礼新医药的独特之处在于它既能够从零开始研发创新药,也能够连续而高效地完成自研产品的对外授权,成为了为数不多的能持续受到跨国制药巨头青睐的中国Biotech。通过对外授权合作,礼新医药不仅获得了可观的现金收入来支持自身发展,同时也借助行业巨头的认可证明了自身的产品研发实力以及国际商务拓展能力。
既在自主研发方面拥有一技之长,又能连续赢得国际大药企的青睐,礼新医药是如何做到的?
授权合作:审时度势,敏捷出击
从与Turning Point和阿斯利康公司的合作来看,善于审时度势并积极寻求合作是礼新医药公司运营策略中的核心要素,也体现了它作为一家Biotech公司的敏捷决策和高效执行。
以去年对外合作的LM-302项目为例,CLDN 18.2靶向治疗在国内早已是白热化竞争的拥挤赛道,有近30款单抗、ADC、细胞疗法药物相继蜂拥进入临床,也让中国成为全球CLDN 18.2资产的富集地。尽管先行者安斯泰来Zolbetuximab的III期成功降低了CLDN 18.2的成药风险,但是如何在国内高度内卷的竞争态势中脱颖而出却是各家企业必须要面临的挑战。
礼新医药去年5月与Turning Point达成的许可协议,成功奏响了国产CLDN 18.2 ADC出海的序章。需要特别指出的是,礼新医药对于交易时机的把握非常精准:既选取了CLDN 18.2靶点的开发前景进一步得到确证的时机,也抓住了DS-8201横空出世,ADC热潮下全球药企对于这一风口资产渴求的机遇。作为一家当时成立仅两年多的Biotech,能够在资本寒冬的行业大环境下实现总价11亿美元的大型项目授权合作,充分体现了公司在自研+对外合作既定战略下的高效执行力。
这笔交易的价值在BMS收购Turning Point之后又得到进一步提升。LM-302虽然不是全球首个进入临床的CLDN 18.2 ADC,但是凭借快人一步的交易合作第一个进入了制药巨头管线,很大程度上提高了产品后期开发成功的概率和触及全球患者的可能性,并为公司提供了未来商业化上的潜在不菲收入。值得一提的是,在LM-302出海之后,科伦博泰SKB315、石药集团SYSA1081以及康诺亚CMG901等CLDN 18.2 ADC随之陆续出海,并且交易价格也水涨船高,这其中LM-302投石问路的推动效应不容忽视。借此交易,礼新医药跻身于国产ADC出海的先行者行列,持续拉升了海外企业对于中国ADC药物的关注,也推动了国产ADC的出海热潮。从去年5月至今,已有24款国产ADC成功实现海外授权。
国产ADC项目许可情况(单位:亿美元)
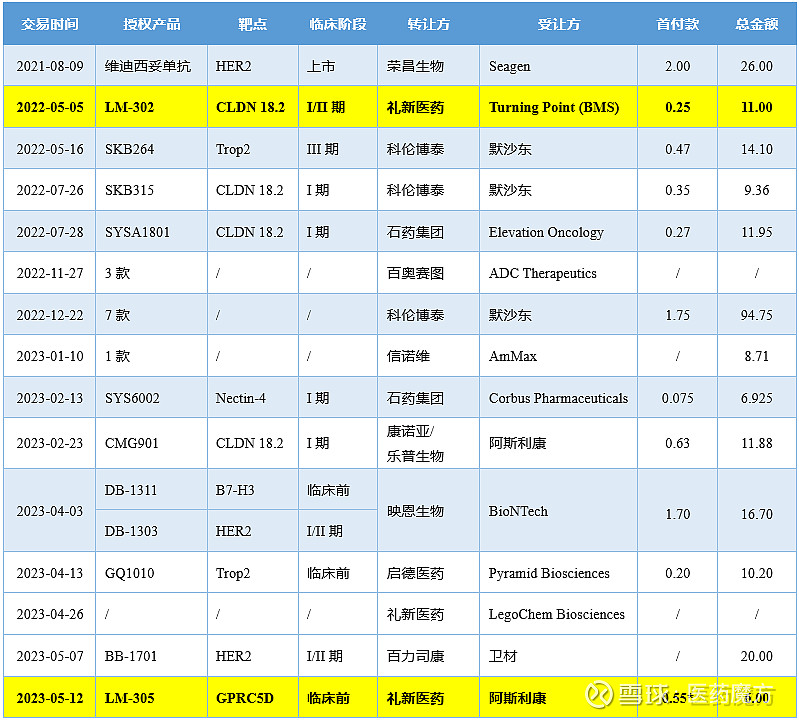
*首付款及近期里程碑付款
来源:医药魔方Nextpharma数据库
时隔一年,礼新医药再传捷报,第二次实现自研ADC产品的海外授权,再次获得了国际大药企的认可。此次的交易跟之前LM-302授权相比,又具备更多独特的亮点。
如果说LM-302项目体现了礼新医药稳扎稳打,针对热门靶点开发潜在“同类最优”差异化产品的实力,那这次的主角LM-305作为目前全球唯一一款针对多发性骨髓瘤(multiple myeloma, MM)的靶向GPRC5D ADC药物, 则是进一步证实了礼新医药发掘临床价值的独到思路,以及敢于挑战“同类首创”产品的过人实力。
从适应症以及靶点来看,由于多发性骨髓瘤具有容易耐药复发的特性,导致大量复发/难治多发性骨髓瘤(R/R MM)患者亟需新的有效治疗手段。GPRC5D(G protein-coupled receptor class C group 5 member D)是近年涌现的为数不多的多发性骨髓瘤免疫治疗靶点,其表达跟另一成熟靶点BCMA相互独立,因此GPRC5D靶向治疗有望解决R/R MM领域的未满足临床需求。目前其它同靶点药物多为CAR-T疗法或双抗,其中以强生公司的双抗Talquetamab以及原启生物的OriCAR-017为代表,两款产品的亮眼临床研究数据均证明了GPRC5D这个靶点的巨大潜力。
根据开发进度推断,礼新医药在成立之初就布局了这个靶点,足以证明其眼光独到。从产品来看,LM-305作为同靶点唯一一款在中美两地获批临床的ADC,在临床前研究中已经展现出了优秀的抗癌药效。综合ADC药物在疗效、安全性、可及性等方面的差异点,LM-305极具潜力成为填补市场空白并为患者带来更大临床收益的优秀产品。最后,从交易双方来看,此次引进LM-305的阿斯利康公司在肿瘤领域非常活跃,无论是跟ADC相关的靶点布局、技术储备、还是临床开发经验方面,阿斯利康都处于全球领先的地位。LM-305能够赢得阿斯利康的青睐,充分说明礼新医药的研发及BD实力已经处于国际水准。
此外,礼新医药在早期产品的研发合作方面也喜报频传。根据公司官网披露的信息,礼新医药于2023年4月与韩国LegoChem Biosciences(以下简称LCB)达成一项研究合作,双方将使用礼新医药基于独家抗体发现平台研发的抗体资产以及LCB的ADC技术平台,共同开发一种有潜力成为“同类首创”的ADC药物。LCB是全球ADC领域的知名企业,其技术平台已经获得包括武田(Takeda)、安进(Amgen)在内的多个跨国药企的广泛认可。与LCB达成该合作,是对礼新医药的早期研发实力的又一肯定。
除了海外授权以外,礼新医药也积极寻求与国内药企的合作。为探索LM-302的联合应用策略,礼新医药已与君实生物和康方生物相继达成临床研究合作,正在开展LM-302联用特瑞普利单抗治疗实体瘤的I/II期临床试验,未来将开展LM-302联用AK112(依沃西单抗)的实体瘤临床研究。
研发实力:专注FIC和BIC,全自研差异化管线布局
高额跨境交易的连续达成,不仅需要公司拥有专业化的商务拓展团队,更加关键的是每个产品本身的质地足够出色。从靶点选取、分子筛选、开发速度、技术创新、到完备的数据分析与呈现,礼新医药独特的管线产品不仅是其赢取外界认可及授权合作机会的关键要素,更是公司研发实力、创新能力和市场竞争力的体现。能够接连收获海外MNC公司的“橄榄枝”,证明了其不容小觑的研发实力,借此机会,我们对礼新医药的研发体系进行了梳理分析。
自创立之初,礼新医药的目标就确立为开发“全球首创”和“同类最优”分子,解决重大未满足临床需求,由“礼敬生命,致力创新”这一使命提炼而成的公司名称亦体现了这一初衷。
为了实现这一目标,礼新医药建立了3个赋能新药开发的技术平台:基于GPCR以及多次跨膜蛋白研究的抗体发现平台、特色连接子+有效载荷的ADC技术平台以及免疫桥接多特异性抗体平台。三个平台互为支撑,根据临床需求,针对肿瘤微环境内的不同靶点,选择最合适的药物形式进行开发,这正是礼新医药的核心竞争力所在。基于这套研发引擎,礼新医药成立虽仅3年有余(2019年9月成立),但已将两款候选产品推进至II期临床阶段,两款产品推进至I期临床阶段,同时还拥有超过10款临床前在研产品,其研发效率着实可圈可点。
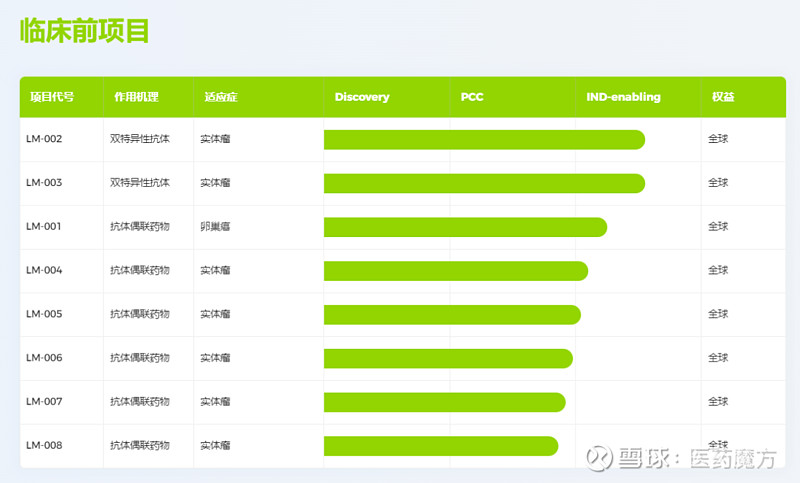
礼新医药管线(来源:礼新医药官网)
从礼新医药的管线可以看出来,其研发宗旨为全自研差异化创新,在保持跟进创新药热门领域的基础上,专攻能做出差异化优势的ADC、单抗和双抗药物。
除本次授权给阿斯利康的LM-305项目以外,礼新医药目前还拥有3款差异化的临床阶段产品,其中两款为具备best in class(BIC)潜质的分子,包括:
1)靶向Claudin 18.2的ADC LM-302,其开发进度处于全球CLDN 18.2药物第一梯队。根据公司官网介绍,LM-302针对CLDN 18.2靶点对抗体部分进行了优化,使得该产品能同时靶向CLDN 18.2高表达与低表达患者,从而扩大了适应症患者人群。此外,LM-302还通过增强内吞活性提高了其肿瘤杀伤疗效。目前,LM-302正在开展3项I/II期临床试验,其中两项将于2024年上半年完成,进度领先于多个同类靶点产品。
2)靶向CCR8的单克隆抗体LM-108。该产品是首个国产CCR8单抗,可以通过靶向清除肿瘤环境Treg,克服其他抗体(如CTLA4)的有限剂量窗口问题,从而解决PD-1耐药或者不应答肿瘤患者的未满足临床需求。该产品潜在的适应症谱相当广泛,涵盖多种实体瘤,有望成为未来又一重磅药物。
3)LM-101是一款处于I期临床阶段的靶向SIRPα(信号调节蛋白α)的单克隆抗体,可以通过阻断肿瘤细胞表面的CD47-SIRPα免疫检查点信号通路,从而激活免疫系统达到抗肿瘤效果。目前该赛道同类药物以靶向CD47的抗体和融合蛋白为主,LM-101项目独辟蹊径,通过靶向SIRPα来避免CD47靶向药物相关的血液毒性,再次体现了礼新医药针对热门靶点的差异化开发思路。适应症方面,该产品可针对多种实体瘤以及血液瘤,此外近期已经有公司(如第一三共)开始探索SIRPα靶向与ADC的联用,考虑到礼新医药丰富的ADC产品,其管线未来空间充满想象。
此外,礼新医药官网显示,多个具有BIC和FIC潜力的临床前ADC和双抗产品已进入pre-IND阶段和PCC阶段,这些产品的治疗潜力同样值得期待。
总结
一年内对外授权两款产品,累计交易金额达到17亿美金,同时实现与两大全球制药巨头携手合作。礼新医药作为一家专注研发的创新药企,探索出了一条适合自身的可持续发展道路:以坚持创新和差异化布局为立足之道,通过持续输出产品磨练“内功”,最后积极寻求合作从而反哺研发,形成良性循环。或许,这也可以称之为“礼新模式”。如此这般,礼新医药做到了创新与发展皆得:既凭借自身研发实力在ADC这样的创新药热门领域站稳脚跟,又通过差异化开发FIC分子避免内卷,同时还通过对外授权合作持续得到MNC的认可。战略得当,决策迅速,礼新医药在走向全球的过程中,正成长为ADC和肿瘤免疫领域的Biotech新星。
放眼全球,类似的发展路径已经被多次证实,诸如Seagen、Genmab等先行者已经崛起为市值数百亿美金的行业中坚。如今在全球医药行业玩家纷纷把眼光转向中国,开始竞相追逐本土企业所开发的创新产品的大趋势下,相信礼新医药扎实的内功和独特的管线会给中国生物制药领域带来更多惊喜。