6月27日,吉利德(Gilead)宣布,已向FDA重新提交lenacapavir的上市申请,用于治疗既往接受过多次治疗、多重耐药的HIV-1感染者。
Lenacapavir是一款first-in-class长效HIV衣壳抑制剂,可通过干扰病毒生命周期的多个重要步骤抑制HIV-1的复制,包括抑制由病毒衣壳介导的HIV-1前病毒DNA的摄取、组装和释放,以及病毒衣壳核心的形成,而且对其他现有药物类型没有已知的交叉耐药性。该产品曾获FDA突破性疗法认定。如果获得批准,它将成为唯一一款每年给药2次的HIV治疗药物。

2021年12月,FDA对硼硅酸盐小瓶装注射用lenacapavir进行的所有临床研究进行了暂停。原因是FDA担忧硼硅酸盐玻璃小瓶与lenacapavir溶液的相容性,而这可能会导致lenacapavir溶液中形成亚可见玻璃微粒。
2022年5月,在审查吉利德全面的计划和lenacapavir溶液与铝硅酸盐玻璃替代小瓶的储存和相容性数据后,FDA决定取消其临床暂停。
今年5月12日,一项关于lenacapavir的多中心III期临床(CAPELLA)试验数据发表在《新英格兰医学杂志》(NEJM)上,旨在评估lenacapavir在既往接受过多次治疗、多重耐药的HIV-1感染者中的疗效。该试验共入组72名受试者,随机分为两个队列,给药方案如下:
队列1:24人口服lenacapavir+入组前抗病毒方案治疗,第15天开始每6个月皮下注射一次lenacapavir,并接受优化背景方案治疗(OBT);12人接受安慰剂+抗病毒治疗,第15、16、22天口服lenacapavir+OBT,第29天开始每6个月皮下注射一次lenacapavir+OBT。
队列2:36人口服lenacapavir(第15、16天600mg,第22天300mg)+OBT,随后每6个月皮下注射一次lenacapavir+OBT。

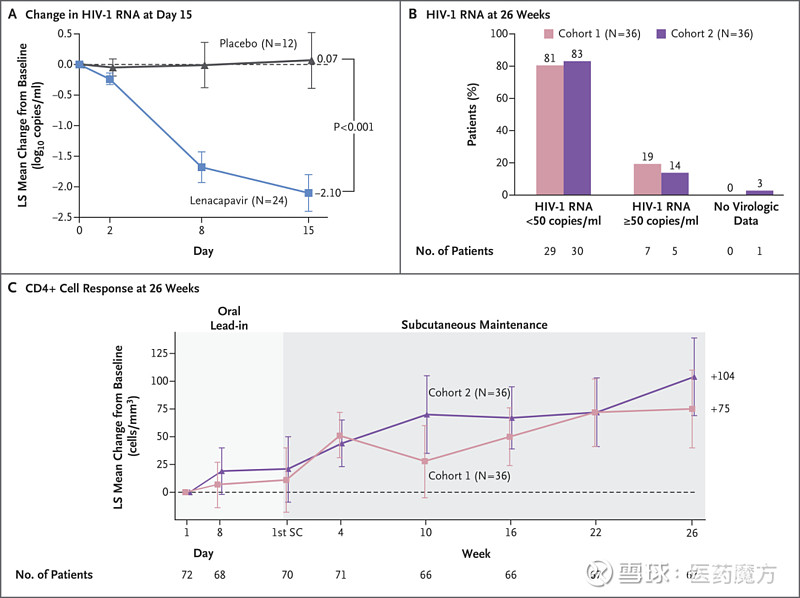
结果表明,队列1的24名患者中,88%的HIV-1 RNA减少0.5 log10拷贝/ml,安慰剂组为17%。第26周时,队列1中81%患者(29/36)的病毒载量低于50拷贝/ml,89%(32/36)的病毒载量低于200拷贝/ml。队列2中,83%(30/36)的病毒载量<50拷贝/ml,86%(31/36)的病毒载量<200拷贝/ml。CD4+计数低于50个/μl的患者比例从24%(17/72)降至0%(0/67)。
病毒学失败和耐药性方面,8名患者(队列1、2各4名)出现与lenacapavir相关突变,其中4名患者在lenacapavir治疗过程再次恢复病毒学抑制(<50拷贝/ml)。
安全性方面,大多数不良事件是轻度或中度的,包括注射部位反应。