今日,医药魔方PharmaGo数据库显示罗氏在中国提交的艾美赛珠单抗注射液新适应症上市申请(受理号:JXSS2000012/13/14/15)已处于“在审批”阶段,有望于近期获得NMPA批准。适用于不存在凝血因子VIII抑制物的A型血友病患者(先天性凝血因子VIII缺乏)成人和儿童患者的常规预防性治疗以防止出血或降低出血发生的频率。
Hemlibra(艾美赛珠单抗)是罗氏/Chugai联合开发的一款重组人源化的IgG4双特异性抗体,其通过桥接凝血因子IXa和凝血因子X,在体内模拟凝血因子VIIIa以恢复A型血友病患者的凝血功能。
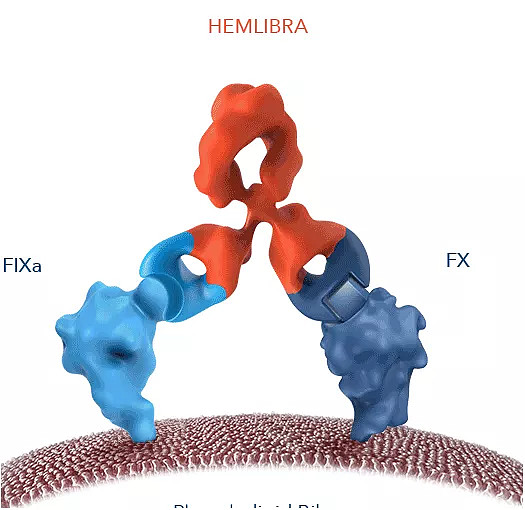
艾美赛珠单抗作用机制
艾美赛珠单抗于2017年11月获得FDA批准上市。在我国,该药物于2018年12月被NMPA以临床急需用药通道加速批准上市用于含凝血因子VIII抑制物的A型血友病的出血预防治疗,中文商品名为舒友乐立,是我国批准上市的首个双特异性抗体药物,也是近20年来首个用于A型血友病的新药。艾美赛珠单抗目前尚未进入我国医保目录。
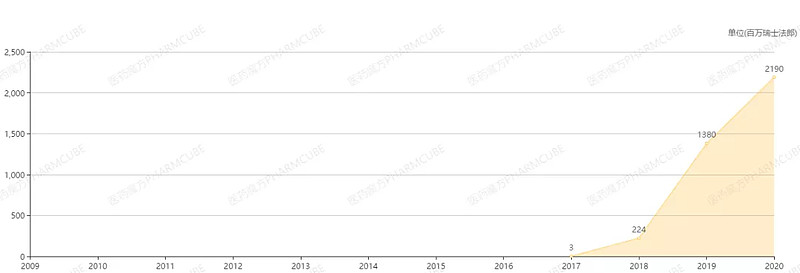
艾美赛珠单抗历年全球销售额
艾美赛珠单抗2020年全球销售额为21.9亿瑞士法郎,是首个销售额进入全球TOP100的双特异性抗体药物。