昨天一篇网文引爆医药圈,$君实生物(01877)$ 今日盘中最大跌幅-5%,盘中已经翻红。$君实生物-U(SH688180)$ 今日盘中最大跌幅-10%。
上交所的问询函昨晚已经发出,君实生物面临飞来大锅,扣在PD-1医保谈判前夕,不知江湖里怎样看待这样的巧合 ? 但是深究下来最后倒霉的可能是 @兽爷 。
(1)君实生物的PD-1定价全球最低。只有海外同类产品的1/6。
时间拉回到2年前,君实生物PD-1(特瑞普利单抗)获批上市的那一刻,在外资PD-1天价背景下,后续排队的国内PD-1企业都在翘首等待君实的官宣售价。
那一刻无数人紧张期盼,有医生,有病人,有ZF,更有同行,也许还有 @兽爷 。
在此之前,2019年很多机构预测中国的PD1市场规模约为1000亿元规模,但君实的惠民定价使得这个市场直接缩水到300亿元,估计那一刻不少人咬牙切齿:君实生物董事长是不是疯了?难道不赚钱了吗?
难道君实生物老板赔钱做研发,带给老百姓便宜好用的抗肿瘤药也需要走后门 ?
马上就进入医保谈判的关键时刻了,如果君实PD-1降价进入医保,按照既往成功进入医保药品至少降价幅度>50%的规律,那中国人真有可能在2021年1月1日使用到年治疗费用4万的PD-1,医保报销后只需自费负担<2万元,这才是能让老百姓切切实实支付得起的价格。
(2)君实生物特瑞普利单抗(PD-1)对比信达生物的信迪利单抗(PD-1)及恒瑞医药的卡瑞利珠单抗(PD-1,上述两款单抗药物均为有条件批准上市情况)的数据显示,
信迪利单抗受试者数量为96人,所有级别的不良反应发生率99%,三级及以上不良反应发生率33.3%;
卡瑞利珠单抗受试者数量为75,,所有级别的不良反应发生率100%,三级及以上不良反应发生率26.7%。
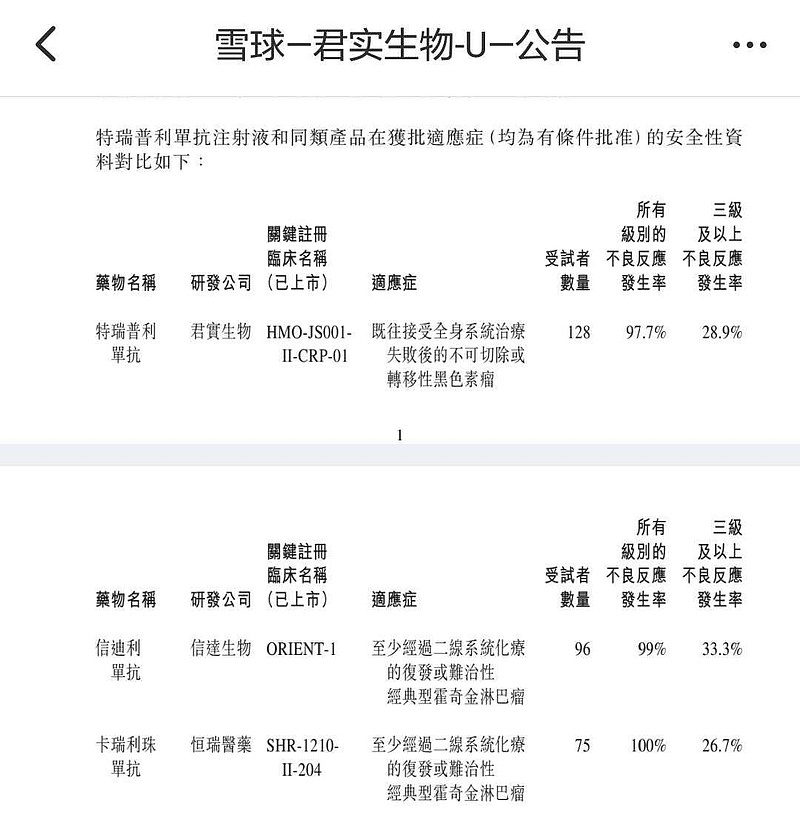
君实生物PD-1安全性不差于其他任何药企。
(3)君实生物特瑞普利单抗注射液和同类产品在相同获批适应症——黑色素瘤,有效性资料对比中显示:
特瑞普利单抗的客观响应率(ORR)为17.3%,疾病控制率(DCR)为57.5%,中位数总生存期(mOS)为22.2月,12个月总生存率为67.3%。
海外进口的默沙东PD-1(K药)的客观响应率(ORR)为16.7%,疾病控制率(DCR)为38.2%,中位数总生存期(mOS)为12.1月,12个月总生存率为50.6%。
君实生物PD-1疗效更优。
再举例,关于肺癌适应症。
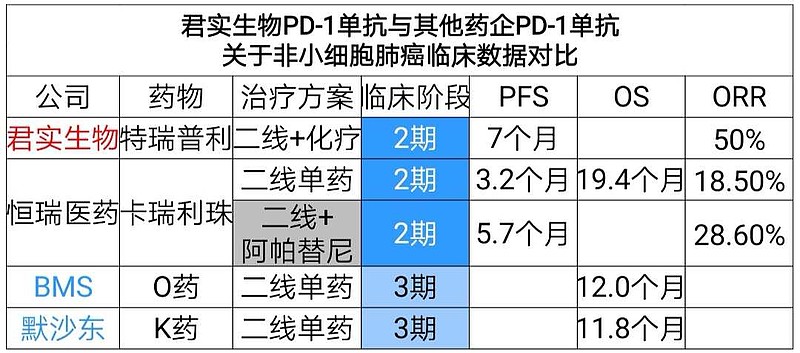
君实生物PD-1在非小细胞肺癌适应症的临床试验疗效数据也是最优。
君实生物PD-1单抗联合化疗,二线治疗#EGFR阳性非小细胞肺癌# ,PFS高达7个月,ORR高达50%。
恒瑞医药、百时美施贵宝、默沙东的PD-1单药,二线治疗#EGFR阴性非小细胞肺癌# ,并不比君实生物更优。
由于君实生物PD-1关于非小细胞肺癌(EGFR阴性)3期临床已经入组完成,正在随访。所以,暂时未列出一线治疗数据。
(4)君实生物的特瑞普利单抗也是中国第一个,获得美国FDA🇺🇸突破性疗法认定的自主研发抗PD-1单抗。
今年,特瑞普利单抗在黏膜黑色素瘤、鼻咽癌、软组织肉瘤治疗领域获得美国FDA授予的3项孤儿药认定。特瑞普利单抗治疗鼻咽癌获得了美国FDA授予的突破性疗法认定(该项认定的定义是:初步临床证据表明,该药物在临床重要终点上可能比现有疗法有实质性改善)。
君实生物开启了PD-1海外上市的先河。
(5)药审中心(CDC)没有江湖。
君实生物的PD-1上市前,国内患者只有默沙东和百时美施贵宝两款进口品种可供选择,年费用100万元高高在上。
中国🇨🇳药监局才给君实开个绿色通道。这难道也需要走后门?我列举一下国内PD1的申请时间和获批发证时间,验证一下是否真的有后门。
君实生物——特瑞普利单抗(受理号:CXSS1800006)CDE承办时间(2018年3月20日),NMPA发证时间(2018年12月21日),历时约9个月。
信达生物——信迪利单抗(受理号:CXSS1800008)CDE承办时间(2018年4月19日),NMPA发证时间(2019年1月3日),历时约8.5个月。
恒瑞医药——卡瑞利珠单抗(受理号:CXSS1800009)CDE承办时间(2018年4月23日),NMPA发证时间(2019年6月3日),历时约13.5个月,因其毛细血管瘤(反应性毛细血管增生症RCCEP)不良反应被专家多次讨论后才最终获批。
百济神州——替雷利珠单抗(受理号:CXSS1800019)CDE承办时间(2018年9月6日),NMPA发证时间(2020年1月6日),历时16个月。
一般来说,君实PD1作为国产首个获批的PD1药物,应该所花时间是最短的,因为市面上已经有了一款药物能够满足老百姓迫切的需求了,同类产品的审批就会适当放慢,但没想到还有一家信达生物历时更短,不知道 @兽爷 有什么见解?
笔者在这呼吁大家不信谣不传谣,不要被某些别有用心之人带了节奏,原因无他,支持尚存于襁褓中的民族企业,让公道长存!