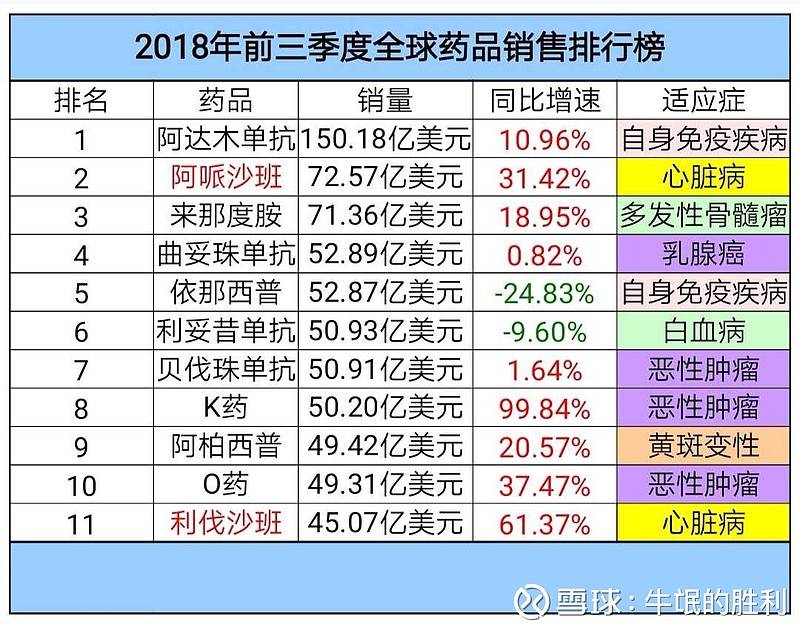
2018年全球销量排名TOP2阿哌沙班,排名仅次于阿达木单抗。
阿哌沙班美国市场属于辉瑞,到2023年化合物专利(02821537.0)到期(保护期延长)。美国以外市场属于BMS,包括中国内地市场专利于2022年9月到期。

需要注意,欧美日海外已经批准了阿哌沙班制剂专利:201180011229.X。而我国却处于实审中,理论上来说应该与海外同步。

豪森药业虽然由NMPA已经批准首仿,只是豪森药业BE进度稍快,并没有涉及挑战原研专利,也没有‘’永久首仿权‘’(被原研专利阻挡)。$东阳光药(01558)$($东阳光科(SH600673)$)和华海药业已经在美国挑战原研专利,与辉瑞对簿公堂。如果成功挑战专利(或者获得ANDA简略批准),将按照国内相关规定,广东东阳光药阿哌沙班已经在欧美上市并且申请国内首仿,可以优先审评,并获得1.5年数据保护期。
反过来,如果豪森药业如果等待到专利到期上市,并没有1.5年数据保护期。

齐鲁制药在国内开展5mg规格BE(适应症是AF,国内未批准该适应症),却试图申请2.5mg规格VTE适应症,理论上会反复发补或者否决。
华海药业并没有申请国内上市。
综上所述,东阳光药(东阳光科)国内首仿上市(美国上市转报国内),很可能获得1.5年数据保护期,赢得市场先发优势。
@今日话题 @水里望月 @老狼牙 @天外飞仙闯股海 @People静谧Parker @wangfugui @陶朱公投资 @梦见莱茵 @格格丫丫 @刘轶南老师 @林奇法则 @TOPCP @HH卡西莫多 @金头和小狐狸的麻麻 @小西zs @舒颜 @大彤哥跑跳碰 @华宝医药_医疗