"ABSK011 irpagratinib 联合用药II期临床试验申请获受理。这是 irpagratinib 在单药肝癌二线治疗取得优异初期结果后,即将开展的一个联合用药临床实验。"
7月11日,据CDE官网显示,和誉医药自主研发的1类化药新药ABSK-011胶囊临床申请已获受理。

ABSK-011是一种高选择性小分子FGFR4抑制剂,拟开发用于治疗FGF19/FGFR4信号高度活化的晚期肝细胞癌(HCC)。
2022年11月,和誉披露了ABSK011对FGF19过表达的二线肝细胞癌患者的初步I期安全性及疗效结果。结果显示,其针对FGF19+HCC患者具有良好疗效,FGF19高度表达患者的客观缓解率(“ORR”)为22%(4/18),每日两次160mg群组中的ORR为33.3%(2/6),表现出良好的安全性,且未见4级或以上的药物相关不良反应。
目前,ABSK-011还在对FGF19过表达的晚期HCC患者进行联合抗PD-L1抗体阿特珠单抗的II期试验。
广泛布局FGFR 管线,
迭代研发泛FGFR、高选择性FGFR
FGFR全称成纤维生长因子受体(Fibroblast Growth Factor Receptor),属于酪氨酸受体激酶(RTKs)家族,包括FGFR-1、FGFR-2、FGFR-3、FGFR-4四种受体亚型。当FGFR发生异常时,通过驱动肿瘤细胞增殖、存活及促进血管生成,促进肿瘤发生和发展。根据弗若斯特沙利文统计,最常受FGFR异常影响的癌症包括泌尿上皮性膀胱癌(31.7%)、胆管癌(25.2%)、肝细胞癌(20.0%)、乳癌(17.5%)及胃癌(6 .7%),靶点可覆盖超16种癌种。
具体而言:
►FGFR1基因扩增在乳腺癌、肺部鳞状细胞癌、卵巢癌及尿道上皮癌较为普遍;
►FGFR2融合则于子宫颈癌及胃癌以及胆管癌中常见;
►FGFR3突变则于尿道上皮癌中常见;
►FGFR4通路则在肝细胞癌的过度激活中常见。
作为目前“不限癌种”疗法聚焦的热门靶点之一,FGFR正在成为越来越多制药企业研发管线中的标配,和誉医药正是其一。
和誉针对FGFR靶点布局了多款小分子药物,包括泛FGFR抑制剂ABSK091、ABSK121,以及高选择性FGFR2/3抑制剂ABSK061,高选择性FGFR4抑制剂ABSK011和ABSK012。
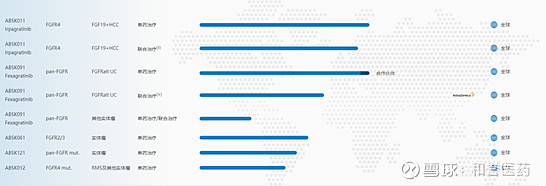
其中,进展相对较快的管线除了ABSK011以外,还有ABSK091和ABSK061,已迈入II期临床阶段。
ABSK091
ABSK091由和誉引进自阿斯利康,是一款针对FGFR1、2及3的高效选择性抑制剂,拟用于治疗多种实体瘤,包括尿路上皮癌、胃癌、胆管癌、肺癌及其它肿瘤。目前该药正在国内开展关于FGFR2/3基因变异的尿路上皮癌患者方面的II期临床试验,并与百济神州达成合作,与替雷利珠单抗启动联合疗法。
目前全球已有三款泛FGFR抑制剂获批上市,分别是强生的Balversa(厄达替尼)、Incyte的Pemazyre(佩米替尼)及QED Therapeutics的Infigratinib(英菲格拉替尼)。其中尚且只有佩米替尼在国内上市,信达生物拥有大中华区权益。
ABSK061
ABSK061由和誉自主研发的,该药靶向FGFR2/3亚型,也是全球范围内第一个进入临床阶段的FGFR2/3抑制剂。其在临床前的各项生化及细胞试验中,都表现出了对 FGFR2/3 的高选择性抑制以及对其他激酶的低活性。此外,在SNU16、RT4 两种肿瘤细胞模型中 ABSK061 均表现出了与厄达替尼相近的抗肿瘤活性、剂量依赖性地抑制肿瘤生长。
围绕FGFR靶点,和誉进行迭代研发,将泛FGFR抑制剂ABSK091与靶向特定FGFR亚型的FGFR抑制剂ABSK011、ABSK061互为补充,以期实现全面的适应症覆盖,也将为和誉在FGFR抑制剂领域奠定话语权基础。
ABSK-011能否带动和誉业绩增长?
高选择性FGFR4抑制剂市场还是一片尚无企业涉足的蓝海。据弗若斯特沙利文预测,中国和全球FGFR4药物市场在2025-2030年的复合年增长率分别为50.9%和60.1%,2026年中国和全球的FGFR4药物市场分别为2.08亿美元和5.55亿美元,2030年分别为7.40亿美元和24.35亿美元。
巨额市场,已吸引众多药企集结。据西南证券统计,目前全球范围内已有13款FGFR4抑制剂进入临床阶段,其中和誉的ABSK011(Irpagratinib)、诺华/云顶新耀的Roblitinib(FGF401)以及基石药业的Fisogatinib处于第一梯队,已迈入临床II期阶段。
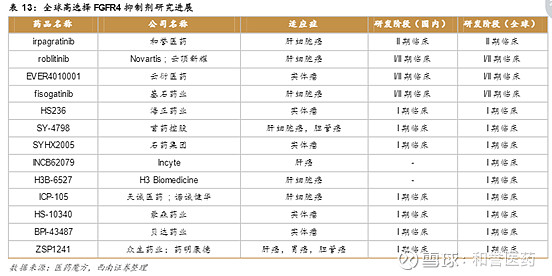
其中ABSK011于2019年12月获批I期临床,于2021年10月获批II期临床,不仅临床推进速度走在前列,基于其在临床前及I期的试验数据,有望成为研发进度及疗效均处于全球领先地位的FGFR4抑制剂。
此外,和誉还布局了新一代FGFR4突变抑制剂ABSK012,并于今年4月获得FDA授予的孤儿药资格认定,用于治疗软组织肉瘤。在临床前研究中,ABSK012在体外及细胞中均对野生型FGFR4及对临床开发中的FGFR4抑制剂具有耐药性的突变体表现出优异的活性,并在FGF19驱动及FGFR4突变体模型中展现了出色的体内功效。
百舸争流,ABSK-011能否在FGFR4抑制剂竞争中脱颖而出,验证和誉研发实力,值得期待。
参考资料:
1.企业官微公告
2..丰硕创投 凭FGFR4抑制剂ABSK011 ,和誉医药未来的业绩可能出现爆发增长