
近期,神刊CA发表了一篇关于肺癌和头颈部肿瘤免疫治疗的综述文章,系统介绍了免疫治疗在这两大癌种中的研究现状和发展方向。 $恒瑞医药(SH600276)$ $药明康德(SH603259)$ $信达生物(01801)$ #投资医药股#

非小细胞肺癌:晚期/转移阶段
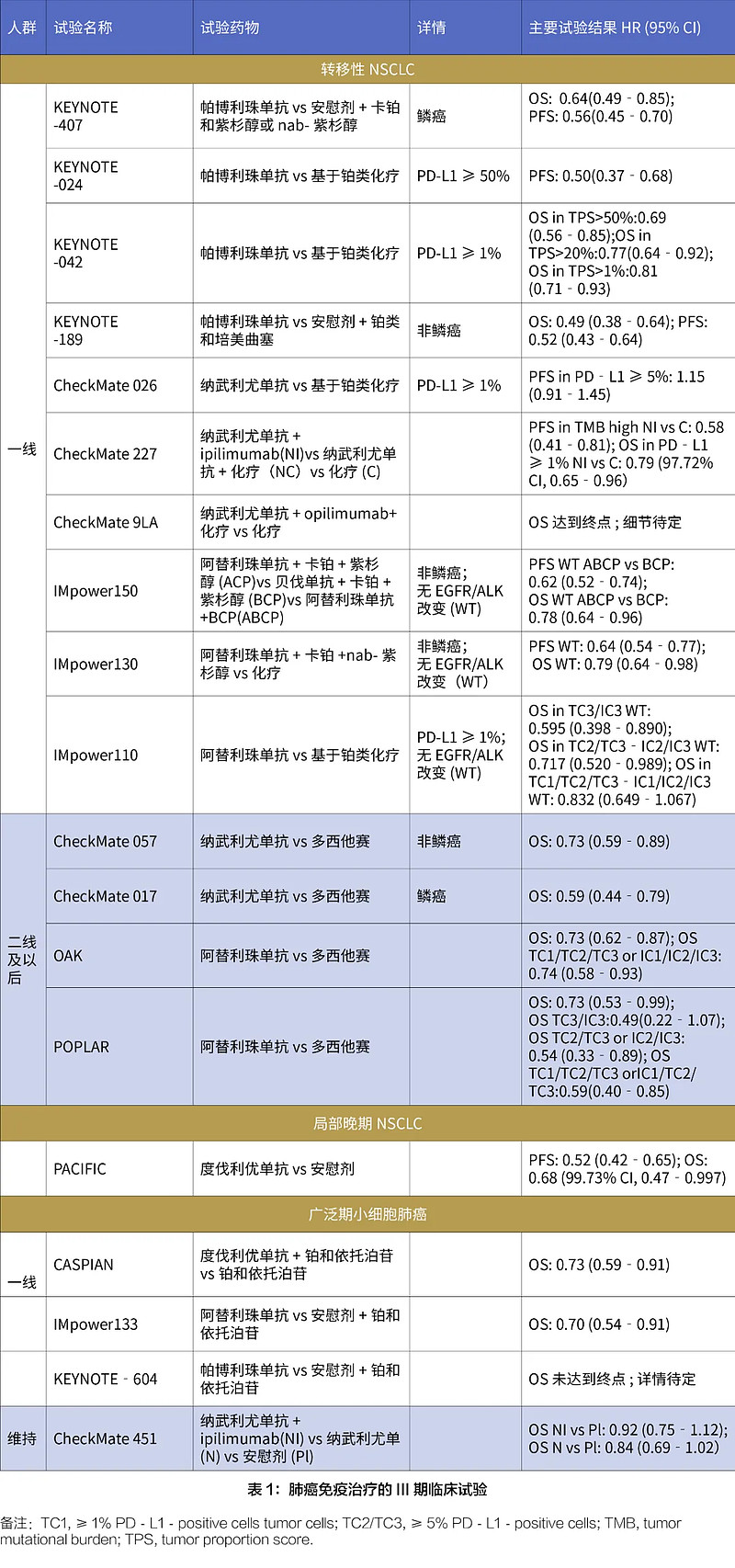
目前,免疫疗法广泛应用于非小细胞肺癌患者的治疗中,多种标准治疗方案已批准用于局部晚期和转移性患者(详见表1)。早期研究主要是PD-(L)1抑制剂单药在二线及以上非小细胞肺癌患者中进行,根据CheckMate 017(NCT16420054)、CheckMate 057(NCT01673867)、KEYNOTE-010(NCT01905657)和OAK(NCT02008227)试验结果纳武利尤单抗、帕博利珠单抗、阿替利珠单抗被批准后线治疗。
基于免疫疗法在后线治疗中较好的疗效,以及认识到PD-L1表达可作为预测性biomarker,促进了这些药物的一线测试。从KEYNOTE-024 (NCT02142738)研究开始,确立了PD-(L)1抑制剂一线治疗地位,在该研究中,PD-L1高表达、肿瘤细胞PD-L1表达评分(TPS)大于50%且EGFR或ALK基因无改变的患者,无论PFS和OS帕博利珠单抗组均显著优于化疗。对于那些可能无法耐受化疗且至少有1% PD-L1表达的患者,根据KEYNOTE-042(NCT02220894)研究也可以考虑使用帕博利珠单抗单药治疗。而具有高症状负担或疾病快速进展症状的患者可以采用化学联合免疫疗法进行治疗。对发生TKI耐药的患者,基于IMpower150试验的亚组分析数据,免疫治疗方案仍然是一种选择,但需要注意免疫相关不良事件(irAEs)。
非小细胞肺癌:局部晚期和早期
不能切除的III期非小细胞肺癌的治疗多年来一直采用同步铂类双重化疗和放疗 (CRT),并伴有或不伴有额外的巩固化疗,5年生存率仅为20%。临床试验PACIFIC (NCT02125461)研究了接受CRT标准治疗之后的患者服用度伐利优单抗和安慰剂的对比效果,结果度伐利优单抗组无论PFS和OS都获得了显著延长,且值得注意的是,PD-L1表达水平≥25%或< 25%的患者都有效。
在PACIFIC试验成功的基础上,目前正在测试如何利用免疫治疗通过预防非小细胞肺癌早期复发来改善预后。大型II期和III期研究正在进行中,研究对象包括手术切除后使用纳武利尤单抗、阿替利珠单抗、度伐利优单抗和帕博利珠单抗进行1年单药辅助免疫治疗。无复发生存率和OS数据预计将在2020年中后期成熟。
广泛期小细胞肺癌
目前,广泛期SCLC的一线标准治疗包括PD-1免疫治疗结合铂和依托泊苷化疗。根据IMpower133(NCT02763579)和CASPIAN(NCT03043872)临床试验结果,与标准治疗相比度伐利优单抗和阿替利珠单抗均显著延长了患者OS。
头颈部癌
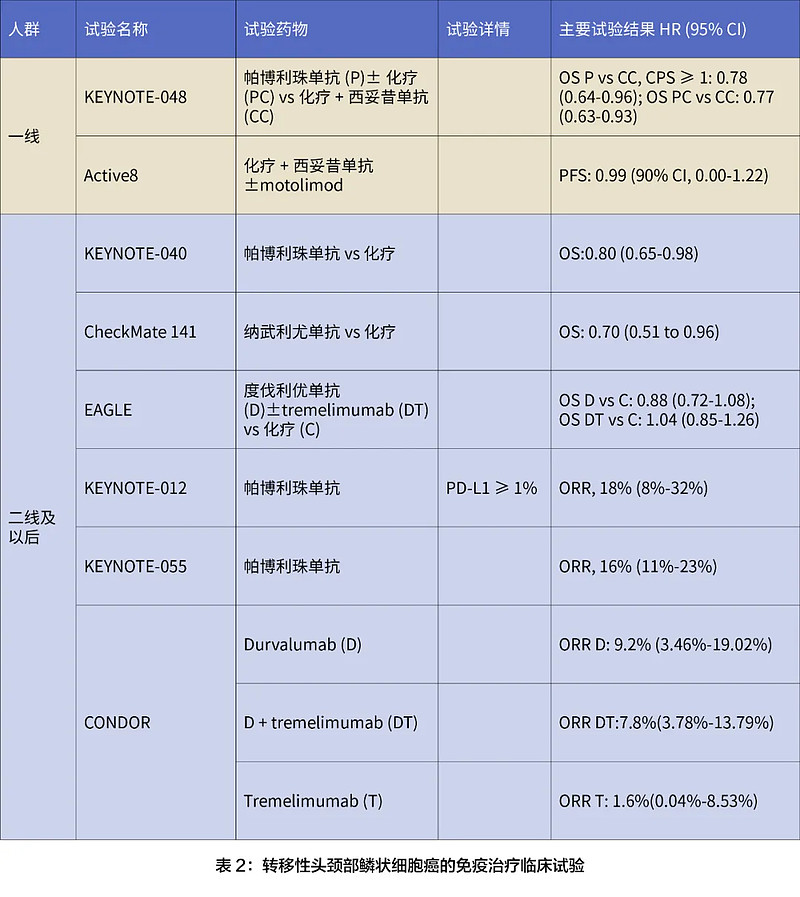
免疫治疗改变了HNSCC的治疗面貌(详见表2)。KEYNOTE-012(NCT01848834)是第一个证明免疫检查点抑制剂在该癌种有效的试验。并基于该试验较好的疗效,FDA在2016年批准帕博利珠单抗用于铂不耐受HNSCC患者的治疗。
CheckMate141(NCT02105636)是第一个证明在复发性转移性HNSCC人群中免疫治疗优于化疗的III期研究。随后的KEYNOTE-040(NCT02358031)、KEYNOTE-012 和KEYNOTE-055类似的对比了帕博利珠单抗与标准治疗(SOC)(西妥昔单抗、多西他赛或甲氨蝶呤),均取得了更好疗效和更低的毒副反应,这些数据牢固地确立了纳武利尤单抗和帕博利珠单抗作为HNSCC人群二线免疫治疗的地位。然而,并不是所有关于检查点抑制剂的研究都在复发性HNSCC中取得阳性结果,3期研究EAGLE就表明,与化疗相比,使用度伐利优单抗或度伐利优单抗联合Tremilumab治疗铂难治性HNSCC没有改善OS。
一直以来,复发和转移性HNSCC患者一线治疗方案都是EXTREME(包括铂、5-氟尿嘧啶(5-FU)和西妥昔单抗)。直到一项大型III期临床研究KEYNOTE-048的出现,对比了帕博利珠单抗±化疗与SOC疗效,在该研究中使用了CPS来评估肿瘤和免疫细胞上的PD-L1染色。基于该研究阳性结果美国FDA批准了帕博利珠单抗单药治疗CPS评分≥1的患者一线治疗,以及无论CPS评分如何,均可采用帕博利珠单抗联合化疗。
免疫治疗反应相关Biomarkers
PD- L1免疫组化表达是最广泛使用的生物标志物,但是,每一种PD(L)-1靶向抗体针对不同的癌种及适应症,会有不同的敏感性和分级标准。PD-L1表达水平会随时间变化,并且还存在瘤内异质性,其表达可能因转移部位不同而不同。TMB是免疫治疗反应的另一个研究性替代生物标志物。目前的想法是突变导致新抗原或新的免疫原性肽,这是这种关联的基础,但这可能是一个全基因组发现的简单化的观点。与PD-L1相似,TMB的测量随测试平台的变化而变化,并且也是一个动态的Biomarker;到目前为止,TMB评估并不是肺癌或HNSCC临床治疗的一个组成部分。对更好的预后和预测性生物标志物的研究仍在进行中。
总结
目前免疫检查点抑制剂在这两大癌种中均已达到了一线治疗地位,但是进展后的标准治疗方案仍然是传统的化疗。这突出了在对检查点抑制剂治疗的原发和继发耐药的情况下,对治疗选择的巨大需求。