
$恒瑞医药(SH600276)$ $药明康德(SH603259)$ $泰格医药(SZ300347)$
2020年6月19日,江苏恒瑞医药股份有限公司自主研发的PD-1抑制剂卡瑞利珠单抗(艾瑞卡®)正式获得国家药品监督管理局(NMPA)批准用于肺癌、食管癌领域的治疗,这是中国首个获批肺癌及食管癌适应症的国产PD-1抑制剂。
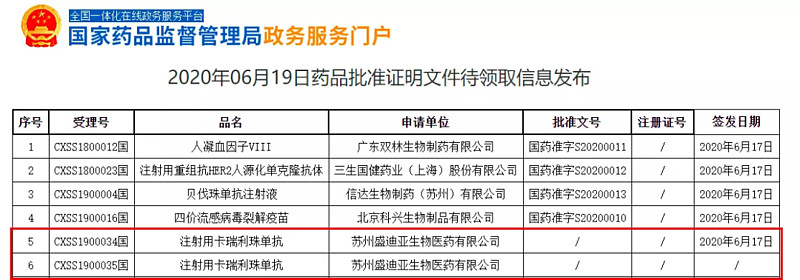
此次获批的适应症为:
01,卡瑞利珠单抗联合培美曲塞和卡铂适用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)的一线治疗。
02,卡瑞利珠单抗用于既往接受过一线化疗后疾病进展或不可耐受的局部晚期或转移性食管鳞癌患者的治疗。
在此之前,卡瑞利珠单抗已分别于2019年5月29日获得NMPA批准用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者的治疗;于2020年3月18日再次获得NMPA批准用于接受过索拉非尼治疗和/或含奥沙利铂系统化疗的晚期肝细胞癌患者的治疗。
自此,卡瑞利珠单抗已拥有4大适应症,成为覆盖适应症种类最多的国产PD-1抑制剂。
作为一款我国自主原研的创新药,卡瑞利珠单抗自问世起便备受行业关注,并多次登上国际舞台,获得国内外肿瘤领域广泛认可。日前,恒瑞医药与韩国CrystalGenomics公司签署协议将卡瑞利珠单抗许可给CG公司,在韩国进行临床开发、注册和市场销售,这标志着卡瑞利珠单抗已走向海外市场。本次肺癌、食管癌适应症的获批,强有力地丰富了我国肺癌、食管癌的治疗格局,同时创下了同一天获批两种适应症的行业记录。
肺癌—一线新星,颠覆格局
肺癌是全球最高发的恶性肿瘤。近年来,免疫治疗的出现将晚期肺癌患者的5年生存率从化疗时代的5%提升至15%,卡瑞利珠单抗肺癌适应症的获批将成为晚期肺癌治疗的一把“利器”。
此次卡瑞利珠单抗肺癌适应症的获批基于CameL研究—卡瑞利珠单抗联合卡铂+培美曲塞用于晚期/转移性 EGFR-/ALK-非鳞状非小细胞肺癌一线治疗的随机、开放、多中心III 期临床关键研究(登记号:NCT03134872)。该研究由同济大学附属上海市肺科医院周彩存教授牵头,是全球首个针对中国人群的非小细胞肺癌一线免疫联合化疗的III期研究。
该研究入组412例EGFR或ALK突变阴性的晚期非鳞状NSCLC患者,按照1:1随机分组,卡瑞利珠单抗组给予卡瑞利珠单抗(200mg)联合化疗(卡铂 AUC=5、培美曲塞500mg/m2),每3周为一个给药周期,治疗4-6个周期后使用卡瑞利珠单抗联合培美曲塞维持治疗,直到疾病进展或出现不可耐受的毒性反应;单纯化疗组给予化疗(卡铂 AUC=5、培美曲塞500mg/m2),每3周为一个给药周期,治疗4-6个周期后使用培美曲塞维持治疗,发生疾病进展的患者允许接受卡瑞利珠单抗单药交叉治疗。205例受试者接受了卡瑞利珠单抗联合化疗方案,207例接受了单纯化疗方案。
研究显示,卡瑞利珠单抗联合培美曲塞/卡铂的方案疗效强悍。ORR方面,卡瑞利珠单抗组达60.0% ,大幅高于化疗组的39.1% (p<0.0001);PFS方面,卡瑞利珠单抗组的中位PFS为11.3个月,同样高于化疗组的8.3 个月 (HR 0.61[0.46‒0.80], p=0.0002)。
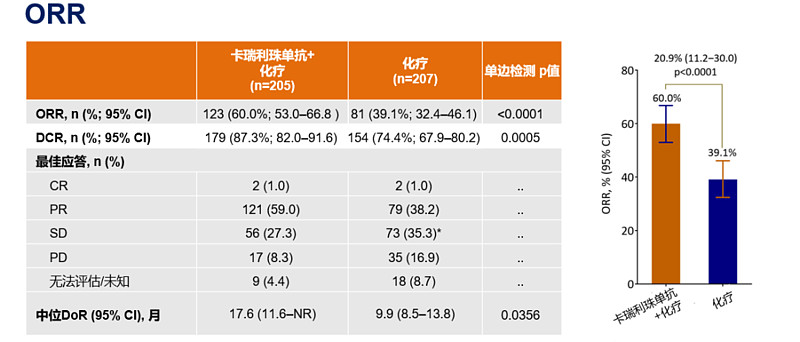
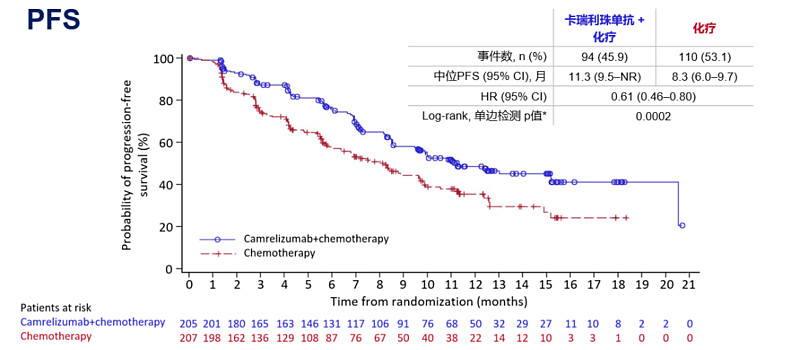
不论从ORR还是PFS上的获益来看,卡瑞利珠单抗的疗效数据源于中国患者群,更具优势。值得关注的是,CameL研究已于2019年世界肺癌大会(WCLC)上以口头报告公布,这一来自世界的认可,是卡瑞利珠单抗出色疗效的最好证明。在《2020CSCO非小细胞肺癌诊疗指南中》,卡瑞利珠单抗以1A类证据,成为唯一纳入指南推荐的自主研发免疫检查点抑制剂。
伴随着此次适应症的获批,卡瑞利珠单抗联合培美曲塞/卡铂方案有望成为该类患者新的一线标准治疗方案。
食管癌—更强免疫,中国智造
食管癌是极具“中国特色”的恶性肿瘤,我国每年新发食管癌病例数和死亡病例数占全球一半以上,而中国的食管癌患者90%以上为食管鳞癌,与欧美地区差异巨大,卡瑞利珠单抗食管癌适应症的获批为中国食管癌患者提供了“特效药”。
卡瑞利珠单抗食管癌适应症的获批基于ESCORT研究—卡瑞利珠单抗在既往接受一线化疗失败的晚期/转移性食管鳞癌患者中的随机、开放、化疗阳性对照、多中心III期临床研究。该研究由中国医学科学院肿瘤医院黄镜教授、解放军总医院第五医学中心徐建明教授牵头,共纳入457例既往接受一线化疗失败的晚期/转移性食管鳞癌患者,入组患者按1:1随机分配为卡瑞利珠单抗组(228例)和化疗组(220例),分别接受卡瑞利珠单抗单药治疗(200 mg,每2周给药一次)或研究者选择的化疗方案治疗:多西他赛(75 mg/m2,每3周给药一次)或伊立替康(180 mg/m2,每2周给药一次),研究的主要终点为总生存期(OS)。
研究结果显示,与化疗相比,卡瑞利珠单抗可显著延长患者的中位OS(mOS,8.3个月对6.2个月,HR=0.71,95%CI为0.57~0.87,P=0.001),降低死亡风险近30%,同时卡瑞利珠单抗组患者的客观缓解率更高(ORR,20.2%对6.4%),持续缓解时间更长(DoR,7.4个月对3.4个月,HR=0.34,95%CI为0.14~0.92)。更重要的是,卡瑞利珠单抗在所有人群中均可获益,也因此在中国独家获批了全人群的适应症,较同类进口产品适应症有着更广泛的适用人群。
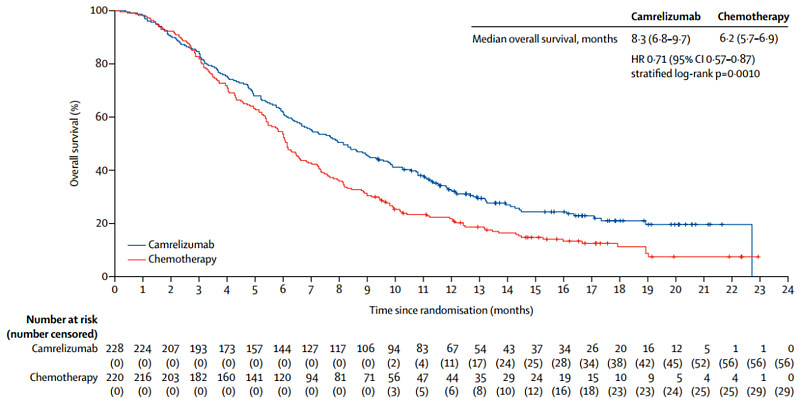
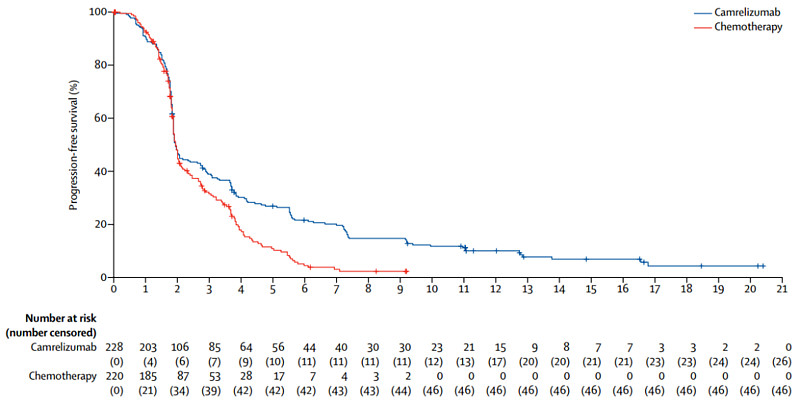
ESCORT研究结果已于2019年世界食管疾病大会(OESO)上口头报告公布,展示了中国食管癌学者在免疫治疗领域的探索成果;今年5月,ESCORT研究结果登上国际顶级期刊《柳叶刀·肿瘤学》杂志。而在日前公布的《2020版中国临床肿瘤学会(CSCO)指南》中,卡瑞利珠单抗更是以1A类证据,作为I级推荐用于晚期食管鳞癌的二线治疗。这些来自国内外的认可,充分证明了卡瑞利珠单抗的强劲疗效,以及在食管癌中的治疗地位。
更强免疫,源自恒瑞
伴随着肺癌、食管癌适应症的获批,卡瑞利珠单抗已拥有4大适应症,成为获批适应症最多的国产PD-1抑制剂,不论在肺癌、食管癌领域的比肩国际,还是在肝癌、淋巴瘤领域的引领首创,卡瑞利珠单抗都已成为我国免疫检查点抑制剂中的佼佼者。多个高级别循证医学证据交叉印证了卡瑞利珠单抗在肿瘤治疗中的强悍疗效。
作为民族医药企业的龙头,近年来,恒瑞医药坚持原研,为中国医生提供好的“武器”,为中国患者提供更多的治疗机会。据悉,卡瑞利珠单抗后续的研发布局也极为“豪华”,不仅聚焦于现有适应症和癌种的联合用药,更致力于其他癌种的适应症拓展。
中国医药企业虽起步晚,它曾一穷二白、落后低迷,但近年来,国人欣喜地看到了它的成长,等到了它的崛起。如今,中国的原创研究已逐步开始主导中国的临床实践,中国的原研药物正在加速实现“弯道超车”,国人首次看到了可以主导自己命运的曙光。这是莫大的踏实感和底气,中国人的健康终于可以掌握在中国人自己的手上。
期待卡瑞利珠单抗未来可以造福更多的中国患者,为抗击肿瘤事业贡献更多中国力量!
