
$恒瑞医药(SH600276)$ $誉衡药业(SZ002437)$ $华大基因(SZ300676)$
今天,FDA正式批准K药(帕博利珠单抗,可瑞达)单药治疗肿瘤突变负荷高(TMB-H,TMB≥10个突变/百万碱基)且既往治疗后疾病进展的无法切除或转移性实体瘤患者,无需考虑癌症类型。2020年4月FDA已授予K药这一适应症的优先审评资格,预期的决定时间是2020年6月16日。这也是2017年FDA已批准K药用于MSI-H/dMMR的不限肿瘤类型的实体瘤适应症后,第二次基于分子标志物选择的 “泛癌种”适应症,数据支撑同样都来源于KEYNOTE-158研究结果。TMB几年前闪亮登场被寄予厚望,后来历经波折饱受质疑,到如今首次获得FDA批准认可,可谓上演了一出完美的王者归来。
TMB-H是更好的分子标志物
KEYNOTE-158研究数据表明,tTMB-H的患者为99例,占比达13.2%。而tTMB-H中MSI-H仅占14.1%,非tTMB-H中MSI-H为0,MSI-H是TMB谱中表达最高的部分。相比MSI-H,使用TMB-H作为分子生物标志物,能够筛选出更多免疫治疗获益患者,扩大获益人群。
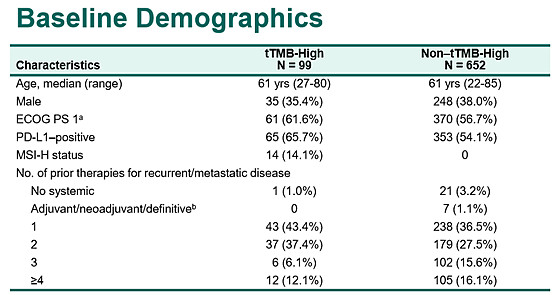
TMB-H是独立有效的分子标志物
KEYNOTE-158研究中大部分患者将K药作为二线或三线治疗,甚至是四线或者五线治疗,TMB-H仍然是有效预测疗效的分子标志物。在tTMB-H组,59.1%患者的靶病灶缩小,45.5%患者的靶病灶超过30%的缩小,9.1%患者的靶病灶100%缩小,相比非tTMB-H均有显著改善。TMB-H患者的总缓解率达到30.3%,排除MSI-H后为27.1%,而非tTMB-H组仅为6.7%。TMB-H能够独立于MSI-H预测免疫治疗疗效。
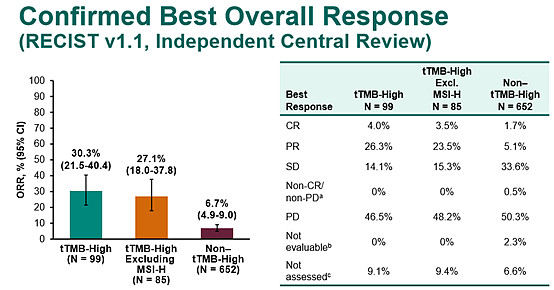
TMB-H是泛癌种有效的生物标志物
KEYNOTE-158研究入组无法手术切除和或转移性癌症,标准治疗失败或者无法耐受的患者,包含的肿瘤类型有胆道腺癌,神经内分泌肿瘤,子宫内膜癌,宫颈鳞状细胞癌,外阴鳞状细胞癌,小细胞肺癌,甲状腺癌和唾液腺癌等。按照肿瘤类型确认的客观缓解率,大部分癌种中tTMB-H组的获益都要明显超过非tTMB-H组,表明TMB-H是泛癌种有效的生物标志物。
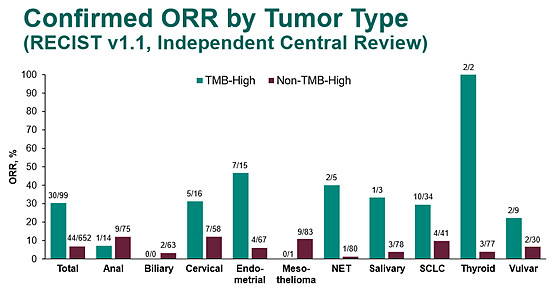
TMB-H代表更高的无进展生存率
KEYNOTE-158研究数据中,6个月,12个月和24个月的PFS率均是tTMB-H组更高,特别是24个月时,TMB-H患者中无进展生存率为18.9%,而非TMB-H患者中仅为6.5%。时间越久,K药的优势越明显。
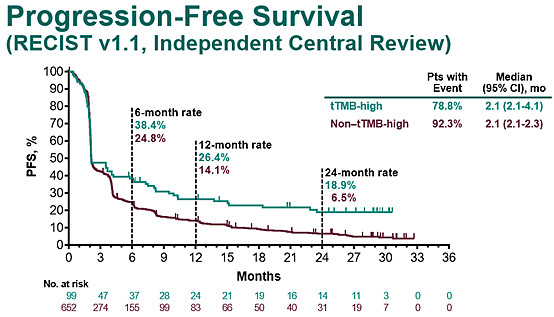
本次TMB-H首次获得FDA批准认可,用于辅助指导K药泛癌种的免疫治疗,不仅有助于筛选更多免疫治疗获益患者,也给其他尚在研究的免疫治疗分子标志物极大的信心。免疫治疗早已进入了精细化治疗时代,单一的分子标志物已不足以满足多样复杂的诊疗需求,多组学多个分子标志物的研究和检测已是必不可少,势在必行。