原创: 玲珑
来源:米内网
精彩内容
近日,江西省发布通知:同品种药品通过一致性评价的企业达到3家以上的,未通过企业暂停其网上采购资格。据米内网统计,截至8月16日,有5个品种(3个在2017年全国销售额超过10亿元)通过一致性评价企业数达3家,涉及企业112家,有5个品种(4个在2017年全国销售额超过10亿元)即将锁定“1+3”格局,涉及企业277家。一致性评价政策逐渐明朗,企业的步伐得加快了,一旦3家已定,未通过者出局,这意味着将市场拱手相让。
非一致性评价品种淘汰赛,江西开始了
8月10日,江西省医药采购服务中心发布《关于延长“双信封”中标结果采购周期及通过仿制药一致性评价药品挂网采购事项的通知》,通知指出,对于已有3个通过一致性评价的产品,暂停未通过一致性评价产品的网上采购资格,也不接受未通过一致性评价的动态增补报名申请。
其实早在2016年3月国务院办公厅印发《关于开展仿制药质量和疗效一致性评价的意见》中就明确:同品种药品通过一致性评价的生产企业达到3家以上的,在药品集中采购等方面不再选用未通过一致性评价的品种。
截至目前,因药企未通过一致性评价而直接暂停网上采购的省份还较少,更多的省份还处在及时将过一致性药品直接挂网采购的阶段。如今随着通过一致性评价品种数增加,达到3家的品种也越来越多了,达到了政策要求,于是江西打响了第一枪,顿时给尚在排队中的企业更强的紧迫感。
需要注意的是,江西省的公告用了“暂停采购”,这意味着虽然同一品种3家企业通过一致性评价之后,不再采购未通过的企业的品种,但只要该企业后期申报并通过了一致性评价,还是可以重返医院市场的,但能否中标,中多少钱价格,那就不得而知了。
不过可以看到的是,一致性评价政策在逐渐明朗,一旦3家的格局已定,未通过一致性评价者出局只是时间早晚的问题,而这也意味着将市场拱手相让,因此企业们的步伐就更得加快了。
5个品种已有3家企业通过一致性评价
从江西省公布的信息看,山东仙河药业的蒙脱石散(3g)和安徽贝克生物的富马酸替诺福韦二吡呋酯片(300mg)已被暂停网上采购资格,暂停原因是:以上产品未通过一致性评价,且已有其他3家企业通过一致性评价,故暂停其网上采购资格。
表1:一致性评价通过企业达3家的品种
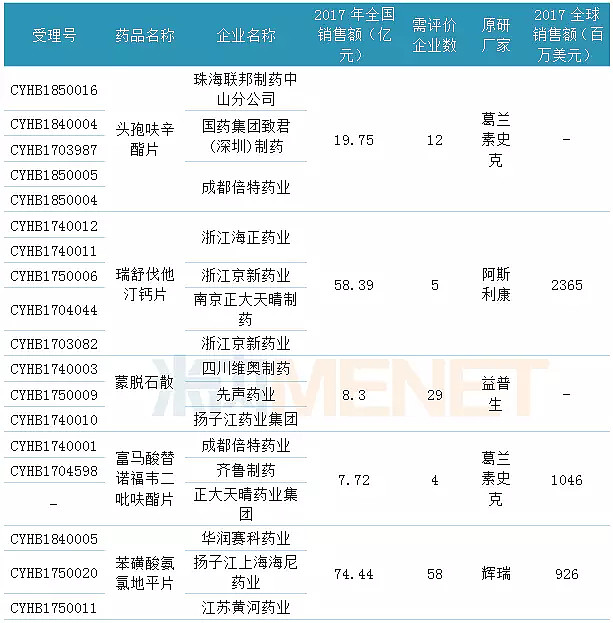
(来源:米内网数据库,数据统计截至8月16日)
截至8月16日,已有5个品种通过一致性评价企业数达3家,除了蒙脱石散和富马酸替诺福韦二吡呋酯片外,还有头孢呋辛酯片、瑞舒伐他汀钙片及苯磺酸氨氯地平片,其中瑞舒伐他汀钙片、苯磺酸氨氯地平片在2017年全国销售额均超过50亿元。
目前拥有头孢呋辛酯片生产批文的企业有13家,除了原研厂家葛兰素史克外,其余12家企业均需要开展一致性评价。珠海联邦制药中山分公司、国药集团致君(深圳)制药、成都倍特药业均已成功“通关”,苏州中化药品、浙江京新药业、白云山天心制药这3家企业已申报该品种一致性评价,国药集团汕头金石制药、华北制药河北华民药业、石药集团欧意药业这3家企业正处于BE试验阶段。
图1:2017年中国公立医疗机构瑞舒伐他汀钙片竞争格局
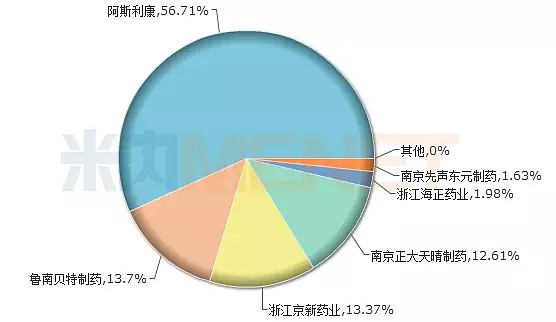
(来源:米内网中国公立医疗机构终端竞争格局)
据米内网数据,2017年瑞舒伐他汀钙片全国销售额为58.39亿元,其中在中国公立医疗机构终端的销售额为50.19亿元,同比去年增长22.86%。目前拥有瑞舒伐他汀钙片生产批文的企业有6家,除了原研厂家阿斯利康之外,其余5家企业都需要进行一致性评价。
从瑞舒伐他汀钙片在2017年中国公立医疗机构终端的竞争格局看,原研厂家阿斯利康占据一半以上的市场份额,已通过一致性评价的浙江海正药业、浙江京新药业、南京正大天晴制药所占市场份额分别为1.98%、13.37%、12.61%。鲁南贝特制药、南京先声东元制药、ek Pharmaceuticals d.d.这3家企业也申报了该品种的一致性评价,目前还处于“在审评审批中”。
目前拥有蒙脱石散生产批文的企业有30家,除了博福-益普生(天津)制药外,其余29家企业均需要开展一致性评价。在进行一致性评价时,蒙脱石散可豁免BE试验,在此政策红利下,申请该品种一致性评价企业数激增,除了已经通过的四川维奥制药、先声药业、扬子江药业集团3家企业外,目前有山东绿叶制药、哈药集团中药二厂、杭州康恩贝制药等6家企业正在申报一致性评价,此外共有22家企业进行了该品种的参比制剂备案。
目前拥有富马酸替诺福韦二吡呋酯片生产批文的企业有5家,除了原研厂家葛兰素史克外,其余4家都需要进行一致性评价,成都倍特药业、齐鲁制药2家企业已按照一致性评价补充申请申报且通过了,正大天晴药业集团按照新注册分类申报生产,获批后视同通过一致性评价。除此之外,安徽贝克生物制药正在申报该品种一致性评价,目前正处于“在审评审批中”,4家需评价企业均有不同程度的进展。
图2:2017年中国公立医疗机构瑞苯磺酸氨氯地平片竞争格局
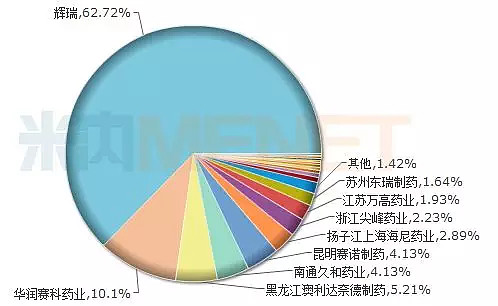
(来源:米内网中国公立医疗机构终端竞争格局)
苯磺酸氨氯地平片2017年全国销售额为74.44亿元,其中在中国公立医疗机构终端的销售额为55.12亿元,同比去年增长8.84%。目前拥有瑞舒伐他汀钙片生产批文的企业有59家,除了原研厂家辉瑞之外,其余58家企业都需要进行一致性评价。
从苯磺酸氨氯地平片在2017年中国公立医疗机构终端的竞争格局看,原研厂家辉瑞占据大部分市场份额,已通过一致性评价的华润赛科药业、扬子江上海海尼药业所占市场份额分别为10.1%、2.89%,江苏黄河药业在医院终端的销售量较小。此外,辰欣药业、亚宝药业、浙江京新药业等7家企业正在申报该品种的一致性评价,东阳光长江药业、重庆科瑞制药、南京海辰药业、白云山制药总厂、山东方明药业等19家企业正处于BE试验阶段。
5个品种即将锁定“1+3”格局
表2:一致性评价通过企业已达2家的品种
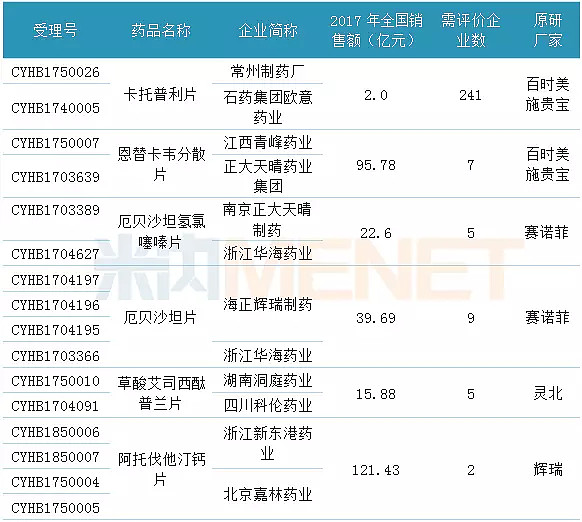
(来源:米内网数据库,数据统计截至8月16日)
截至8月16日,共有6个品种通过一致性评价企业数达到2家,只要再有1家企业通过,那么在招标采购中就不再选用未通过一致性评价品种了。这6个品种中,阿托伐他汀钙片虽有6家企业拥有生产批文,但实际需要进行一致性评价的企业只有2家,分别为浙江新东港药业、北京嘉林药业,目前这2家企业均已顺利通过一致性评价,不受限于上述一致性评价政策。
目前拥有卡托普利片生产批文的企业多达241家,除了原研厂家施贵宝,剩下的企业都需要开展一致性评价工作,目前按照一致性评价补充申请申报且通过的企业是常州制药厂和石药集团欧意药业,山东罗欣药业正在申报该产品的一致性评价,已经开展BE试验约有10家企业,无法预测第三家通过企业,但至少200家企业将面临出局风险。
表3:部分一致性评价通过企业已达2家的品种的一致性评价申请情况
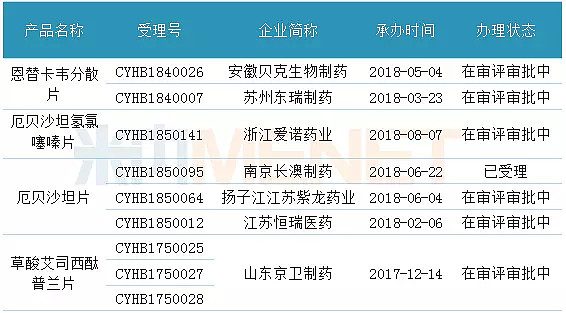
(来源:米内网数据库,数据统计截至8月16日)
恩替卡韦分散片,8家企业拥有该品种生产批文,7家企业需要进行一致性评价工作。目前按照一致性评价补充申请申报且通过的企业是江西青峰药业和正大天晴药业集团,安徽贝克生物制药和苏州东瑞制药还处于一致性评价申请阶段,从承办时间看,苏州东瑞制药承办时间更早,预计也会较快有审评结果。此外,湖南千金协力药业的BE试验也正在开展中,山东鲁抗医药及海南中和药业还未有进展。
厄贝沙坦氢氯噻嗪片,6家企业拥有该品种生产批文,5家企业需要进行一致性评价工作。目前按照一致性评价补充申请申报且通过的企业是南京正大天晴制药、浙江华海药业,处于一致性评价申请阶段的是浙江爱诺药业处于一致性评价申请阶段,预计会成为该品种第3家通过的企业。常山生化药业暂无进展。
厄贝沙坦片,10家企业拥有该品种生产批文,9家企业需要进行一致性评价工作。目前按照一致性评价补充申请申报且通过的企业是海正辉瑞制药(现改名瀚晖制药)和华海药业,南京长澳制药、扬子江江苏紫龙药业、江苏恒瑞医药3家企业还处于一致性评价申请阶段,从承办时间看,江苏恒瑞的承办时间更早,预计会是第3家通过的企业。扬子江北京海燕药业、南京长澳制药、深圳市海滨制药这3家企业的BE试验也正在开展中,其他企业暂无进展。
草酸艾司西酞普兰片,6家企业拥有该品种生产批文,5家企业需要进行一致性评价工作。目前按照一致性评价补充申请申报且通过的企业是湖南洞庭药业和四川科伦药业,山东京卫制药还处于一致性评价申请阶段,预计会是第3家通过的企业,金华康恩贝生物制药和吉林西点药业暂无进展。
注:本文BE试验开展情况根据已上市药品参比制剂备案、临床试验公示情况、一致性评价CDE审评情况等信息综合统计,如有疏漏,欢迎指正。
来源:米内网数据库、江西省医药采购服务中心