2006年-2024年,18年历程、独有的基因编辑技术平台、巨头药企青睐合作、IPO当天股价暴涨超3000%、股价最高超过710美元/股,这些都是Precision Biosciences的高光。
被药企退货、打包出售管线和团队、可支持运营至2026年下半年的现金、几乎所有管线都在临床前,是Precision目前的处境。
美好的开始
2004年,杜克大学的博士后Jeff Smith博士和Derek Jantz博士新发现一种天然归巢内切酶I-CreI,并基于此开发了ARCUS基因组编辑平台,以及于2006年创立Precision BioSciences。
最早,ARCUS基因组编辑平台成功应用在玉米、大豆、棉花和其他农作物上;后来便扩展到基因治疗领域。随着在医学治疗领域上的研究和发展,Precision将食品和农业的业务拆分为Elo Life Systems,作为全资子公司运营。
Precision起初在医学领域,为ARCUS基因组编辑平台瞄定了两大方向——体外“通用”CAR-T和体内基因编辑治疗,最主要的重点应该还是体外“通用”CAR-T细胞。
Azercabtagene Zapreleucel(azer-cel,PBCAR0191)是Precision最早推进临床的产品,也曾被Precision吹捧为“潜在的第一款商业化异体CAR-T”——Precision公司在2023年7月收到了与FDA就azer-cel举行的B类会议的最终会议纪要,进一步明确了azer-cel的潜在注册路径,包括研究设计。
此外,由于当时基因编辑的兴起,以及ARCUS基因组编辑平台相较于其他基因编辑技术的优势,吸引了药企巨头们的青睐,吉利德、诺华、礼来等纷纷与Precision达成大金额合作。
先被吉利德退货
2018年9月,吉利德与Precision达成一项合作,利用ARCUS基因编辑平台开发体内消除乙型肝炎病毒(HBV)的创新疗法。根据协议,Precision将有机会获得总计高达4.45亿美元的里程碑付款,以及商业化后的分层特权使用税。
但是可惜的是,2020年9月,吉利德和Precision终止了该合作,Precision重新获得该乙肝项目的全部临床开发和商业权利。
该项目当时在2020年美国遗传与细胞治疗学会(ASGCT)年度会议上发表了临床前数据,数据显示优化的ARCUS核酸酶可有效靶向并降解cccDNA 达 75%,并伴随HBV感染原代人肝细胞中的乙肝表面抗原敲低。来自鼠类研究的数据还显示,在体内单次给药后,脂质纳米颗粒(LNP)传递的ARCUS核酸酶可编辑高达70%的HBV DNA靶标。
一款CAR-T卖了两次
事实上,Precision曾经最领先的管线CD19异体CAR-T细胞治疗azer-cel,是Precision与施维雅合作开发的,施维雅曾拥有该项目的全球开发和商业化权利。
后来,因azer-cel展现出较强的潜力。Precision于2021年4月与施维雅签订了一项购买协议,收购了双方关于CAR-T合作的所有项目的全球开发和商业化权利,包括azer-cel、PBCAR19B以及其他四个项目。
2023年5月,Precision更新了azer-cel的数据,数据显示:azer-cel在r/r NHL患者(n=61)中,ORR为58%,CR为41%;具有可接受的安全性。在自体CAR-T治疗后复发的患者中(n=18)疗效更为显著,ORR达到83%,CR为61%。在可评估的自体CAR-T复发患者中(n=11),55%的患者≥6个月持续缓解。安全性方面:未观察到≥3级的CRS、ICANS、感染和移植物抗宿主病。
这个数据在一众同种异体CAR-T项目中,还算不错。尽管如此,Precision还是选择将该项目出售,以募集资金专注于体内基因编辑药物的开发。
2023年8月,Precision宣布,将azer-cel肿瘤相关适应症的全球权利、CAR-T基础设施和细胞治疗团队一起打包出售Imugene Limited。根据协议,Precision公司将获得2100万美元的前期收益(现金和股权),以及后续的付款。
2024年1月,Precision宣布与TG Therapeutics达成交易,将azer-cel自身免疫性疾病以及癌症以外相关适应症的全球权利授予TG Therapeutics。根据协议,Precision获得了1750万美元的前期付款,以及后续的里程碑付款,和产品销售的分级特许权使用费。
在新闻稿中,Precision表示后续将专注于体内基因编辑疗法的开发,做一个体内基因编辑单一技术平台公司。
出售临床CAR-T管线,获得资金能够缓解Precision公司当时面临的现金压力,同时节省后续临床开发的费用,这也是Precision公司的用意之一。
分手礼来
2024年4月16日,Precision宣布,礼来的全资子公司Prevail Therapeutics结束了双方关于体内基因治疗项目的合作。Precision行使了选择权,重新获得了包括DMD项目在内的三个项目的权利,预计将来独立开发或者寻找新的合作伙伴共同开发。
该消息传出后,当日收盘,Precision公司股价大跌10.57%。
礼来/Prevail与Precision的合作可以追溯到2020年11月,但似乎礼来/Prevail与Precision的分手早有预示——9个月之前,双方重新调整了协议,降低了里程碑付款。同时,礼来/Prevail接管了为第一个潜在项目制造初始临床试验材料的责任,原本是由Precision负责,Prevail资助。
这些信息其实透露出,礼来/Prevail对于双方合作项目的进度太慢而感到不满。
说实话,对于DMD来说,市场上已经有商业化的基因治疗产品,以及几款临床后期产品。而礼来/Prevail与Precision合作的项目于2020年11月开始,三年多的时间还未推进IND准备阶段,确实是进度太过落后,未来的市场又过于激烈。
但无论如何,礼来的退货对于决心做专注于体内基因编辑的单一平台公司的Precision来说,是一个重大打击。
双方合作历史信息:
2020年11月,礼来与Precision达成一项研究合作和独家许可协议,将利用Precision公司专有的ARCUS基因编辑平台开发遗传性疾病的潜在疗法,其首要关注目标是杜兴氏肌营养不良症(DMD),此外还有两个未公开的目标病症。根据协议,礼来向Precision公司支付1亿美元现金的预付款,并投资3500万美元购买Precision公司的普通股票。此外,Precision还能够获得可以获每个项目最高4.2亿美元的潜在里程碑付款,以及产品销售的分级特许权使用费。
2020年12月,礼来以8.8亿美元收购了Prevail,并指派Prevail接管与Precision的合作项目。
2023年7月,Prevail宣布重新修订了与Precision之前的协议。根据新条款,两方继续合作开发Precision的ARCUS核酸酶,为DMD和两个基因靶标开发体内基因疗法。但降低了里程碑付款金额,从原始协议的每个许可产品4.2亿美元里程碑付款降低至3.9亿至3.95亿美元。其他目标的潜在提名费和特许权使用费的条款没有改变。
管线推进太慢
管线进度太慢是Precision面临的一个很严峻的问题。
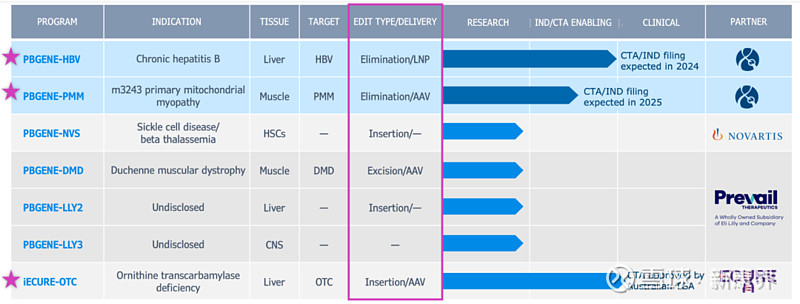
在出售CAR-T项目之后,Precision目前的管线均为体内编辑项目,除了一款与iECURE合作的项目之外,其他均处于临床前阶段。
进度最快的是与iECURE合作的OTC缺陷项目,IND和CTA已经在美国、英国和澳大利亚获得批准,预计将于2024年启动首次人体临床给药。
在被吉利德退货后,Precision全资拥有的PBGENE-HBV,正在进行最终的IND和CTA支持研究,努力向临床推进,计划于今年提交相关申请。
另外还有一款突变线粒体DNA项目PBGENE-PMM也计划有望在2025年提交IND或CTA。
其他管线就剩下还在更早期概念验证阶段的,被礼来退货的三款项目(PBGENE-DMD、PBGENE-LLY2、PBGENE-LLY3),以及和诺华合作的PBGENE-NVS。
小编总结
目前,Precision公司通过CAR-T项目的两笔交易、与Caribou Biosciences签署的授权许可(授予Caribou一项非排他性的全球许可,并有权再许可Precision的基础细胞疗法专利家族之一,用于CRISPR的人类治疗领域)、以及公开发行,募集了9000万美元的资金。
加上原有的现金,截至2023年12月31日,Precision拥有1.167亿美元的现金和现金等价物。
同时,Precision通过管线精简,相较于之前,全资拥有的管线相对早期运营费用降低,合作项目有合作方付款;现金能够支撑Precision运营至2026年下半年。
参考资料:
1.网页链接
2.网页链接
END
◆新康界广泛征集投稿,内容可涉及医药政策、研发动向、资本市场等产业相关话题,投稿请发送至(hejing@sinohealth.cn),请注明联系方式;
◆商务合作/转载开白,请联系13610303540(微信同号)。
点击下面,关注新康界,获取更多热点分析/行研报告/蓝皮书。
【免责声明】
1.“新康界”部分文章信息来源于网络转载是出于传递更多信息之目的,并不意味着赞同其观点或证实其内容的真实性。如对内容有疑议,请及时与我司联系。
2.“新康界”致力于提供合理、准确、完整的资讯信息,但不保证信息的合理性、准确性和完整性,且不对因信息的不合理、不准确或遗漏导致的任何损失或损害承担责任。
3.“新康界”所有信息仅供参考,不做任何商业交易及或医疗服务的根据,如自行使用“新康界”内容发生偏差,我司不承担任何责任,包括但不限于法律责任,赔偿责任。
4.本声明未涉及的问题参见国家有关法律法规,当本声明与国家法律法规冲突时,以国家法律法规为准