在2021年12月2日某公众号中说礼来裁员PD-1业务线,予以N+1奖励,主要可能原因是销售不及预期并且本身就会跟信达合作

2. 有信息说FDA的Pazdur说中国数据有问题

根据以上信息大概可以推测Pazdur可能是FDA肿瘤卓悦中心主任Richard Pazdur

此外还有某会议纪要截图流传出来,其中也有人在问礼来信达合作的Tyvyt(信迪利单抗)的情况,关注FDA对于Tyvyt(信迪利单抗)的审批情况,会议纪要中的回答也比较偏保守

在2021年5月份的时候也有消息说FDA可能会在2022年3月份前有进展,并且Richard Pazdur公开表示FDA将根据中国的临床数据来做决定

3. 可能是受此影响,港股biotech大跌
截止2021年12月17日下午15:30,康宁杰瑞、信达生物、康方生物等biotech公司都出现了较大跌幅
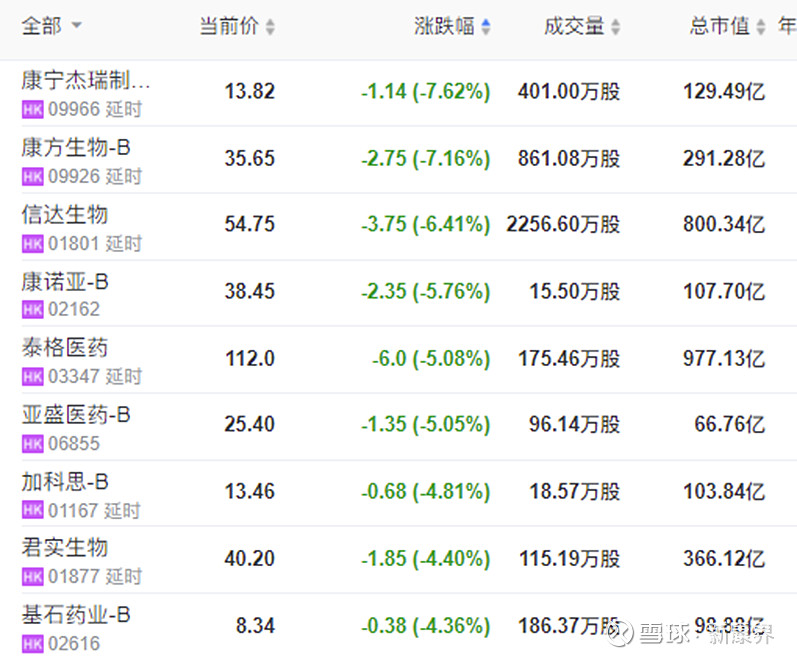
5.在传闻较多,目前仍需冷静分辨
创新药大熊市的情况下,任何风吹草动都会让市场过度反应,但现在尚未有官方信息,尚且是传闻,若情况属实,国内biotech公司将会迎来更大的挑战,仅用国内临床数据可能会更加难以获批,其研发成本将会进一步增加。
但在今天15:30的时候,本人又收到一些的信息,说FDA对于结果比较认可,还请各位读者仍需冷静对待目前的各类传闻!
FDA肿瘤卓越中心(Oncology Center of Excellence,OCE)主任Richard Pazdur正在敦促中国公司将PD-1/PD-L1抑制剂引入美国市场,降低跨国制药公司的定价。
在美国癌症研究协会(American Association for Cancer Research)的一次名为“东方与西方相遇:中国制药探索西方市场”的会议上,Pazdur在问答环节中发表了讲话:“中国公司在美国竞争PD-1的价格,可能对所有人都是件好事,因为我们还没有看到西方主要制药公司在价格上做出改变”。
Pazdur说,FDA可能只根据中国的临床数据批准药物,包括PD-1/PD-L1抑制剂。去年夏天访问中国时,经常有人问他,FDA是否会接受只在中国产生临床数据的申请。他说:“如果质量好,答案是肯定的” 。
他说,他还被问及FDA在做出监管决定时是否考虑价格。Pazdur说,FDA不考虑价格,但他也明确表示,FDA将欢迎价格低廉的PD-1/PD-L1抑制剂。
他指出,美国已经批准了6个PD-1药品,价格没有差别。FDA已经批准了7家公司的6种PD-1/PD-L1抑制剂,用于近50种适应症:Merck的Keytruda pembrolizumab、Bristol-Myers Squibb的Opdivo nivolumab、Roche的Tecentriq atezolizumab、Merck KGaA和Pfizer的Bavencio avelumab、AstraZeneca的Imfinzi durvalumab和Regeneron的Libtayo cemiplimab-rwlc。
Pazdur表示,跨国制药公司已经为PD-L1药物制定了一套方案,可以简化竞争产品的开发。
“我可以看到一个非常简单的开发战略,”他说。“例如,在肺癌方面,你可以简单地做一些大型制药公司已经做过的研究。事实上,你已经知道效应值(effect size),所以这些是非常、非常低风险的研究,可能会导致药物得到批准。”
在谈到这个话题时,Pazdur告诉中国企业:“你不必做非劣效研究。你已经知道效应值了。这里风险很小。他补充说,统计计划写起来会很容易,“你甚至不需要成为一名统计学家就能做到这一点。”
他还建议,FDA基于模仿FDA批准产品的开发方案批准中国的PD-1将是顺利的。“很明显,它们可能会产生非常相似的结果,所以我们在批准这些药物方面几乎没有什么可说的。”

作者:剑舞之秋,创新药领域的个人投资人
新康界注:本文仅限于交流行业观点,不做任何投资推荐,以上信息为作者供稿,新康界不保证以上信息属实,新康界将持续跟踪此事件,也欢迎各位读者后台回复“交流”进行沟通及获取图片原文链接。
