
日前,据外媒 Endpoints News 披露,艾伯维停止了一项 CD47 抗体 Lemzoparlimab(来佐利单抗)的临床试验,这项临床试验旨在评估 Lemzoparlimab 与口服或静脉注射地塞米松制剂联用或不联用,以及联合抗骨髓瘤方案在成人多发性骨髓瘤(MM)中的治疗效果。
这项临床试验始于今年1月,原定于 2025 年 7 月完成。该临床试验由艾伯维主持,原定招募 163 名患有 R/R MM 的成年受试者在全球 60 个地点参与该临床研究。根据 clinicaltrials 官网的数据,实际上,艾伯维只招募了 8 名受试者,并于今年 6 月 24 日就停止了此项临床研究。
此前,吉利德旗下 CD47 抗体 Magrolimab 也曾遭遇了一系列临床挫折。目前 Magrolimab 与 Azacitidine 联用治疗 MDS 和 AML 的临床研究已于 4 月恢复,针对弥漫性大 B 细胞淋巴瘤和MM的临床研究于 6 月恢复。

(来源:clinicaltrials)
在 clinicaltrials 官网可以看到,在这项研究停止状态处标明了艾伯维停止临床的原因——出于战略考虑。
这一观点在天境生物回复外媒的一封电子邮件中也得到了证实。“该研究是一项艾伯维发起的探索性试验,最近艾伯维由于战略原因停止了这项临床试验。”
天境生物在邮件中还表明,艾伯维并非因为安全问题做出停止研究的决定,并表示取消这项临床试验并不会影响潜在的里程碑付款。
据公开资料介绍,Lemzoparlimab 是一款差异化且具有 BIC 成药潜力的“独特”CD47 抗体。这款候选药根据 CD47 在红细胞表面糖基化的修饰情况进行大规模筛选,能够最大程度减少与正常红细胞结合,从而减少 CD47 抗体引发的严重贫血等副作用。目前,Lemzoparlimab 联合疗法治疗 AML/MDS 和实体瘤的多项临床研究正在美洲、欧洲、澳洲和亚洲多个地区开展。
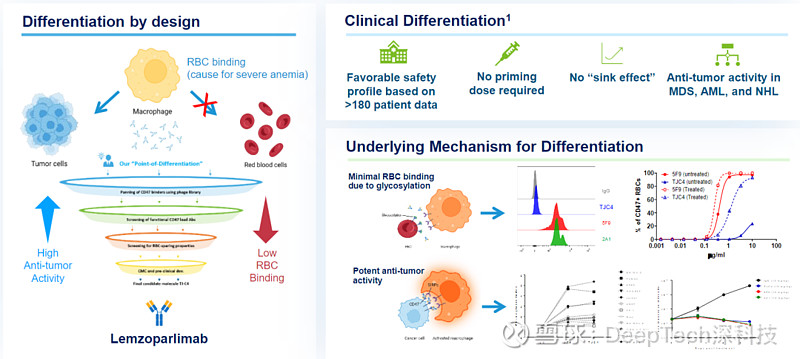
(来源:天境生物研发日活动资料)
Lemzoparlimab 由天境生物自主研发,2020 年 9 月,艾伯维与天境生物达成全球合作协议,在全球共同开发和商业化后者的在研抗癌药 Lemzoparlimab。为此,艾伯维将支付高达 19.4 亿美元的首付款和里程碑付款。根据合作协议,双方将合作设计并进一步在全球范围开展临床试验,评估 Lemzoparlimab 在多种癌症中的治疗潜力。
在 clinicaltrials 官网也可以看到,艾伯维正在主持另一项 Lemzoparlimab 联合疗法治疗急性髓系白血病(AML)和骨髓增生异常综合征(MDS)的临床研究,评估 Lemzoparlimab 在 AML 和 MDS 中的治疗潜力。这项研究于 2021 年 6 月 25 日开始,目前正在招募受试者。
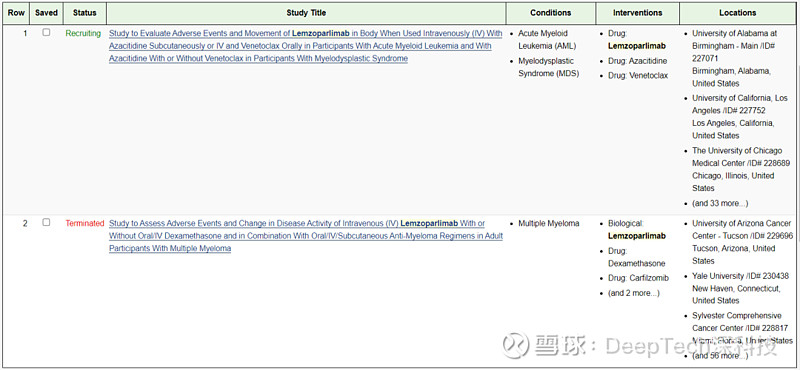
(来源:clinicaltrials)
天境生物方面也在测试该药物在治疗 MDS、其他血液恶性肿瘤以及在实体瘤治疗上的潜力和价值。此外,天境生物还在推进旗下在研药 CD38 抗体 Felzartamab 用于治疗 MM,并表示预计 2023 年在中国递交 BLA。
近日,天境生物还宣布将于 2022 年欧洲肿瘤内科学会(ESMO)年会期间通过优选口头报告方式公布 Lemzoparlimab 与阿扎胞苷联合治疗初诊中高危骨髓增生异常综合征(HR-MDS)的临床 2 期研究数据。
参考资料:
1.网页链接
2.网页链接
3.网页链接

