“明日之星”CD47分化:罗氏、艾伯维、吉利德减速,康方、信达却迎来曙光!
原创 Tim/Ling/Mars 2023-01-15 12:13 发表于上海
作为继PD-1、PD-L1、CTLA-4之后新一代免疫肿瘤学疗法的热门靶点,CD47自2020年爆发以来备受追捧。无论是Big Pharma还是Biotech,都布下重兵激战这一热点技术。凭借与PD-1相似的广谱治疗特性,CD47也被称为肿瘤学疗法的“明日之星”。
然而,CD47单抗相关血液学毒性严重限制其临床应用。仅仅过了两年,CD47赛道就出现了巨大分化:有人果断放弃,也有人迎来曙光。问题是,作为热门靶点的CD47,到底是一场共襄盛举的豪门盛宴,还是一个吞噬一切的研发黑洞?只有更多的临床数据才能给出答案。
1药企巨头减速
1月13日,据Endpoints独家披露称,Arch Oncology结束了抗CD47抗体AO-176的临床开发,全体员工已经遣散,目前该公司官网已经无法打开。
作为CD47领域的明星公司,Arch Oncology之前的可谓顺风顺水,吸引了包括罗氏在内的众多投资方顺利完成多轮融资,并且获得了FDA授予的孤儿药资格。
► 2019年3月,Arch Oncology完成5000万美元的B轮融资,由Lightchain领投,罗氏风险基金参与。募集资金用于加速针对CD47靶点的潜在Best-in-class的AO-176临床开发。
► 2021年4月,Arch Oncology宣布完成共计1.05亿美元的C轮融资,罗氏风险基金再度参投。
► 2022年1月,FDA授予AO-176孤儿药资格,用于治疗复发/难治性多发性骨髓瘤(r/r MM)。
获授孤儿药资格仅一年之后,一切便戛然而止。值得注意的是,在CD47这一热门靶点方向,Arch Oncology的挫败并非个案。► 2022年6月,艾伯维终止了Lemzoparlimab(来佐利单抗/TJC4)用于多发性骨髓瘤(MM)的1期临床研究,具体原因未披露,但明确并非涉及任何安全性问题。
► 2022年8月16日,天境生物披露,艾伯维又终止了Lemzoparlimab+阿扎胞苷+venetoclax联合治疗骨髓增生异常综合征(MDS)/急性髓系白血病(AML)的1期临床,同样并非是安全性问题。
好消息是,除MDS/AML和MM两项研究外,对于其他适应症,艾伯维与天境仍在合作推进。
作为天境生物自主研发的一款差异化CD47单抗,Lemzoparlimab能有效地靶向肿瘤细胞,同时将对红细胞产生的不良影响降至最低,从而可避免严重贫血。
2020年9月,艾伯维以1.8亿美元首付款及最高17.4亿美元里程碑付款从天境生物引进 Lemzoparlimab ,拿下Lemzoparlimab大中华区以外的开发和商业化权益。
CD47领域地另一玩家——再鼎医药,在此前的2022年半年报里,也因CD47未达预期,且基于不断变化的竞争格局,降低了CD47抑制剂ZL1201的内部开发优先级。ZL1201已完成第一阶段临床试验,且已确定了临床II期的推荐剂量。
再往前追溯,2022年1月,吉利德宣布部分暂停CD47抗体+阿扎胞苷联合治疗的所有临床研究,CD47抗体其他临床研究则不受影响。
2康方和信达却迎曙光?
罗氏、吉利德、艾伯维等医药巨头减速,让CD47这一领域地研发蒙上一层阴影,不过,来自中国的两家创新药企业,最近却发布积极成果,又让人们看到这一领域地一丝曙光。
2022年12月12日,康方生物宣布其自主研发的新一代CD47单抗(AK117)的作用机制研究成果全文发表于肿瘤免疫学核心期刊《癌症免疫治疗杂志》(JournalforImmunoTherapyofCancer,JITC)。
AK117是康方生物自主研发的一种新型人源化IgG4抗CD47抗体,无血凝作用,可诱导巨噬细胞对肿瘤细胞的强大吞噬作用,无需较低的预剂量来预防贫血,且抗肿瘤活性良好。
作为新一代CD47单抗,AK117有望在临床实践中带来更好的疗效、安全性,以及适应症的拓展:
AK117具有较好的抗体结合活性,可高效阻断SIRPα与CD47相互作用。AK117可高亲和力特异性结合人CD47,竞争性结合活性与Hu5F9-G4相当。
AK117不引发红细胞凝集,其机制可能与CD47的结合表位有关。AK117不会诱导人红细胞的血凝反应,且直到3000nmol/L仍不会引起人红细胞凝集;相比之下,Hu5F9-G4在浓度≥4.1nmol/L就会诱导人红细胞凝集。其机制可能与结合表位有关。
AK117可诱导巨噬细胞的肿瘤吞噬,在小鼠模型中抗肿瘤活性良好。AK117剂量依赖性地诱导巨噬细胞对肿瘤细胞的强吞噬作用,与Hu5F9-G4活性相当。AK117在小鼠模型中产生的抗肿瘤活性和Hu5F9-G4治疗疗效无显著差异。
AK117单药或联合AK112显示出显著的抗肿瘤活性。AK117单药或联合AK112(PD-1/VEGF双抗)在小鼠模型中抗肿瘤疗效明显,抗肿瘤活性良好。
AK117较Hu5F9-G4,安全性优势突出。在食蟹猴中的毒理学研究数据显示,AK117不引起红细胞凝集,与Hu5F9-G4相比,AK117引起贫血的程度更轻,且快速恢复,安全性更好。
2022年12月11日,信达生物在2022年美国血液病学年会(ASH)上公布了IBI188(抗CD47单克隆抗体)治疗一线初诊中高危骨髓增生异常综合征(MDS)的临床数据更新。
MDS全球发病率约为(2~12)/10万,中国发病率为(0.23~1.51)/10万,且随着年龄增高,发病率显著增高。如果不接受治疗,中高危患者中位生存期只有0.8~1.6年。IBI188是信达生物自主研发的IgG4型重组全人源抗CD47单克隆抗体。本次Ib期队列研究旨在评估IBI188联合阿扎胞苷在一线初诊中高危骨髓增生异常综合征受试者中的安全性、耐受性和有效性。
截至2022年10月20日,共有93例既往未接受过系统治疗的初诊中高危骨髓增生异常综合征受试者接受了IBI188(从0.1mg/kg诱导剂量逐渐升至30mg/kg维持,QW)联合阿扎胞苷治疗。
在接受超过6个周期治疗的30例受试者中,客观缓解率(ORR)为100%(30/30),完全缓解率(CRR)为63.3%(19/30)。
在接受超过4个周期治疗的42例受试者中,ORR为97.6%(41/42),CRR为45.2%(19/42)。
在接受超过3个周期治疗的49例受试者中,ORR为93.9%(46/49),CRR为38.8%(19/49)。
中位缓解持续时间(mDOR)未达到。
安全性方面,88例(94.6%)受试者出现治疗相关不良事件(TRAEs)。最常见的TRAEs包括血小板降低,贫血,白细胞降低、中性粒细胞降低等。7例(7.5%)患者因为TRAEs导致研究药物停药。
3CD47未来何去何从?
作为一种广泛表达的跨膜糖蛋白,CD47既表达于红细胞、T细胞,也在肿瘤细胞中高表达。CD47通过与SIRPα的相互作用向巨噬细胞传递抗吞噬信号。针对CD47开发抗体类药物需要攻克多个难点:首先在安全性方面,需要避免误伤红细胞和T细胞;在有效性方面,仅仅阻断CD47-SIRPα相互作用不足以激活巨噬细胞,激活这类细胞依赖于Fc-FcgR相互作用,所以CD47抗体需要选择IgG亚类。积极的一面在于,CD47在多种实体瘤细胞及恶性血液瘤细胞上呈现高表达,而且其表达水平与疾病进展呈正相关。这一广泛表达性意味着CD47或将是继PD-1之后肿瘤治疗领域的下一个重要靶点。凭借与PD-1相似的广谱治疗特性,CD47药物一旦成功获批上市,其潜在市场也可能接近PD-1的规模。正因如此,CD47已成为继PD-1/PD-L1及CTLA-4之后的新一代免疫肿瘤学疗法的热门靶点,已有多家企业入局。据Insight数据显示,全球共有123款靶向CD47新药在研。其中单抗39款,而双抗48款。此外,还涉及抗体类融合蛋白、ADC、化药等。2020年以来,从首次申报临床的国产单抗新药来看,CD47靶点名列前茅。CD47/SIRPα通路抗体药多达27 款。天境生物、信达生物、宜明昂科、翰思生物、恒瑞医药、再鼎医药、康方生物、石药集团等多家企业都已布局该领域,甚至单、双抗并进,广泛覆盖。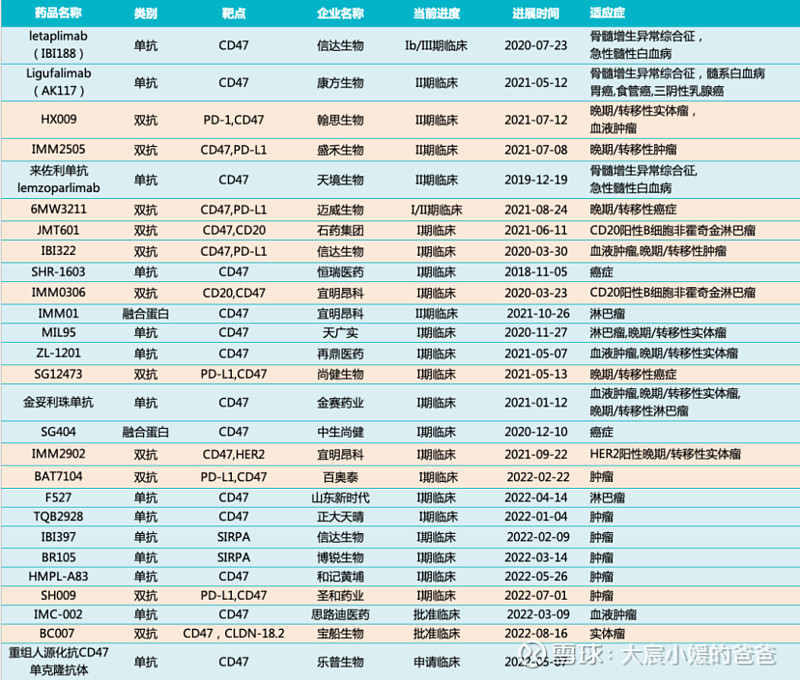
表格来自:Insight整理
从成分类别来看,单抗最多,已有14款。CD47双抗居次位,共布局有11款。如信达的IBI-322,可靶向肿瘤细胞表面CD47与PD-L1。石药布局的JMT601同时靶向 CD47/CD20。此外,2款融合蛋白在研。其中,宜明昂科的IMM001是国内首款进入临床阶段的SIRPα-Fc融合蛋白,具有IgG1Fc的IMM01能够通过双重作用机制充分激活巨噬细胞,同时通过干扰CD47/SIRPα相互作用阻断抗吞噬信号,并通过激活巨噬细胞的Fcγ受体传递吞噬信号。可见,在CD47这一热门靶点,中国创新药企业同样冲锋在前,尤其是在罗氏、吉利德、艾伯维等巨头减速的背景下,康方生物和信达生物呈现出良好的发展势头。这也是中国创新药企业研发实力的一个突出表现。
值得注意的是,虽然全球市场有无数以CD47为靶点的候选药物正处于临床前及临床开发阶段,但目前中国及美国仍无获批准的抗CD47疗法。
作为热门靶点的CD47到底是一场共襄盛举的豪门盛宴,亦或是一个吞噬一切的研发黑洞,也许只有更多的临床数据才能给出答案。