
本文由医麦客原创,欢迎分享,转载须授权
2020年2月5日/医麦客新闻 eMedClub News/--据2月3日港交所披露易披露,国内生物科技公司康方生物科技(开曼)有限公司(以下简称康方生物,H01309.HK)再次向港交所交了上市申请表,这是康方生物第二次向港交所递表。
2019年12月3日,康方生物首次向港交所递表,但是12月5日因财务资料准备不足被被港交所发回。


疫情对药企IPO的影响
武汉爆发的新型冠状病毒疫情推高了大量制药企业(主要是海外制药企业)的股价,似乎也迫使一些国内生物科技公司放慢了在香港的IPO计划。
据彭博社(Bloomberg)报道,总部位于北京、专注于癌症和自身免疫性疾病的InnoCare Pharma(诺诚健华)决定推迟旨在评估港交所上市需求的投资者会议。据匿名内部人士透露,InnoCare原本计划融资约2亿美元。这可能标志着许多中断的IPO计划中的第一个,具体取决于大流行是否会发生,以及随后会以多快的速度发生。
InnoCare(诺诚健华)在去年10月份提交的文件中表示,它将把IPO的大部分收益分配给主导药物orelabrutinib。orelabrutinib是一种BTK抑制剂,已被NMPA接受用于治疗复发或难治性慢性淋巴细胞白血病和小淋巴细胞淋巴瘤。另外两个临床阶段的资产分别针对pan-FGFR和FGFR4,此外还有是6个希望进入I期的候选药物。
尽管中国内地与香港之间的主要港口目前仍在开放,但许多支持首次公开发行的机构投资者和他们聘请的账簿管理人都处于危机状态。银行已经开始要求从中国大陆回来的员工在家工作两周(大约是2019-nCoV的潜伏期),这可能会使与公司高管的会面变得困难。此外,旅行限制已经暂停了面对面的讨论,一位欧洲银行家告诉彭博社(Bloomberg),他将在海外待更长时间。
但在为期10天的春节假期后中国股市重新开盘出现灾难性暴跌之际,一些已经在香港或中国内地上市的制药公司却成为一些罕见的亮点。
歌礼生物(Ascletis)是港交所上市的首家创收前生物科技公司。该公司在通知投资者其正与医疗机构合作,准备推出ASC09和ritonavir试验性组合的临床试验后,股价飙升19%,至4.95港元。该生物技术公司表示,他们已经向国家药品监督管理局(NMPA)提交了一份紧急使用申请,将这种原本用于治疗HIV的药物用于治疗2019-nCoV感染。
上海医药(Shanghai Pharma)、哈尔滨医药集团(Harbin Pharmaceutical Group)和豪森(Hansoh)等知名药企也实现了个位数增长,尽管它们表面上并未采取任何措施来抗击冠状病毒。但也并不是所有的船都能浮起来。尽管药明生物(WuXi Biologics)宣布已经成立了一个专门的团队来开发中和病毒的抗体,但该公司的股价仍保持在99.65港元的水平。

尚无产品创收但管线丰富的康方生物
康方生物团队由来自全球知名药企工作多年的免疫学家、抗体药物研发和GMP生产专家组成,于2012年3月创建成立。自康方生物成立以来,康方生物开发出独特的Tetrabody双功能抗体开发技术,成为现有屈指可数的获得生产和临床验证的双抗平台之一;以及端对端平台(ACE平台),涵盖了所有药物研发和开发功能,包括靶点验证、抗体发现与开发、CMC和符合GMP要求生产。

2015年7月,A轮融资1.3亿元;由深圳创新投资集团、中山迅翔资本、上海建信资本、深圳前海信诺共同出资
2015年11月,康方生物与默沙东就一项肿瘤免疫疗法的单克隆抗体药物AK107的研究、开发和推广达成合作,合作高达2亿美元。
2017年8月,B轮融3亿元人民币;高特佳投资领投、A轮领投机构深圳创新投资,原股东前海母基金以及前海勤智资本共同参与。
2018年10月,C轮融资数亿元;汇桥资本领投,原投资人深圳创新投资集团、前海勤智资本、建信资本海外基金共同参与。
2019年11月,D轮融资约1.26亿美元;正新谷创新资本和中国生物制药领投的投后估值8.36亿美元。

目前该公司已建立了逾30个抗体新药产品线,涵盖肿瘤、自身免疫性疾病、心血管疾病、炎症、代谢疾病及痛症等疾病领域,其中10个品种处于国内及国际临床试验阶段,4个针对广谱恶性肿瘤和重大免疫性疾病的抗体新药入选国家卫计委“重大新药创制”科技重大专项课题。
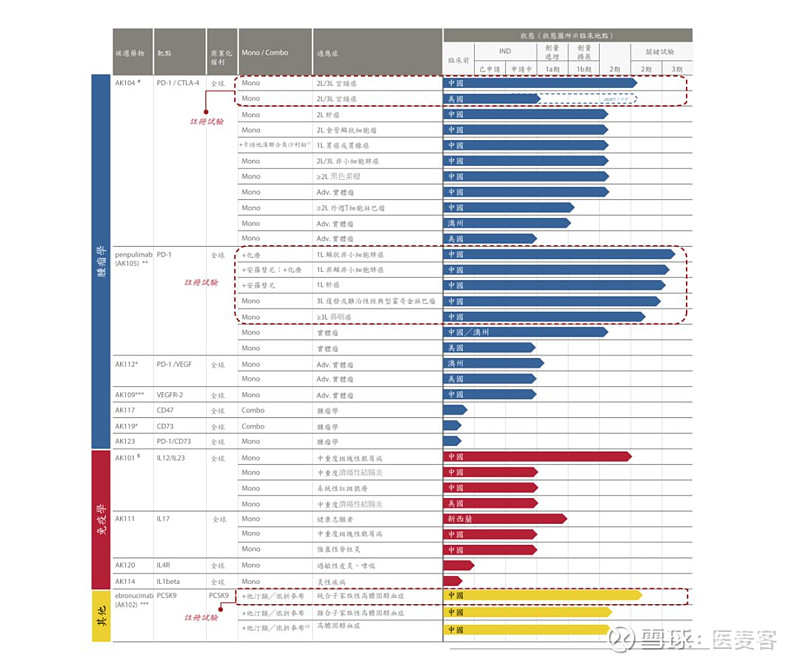
▲ 康方生物产品管线(康方生物公司官网)
根据弗若斯特沙利文资料,在生物制剂的市场份额中,单克隆抗体是最大的分部,按销售收入计,2018年占全球生物制s剂市场的55.3%。全球最畅销的10种药物中有9种为单抗。其中,PD-1/L1及CTLA-4单抗被视为最有效的单治疗剂免疫性肿瘤抗体疗法。
康方生物专注于研发此类药物并得到国际领先药企的认可。2015年自主研发了CTLA-4单克隆抗体候选药物AK107,并将其授权给默克,总对价高达2亿美元,因此康方生物成为了中国第一家向全球领先制药公司授权完全自主研发的单克隆抗体的生物技术公司。除默克外,康方生物还和中国生物制药(01177.HK)的主要附属公司正大天晴合作,开发及商业化PD-1抗体候选药物AK105。
不过,虽然康方生物产品线众多,但公司目前并无产品获批准进行商业销售,也没有来自产品销售产生的任何收入。康方生物目前的收入全部来自许可收入,包括与对外授权产品(包括AK107、AK103及AK106)有关的预付款及里程碑付款。但是康方生物D轮投资后,其估值从2015年10月A轮的3.3亿人民币升到了8.36亿美元,四年估值涨幅超过17倍。

2019年4月2日,康方生物旗下子公司康方药业有限公司的抗PD-1/CTLA-4双特异抗体新药——AK104的临床试验IND获得美国食品及药物管理局(FDA)的批准,将在美国开展针对多种恶性肿瘤的临床试验。
AK104是新一代的抗肿瘤免疫治疗药物,是康方生物利用康方独特的Tetrabody双抗平台自主研发,全球首个进入临床试验的PD-1/CTLA-4双特异抗体。目前,AK104已在澳洲完成Ia期剂量爬坡临床研究,在中国已启动Ib/II期临床试验,主要评估AK104单药治疗晚期实体瘤和AK104联合标准化疗一线治疗针对不可手术切除的晚期或转移性胃腺癌或胃食管结合部腺癌患者的有效性和安全性。
目前,公司正在加大临床开发的投入,将在中国和海外加速开展一系列II期和III期AK104单药以及AK104联合用药的临床研究,寻求在合适的适应症加速AK104获批可能性。
2019年7月1日,其自主研发的基于其Tetrabody双抗平台的PD-1/VEGF双特异抗体新药AK112获得美国FDA颁发的药物临床试验(IND)批件,是继AK104后康方生物再次获得美国FDA IND批件的双特异抗体。

结语
目前,受新型冠状病毒疫情的爆发,众多行业的业务与运营受到影响,地方经济、中国经济均受到损害,康方生物此时提交上市申请,其收益及盈利能力也可能会下降;资本市场的未来动向值得关注!
参考出处:
康方生物官网
热文精选
Nature子刊:给CAR-T安上开关,小分子STOP-CAR控制系统显示早期潜力
最新:HIV多抗体的联合疗法增强感染个体的免疫反应
最新:欧洲药品管理局接受葛兰素史克靶向BCMA的抗体偶联药物(治疗多发性骨髓瘤)上市许可申请
最新:百时美施贵宝撤回Opdivo与 Yervoy联用治疗非小细胞肺癌的欧盟申请

点击“阅读原文”,可以下载很多干货哦!