作者:Kirkland Hwang
微信公众号:蹊之美股生物医药 / CaesarBiotech
标的公司:Syndax Pharmaceuticals, Inc.(NASDAQ:SNDX)
• MLLr或NPM1c患者的总有效率达48%;有效患者中67%达到MRD阴性
• 确定了2期临床治疗剂量
• 公司已在启动计划于2021年2季度开展的关键性临床2期试验
Syndax制药公司(NASDAQ:SNDX)是一家临床阶段的生物制药公司,正在开发创新管线用于癌症治疗。该公司今天公布了正在进行的对于SNDX-5613的AUGMENT-101 1/2期研究中,1期试验部分的最新积极数据。截止4月21日收盘,公司股价跌30.75%。
该试验用于混合谱系白血病基因重排(MLLr)和核磷蛋白(NPM1c)突变的复发/难治性(R/R)急性白血病患者。SNDX-5613是该公司的高选择性口服Menin蛋白(多发性内分泌癌蛋白)抑制剂。
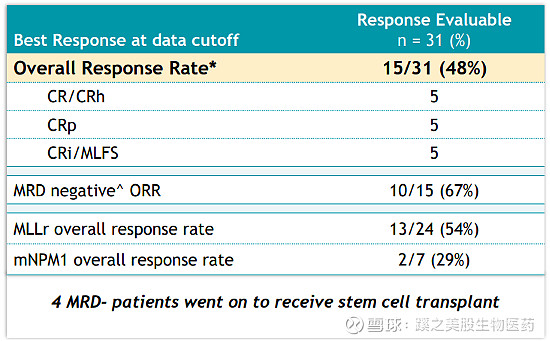
至2021年3月12日数据截止日,共43名患者参与了AUGMENT-101研究并接受治疗。这些患者在研究开始前均接受多次治疗(如先期干细胞移植,BCL-2小分子抑制剂venetoclax治疗,化疗等),中位数为3次。数据截止日时,共31名患者可评估疗效,其余患者尚未进行初始疗效评估(n=4)或未携带MLLr或NPM1c突变(n=8)。可评估患者的总有效率(ORR)为48%(15/31),其中67%(10/15)的患者达到MRD(白血病微小残留病变)阴性,其中4例患者继续接受了干细胞移植。携带MLLr的可评估患者有24名,ORR为54%(13/24);携带NPM1c突变的可评估患者有7名,ORR为29%(2/7)。
对于未接受强CYP3A4抑制剂治疗的患者,候选RP2D(2期临床试验推荐剂量)为226 mg /12h;对于接受强CYP3A4抑制剂治疗的患者,候选RP2D为113mg /12h。在RP2D治疗的18例患者疗效可评估,观察到的反应情况与总体人群一致。
在数据截止日,43例患者中,34例患者(79%)停止治疗,15例患者因疾病进展:
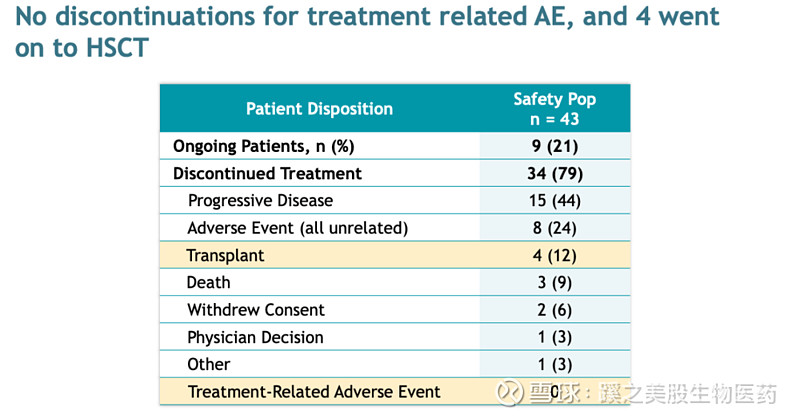
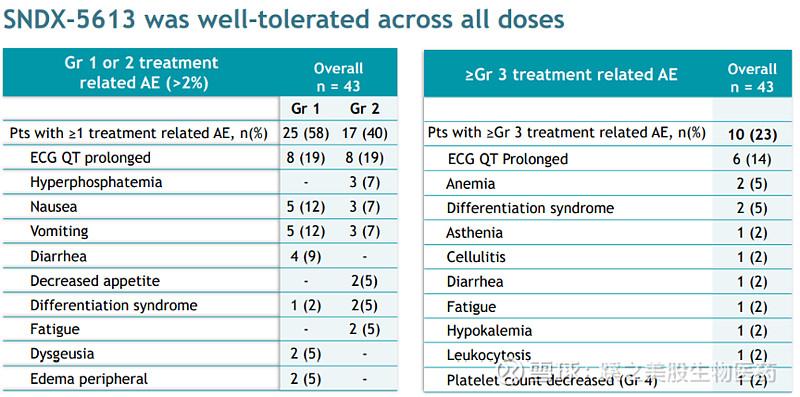
所有参加试验的43名患者对SNDX-5613基本耐受良好,在经过大量预先治疗的患者中未观察到因治疗相关不良事件导致的停药。发生率>5%的3级或以上不良事件为QT间期延长、贫血和分化综合征。数据截止时,22名患者接受候选RP2D治疗,其中9%(2/9)患者出现3级QT延长。
关于SNDX-5613
SNDX-5613是Menin-MLL相互结合作用的高效、高选择性小分子抑制剂,正开发用于治疗混合谱系白血病基因重排(MLLr)急性白血病(表现为急性淋巴细胞白血病,ALL;和急性髓性白血病,AML)以及NPM1c突变型AML。在MLLr急性白血病的临床前模型中,SNDX-5613表现出剂量依赖性的肿瘤生长抑制,提示显著的生存改善。SNDX-5613在多种NPM1c突变型AML临床前模型中也显示出有力的治疗获益,而该类型为成人AML中最为常见的遗传异常。SNDX-5613目前正在该公司的AUGMENT-101 1/2期开放标签临床研究中进行评估,以用于治疗复发/难治性急性白血病。该药目前已被FDA批准为治疗AML患者的孤儿药。
关于混合谱系白血病基因重排(MLLr)急性白血病
MLL基因的重排导致已知预后不良的混合谱系白血病基因重排(MLLr)急性白血病,在过去五年中成年患者存活率不到25%。MLLr产生融合蛋白,与Menin蛋白相互结合作用并驱动白血病肿瘤生长。数据表明破坏menin-MLLr相互作用,能阻止MLLr白血病细胞的生长。通过目前可用的细胞遗传学或分子诊断技术,可对该病进行常规诊断。MLLr白血病发生于约80%的婴儿急性白血病和高达10%的所有类型急性白血病中。目前尚无批准针对MLLr白血病的疗法。
关于NPM1c突变的急性髓细胞性白血病(AML)
NPM1c突变型AML的特征是驱动白血病表型的NPM1c基因中的点突变,是普通成人AML细胞遗传学的最常见类型,约占30%。该亚型五年总生存率约为50%。与MLLr急性白血病相似,其高度依赖于特定基因的表达,而这些基因受menin-MLL相互作用抑制剂的负向调控。目前尚无批准针对NPM1c突变型AML的疗法。
蹊之美股生物医药 / CaesarBiotech
追踪和剖析全球最前沿生物科技公司,寻找低估值/革命性的生物科技产品或技术平台,深入挖掘其投资价值。
联系方式:CaesarBiotech@aliyun.com
本文首发:蹊之美股生物医药
版权声明
本文原创,如需转载请联系授权