点击上方的 行舟Drug ▲ 添加关注



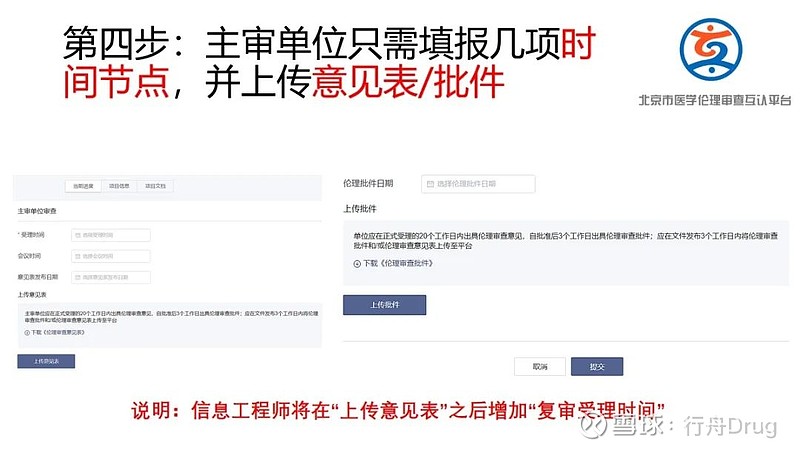
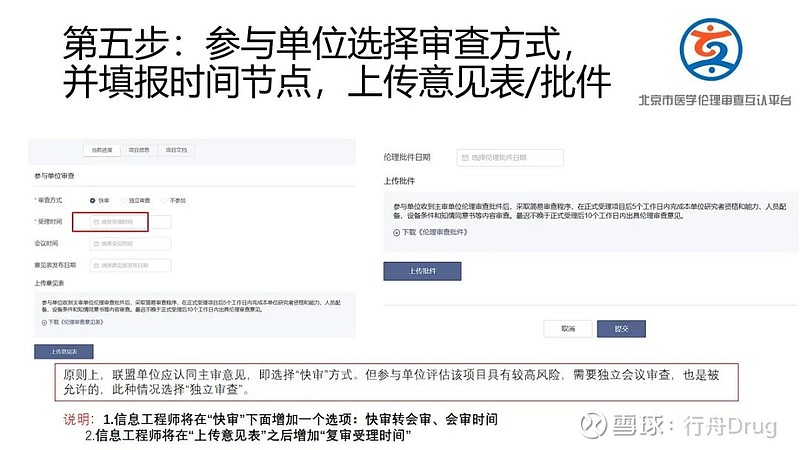
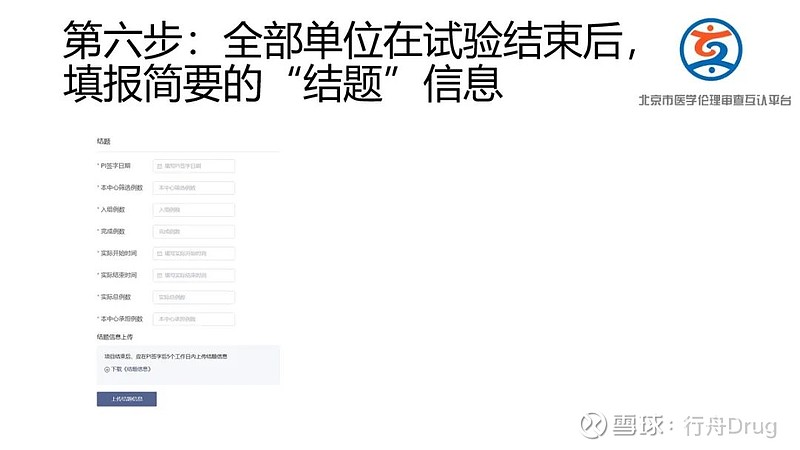



联盟互认卫健委平台信息录入方法
符合以下条件的项目进行互认项目信息录入
(1) 15家医院内既有组长单位,又有参与单位(至少1家)
(2) 组长单位即将或已通过伦理审查;
(3) 参与单位还未伦理审查。
信息录入方法:
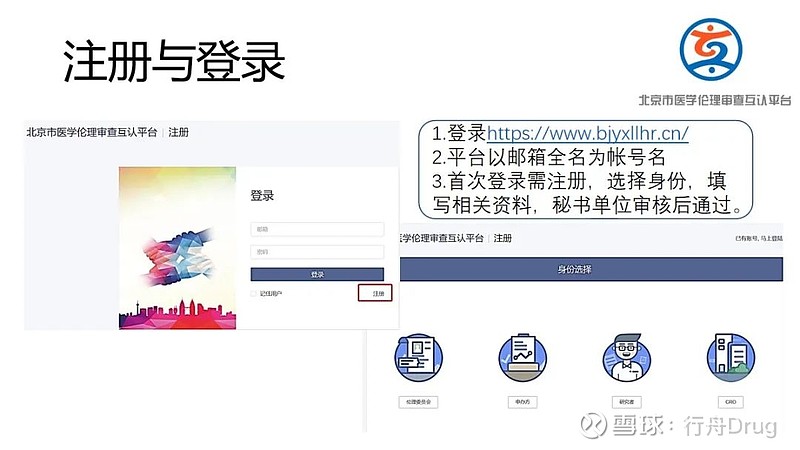
(1)请组长单位将“北京市医学伦理审查互认平台”网址(网页链接) 告知申办方/CRO/主要研究者;
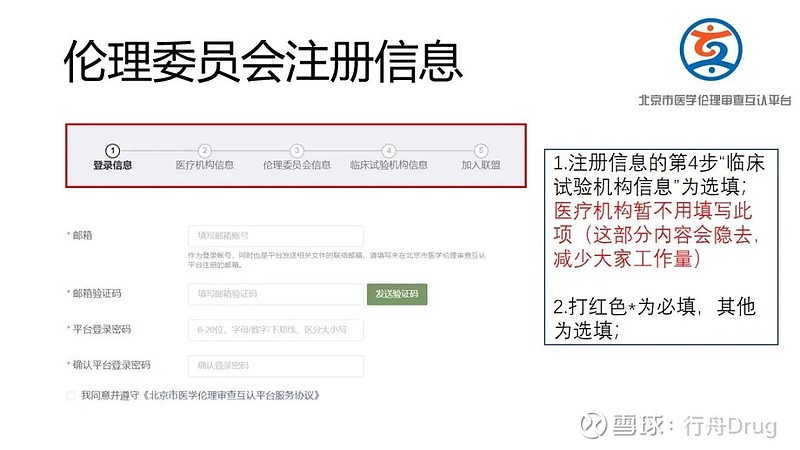
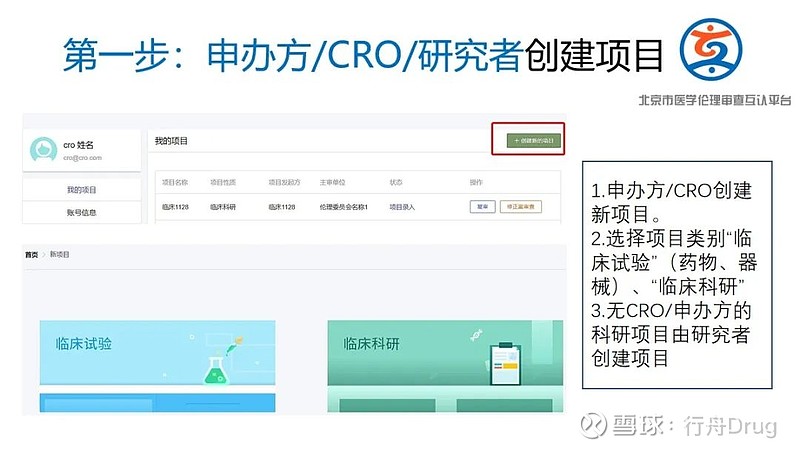
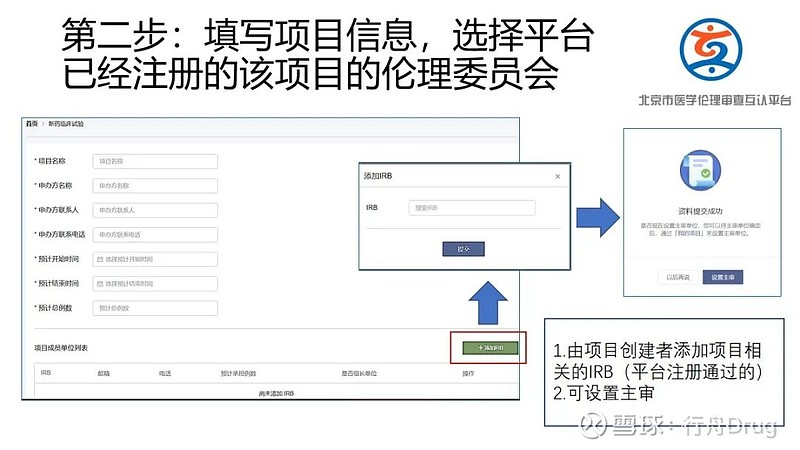
(2)请申办方/CRO(临床科研项目为研究者)在平台进行注册并进行信息填报,发起互认申请;
(3)如有疑问,组长单位伦理办公室/申办者/CRO(临床科研项目为组长单位伦理办公室)可联系宣武医院伦理办李晓玲 83198856
送审文件清单
(文件格式,均需PDF扫描件,不接受任何.jpg等照片格式的文件)适用于以下所有文件
伦理审查申请文件清单
一、初始审查文件
1.药物临床试验初次申请审查提交文件
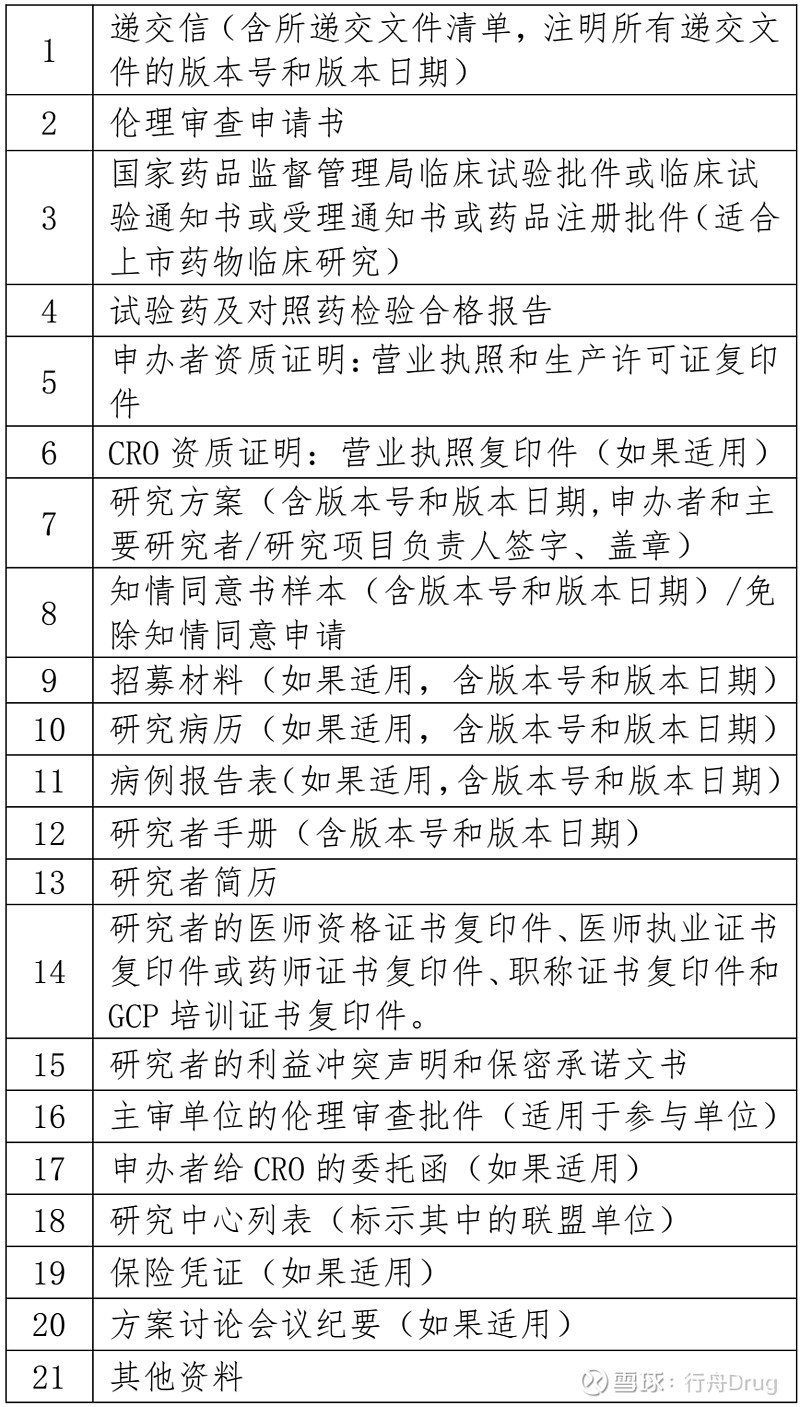
2.医疗器械临床试验初次申请审查提交文件
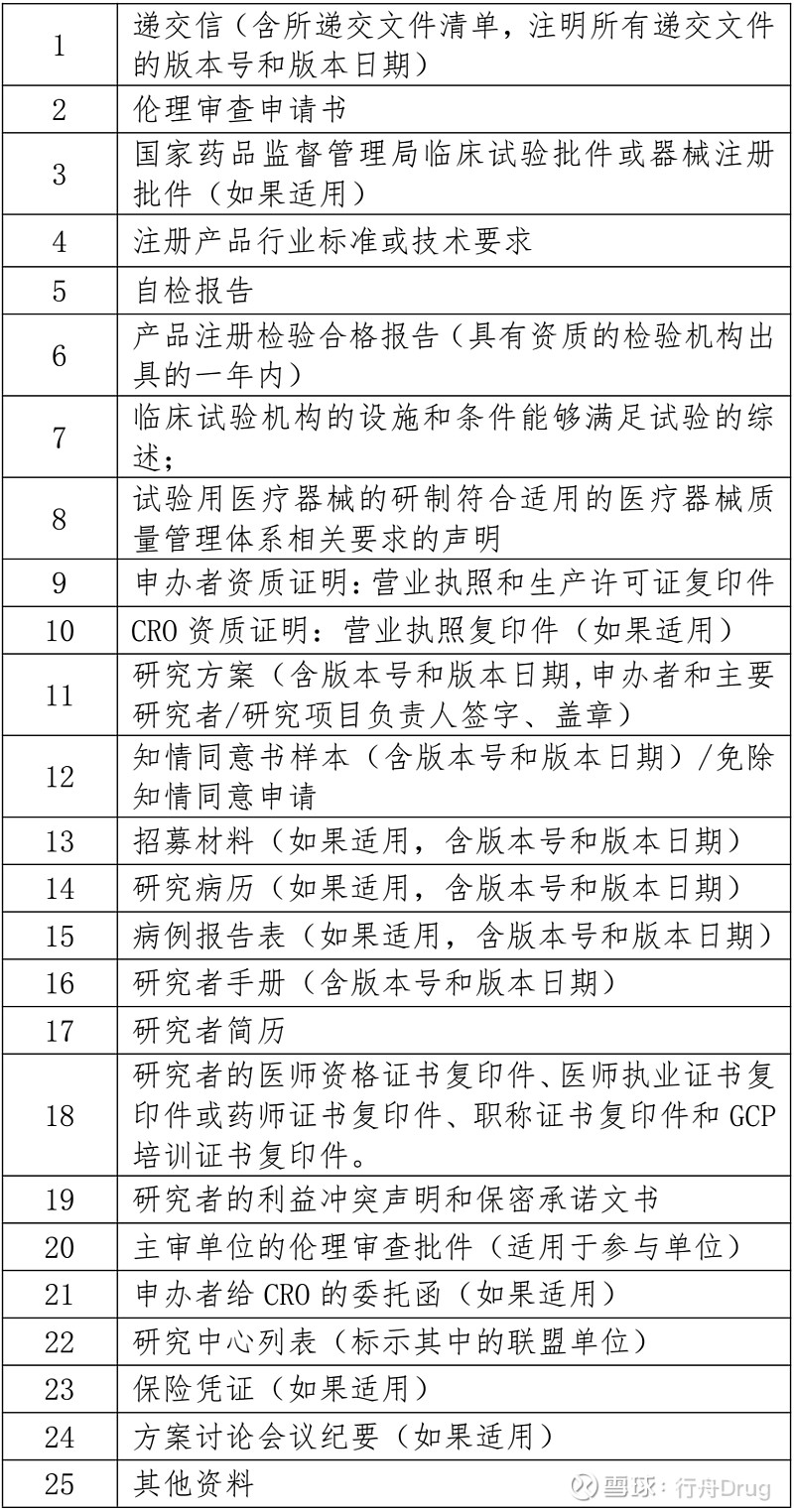
3.临床科研项目初次申请审查需提交文件
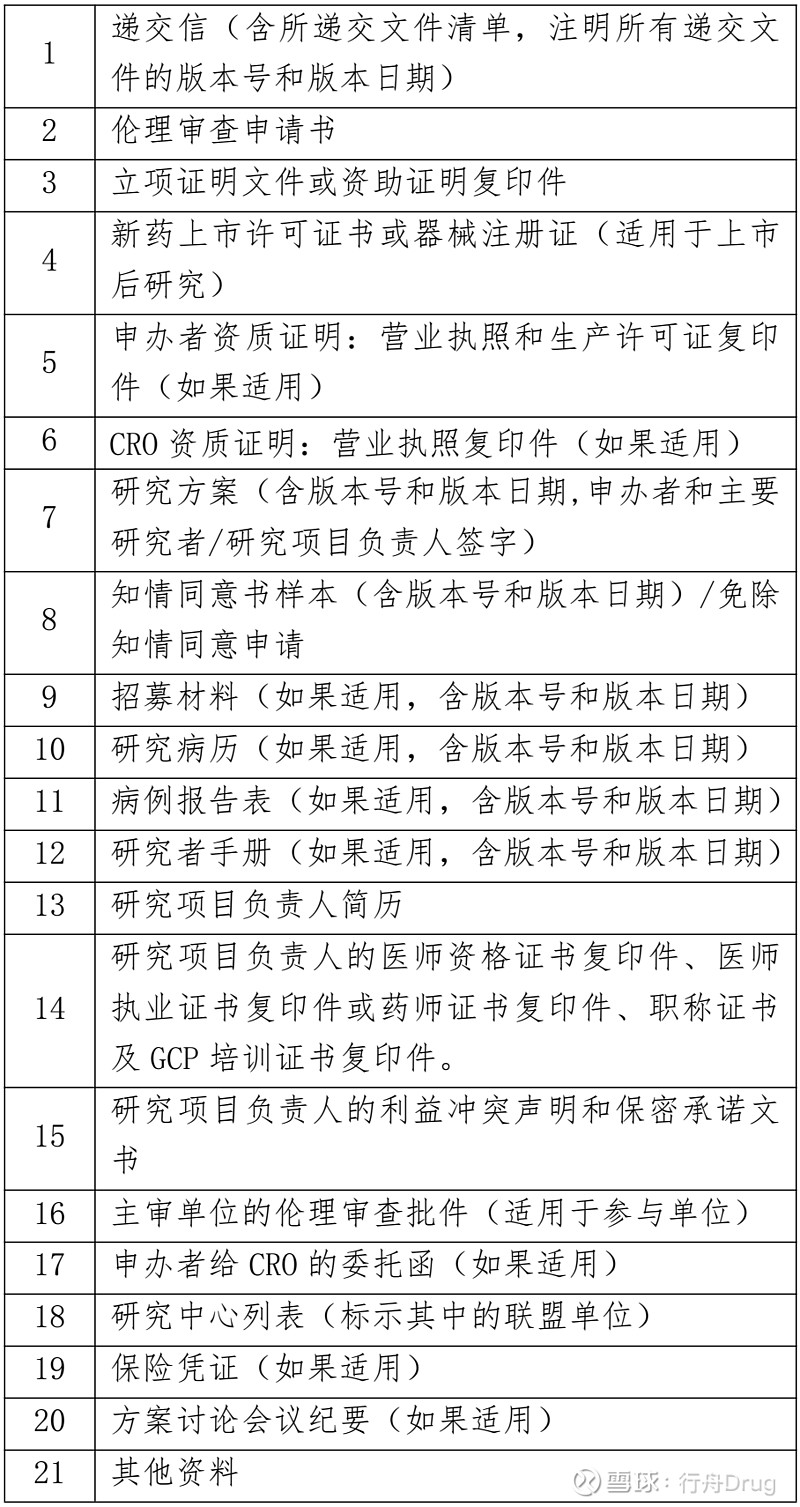
二、复审文件

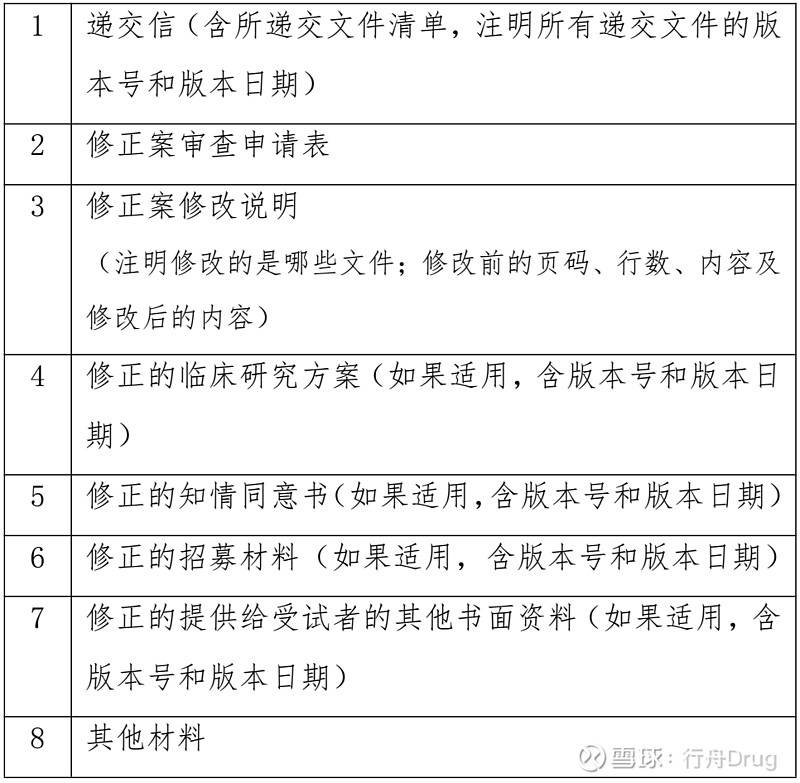
三、修正案文件
文章信息源于公众号临床研究大汇,登载该文章目的为更广泛的传递行业信息,不代表赞同其观点或对其真实性负责。文章版权归原作者及原出处所有,文章内容仅供参考。本网拥有对此声明的最终解释权,若无意侵犯版权,请联系小编删除。
学如逆水行舟,不进则退;
心似平原走马,易放难收。

行舟Drug
每日更新 欢迎订阅+
医药大数据|行业动态|政策解读