当地时间5月31日至6月4日,2024年美国临床肿瘤学会(ASCO)年会于芝加哥盛大召开。中国生物制药(1177.HK)下属企业正大天晴近期上市的1类创新生物药贝莫苏拜单抗在会上公布了多项研究成果,涵盖消化系统肿瘤和妇科肿瘤等领域。贝莫苏拜单抗是一款全新序列的创新人源化抗PD-L1单克隆抗体,于2024年5月刚刚获批上市,首个获批的适应症为联合盐酸安罗替尼胶囊、卡铂和依托泊苷用于广泛期小细胞肺癌(ES-SCLC)患者的一线治疗。
子宫内膜癌是最常见的妇科恶性肿瘤之一,其发病率在世界范围内呈上升趋势[1-4]。大多数子宫内膜癌患者诊断时处于早期,整体预后较好,5年生存率可达到95%。一旦出现局部扩散或远处转移,5年生存率明显降低,发生远处转移子宫内膜癌患者的5年生存率仅为17%[5-7]。
目前,晚期、转移性或复发性子宫内膜癌的一线系统治疗方案主要是紫杉醇联合铂类化疗,对于铂类化疗失败后的晚期子宫内膜癌,尚无明确的标准治疗方案,晚期子宫内膜癌二线及其以后的治疗有着严重未满足的需求。
TQB2450-II-08:贝莫苏拜单抗联合安罗替尼治疗晚期复发性或转移性子宫内膜癌:一项多中心、开放标签II期临床研究

研究结果显示,客观缓解率(ORR)为31.76%,中位无进展生存期(mPFS)为8.38个月,中位总生存期(mOS)为21.72个月(表1和图1)[8]。贝莫苏拜单抗联合安罗替尼或贝莫苏拜单抗单药治疗复发性或转移性子宫内膜癌显示出有希望的抗肿瘤活性。
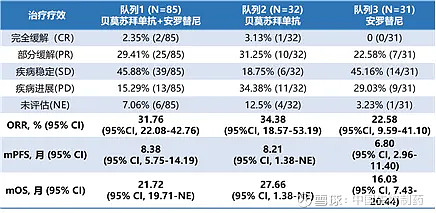
表1. 治疗疗效总结(N=148)
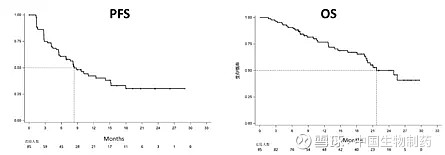
图1. 队列1第二阶段患者PFS和OS(N=85)
2022年4月,贝莫苏拜单抗联合盐酸安罗替尼胶囊治疗复发性或转移性子宫内膜癌已被中国国家药品监督管理局药品审评中心(CDE)纳入突破性治疗品种,并于2024年1月被纳入CDE优先审评审批程序。
目前,贝莫苏拜单抗联合盐酸安罗替尼胶囊正在开展多项临床III期试验,包括一线肾细胞癌、一线非小细胞肺癌、非小细胞肺癌放化疗后维持等。其中,贝莫苏拜单抗联合安罗替尼用于晚期肾细胞癌一线治疗III期研究取得阳性结果,并将于近期向CDE递交上市申请。这是国内首个双国产创新药组合用于晚期肾癌免疫治疗关键III期研究,有望为广大晚期肾癌患者带来新的治疗希望,解决尚未被满足的临床需求。
未来,正大天晴将持续推进贝莫苏拜单抗和盐酸安罗替尼胶囊的开发,为更多患者带来新的治疗方案。随着公司在创新药研发中的不断投入,创新产品取得不断突破,创新管线已进入收获期。
参考文献:
1. Bray F, et al. CA Cancer J Clin. 2024 May-Jun;74(3):229-263.
2. Rahib L, et al. Cancer Res. 2014 Jun 1;74(11):2913-21.
3. Xia C, et al. Chin Med J (Engl). 2022 Feb 9;135(5):584-590.
4. Han B, et al. J Natl Cancer Cent. 2024;4(1):47-53.
5. Lu KH, Broaddus RR. N Engl J Med. 2020 Nov 19;383(21):2053-2064.
6. Brooks RA, et al. CA Cancer J Clin. 2019 Jul;69(4):258-279.
7. Colombo N, et al. Ann Oncol. 2016 Jan;27(1):16-41.
8. Xiaohua Wu, Benmelstobart (TQB2450) combined with anlotinib hydrochloride capsule in the treatment of advanced, recurrent, or metastatic endometrial cancer: A multicohort, open label, multicenter, phase II clinical trial (TQB2450-II-08).Asco 2024.
声明:
1. 本新闻稿旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参阅,非广告用途。
2. 本公司不对任何药品和/或适应症作推荐。
3. 本新闻稿中涉及的信息仅供参考,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。若您想了解具体疾病诊疗信息,请遵从医生或其他医疗卫生专业人士的意见或指导。
前瞻性声明:本新闻稿中包含若干前瞻性陈述,包括有关【贝莫苏拜单抗注射液、盐酸安罗替尼胶囊】的临床开发计划、临床获益与优势的预期、商业化展望、患者临床获益可能性,以及潜在商业机会等声明。“预期”、“相信”、“继续”、“可能”、“估计”、“期望”、“有望”、“打算”、“计划”、“潜在”、“预测”、“预计”、“应该”、“将”、“拟”、“会”和类似表达旨在识别前瞻性陈述,但并非所有前瞻性陈述都包含这些识别词。这些前瞻性陈述为公司基于当前所掌握的数据和信息所做的预测或期望,可能因受到政策、研发、市场及监管等不确定因素或风险的影响,而导致实际结果与前瞻性陈述有重大差异。请现有或潜在的投资者审慎考虑可能存在的风险,并不可完全依赖本新闻稿中的前瞻性陈述,该等陈述包含信息仅及于本新闻稿发布当日。除非法律要求,本公司无义务因新信息、未来事件或其他情况而对本新闻稿中任何前瞻性陈述进行更新或修改。