当地时间5月31日至6月4日,2024年ASCO年会在美国芝加哥盛大召开。这是国际肿瘤学领域规模最大、学术水平最高、最具权威性与影响力的年度盛会之一。会上,中国生物制药(1177.HK)1类创新药安罗替尼共有44项研究成果公布,涵盖肺癌、骨与软组织肉瘤、头颈部肿瘤、消化系统肿瘤、妇科肿瘤、乳腺癌、泌尿系统肿瘤、皮肤癌等10多个癌种,展现了中国创新的多元潜力。
中国原研创新 闪耀国际学术盛会
01. 安罗替尼联合贝莫苏拜单抗治疗腺泡状软组织肉瘤的II期研究
该项研究在本次ASCO大会上以快速口头报告的形式展示了研究成果,公布了腺泡软组织肉瘤一线队列的数据。
研究结果显示,客观缓解率(ORR)达79.3%(n=28),包括3例完全缓解(CR)和20例部分缓解(PR)(图1),主要不良事件为1级和2级[1],为肉瘤抗血管生成药物联合免疫治疗再添新的证据。
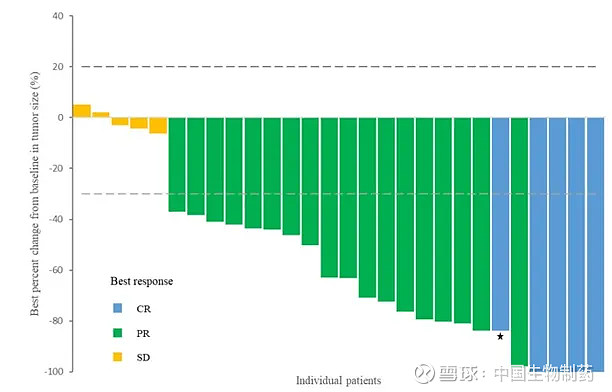
图1. 靶病灶最佳疗效(安罗替尼联合贝莫苏拜单抗治疗肉瘤的研究数据)
02.安罗替尼在免疫经治实体瘤中的治疗进展
免疫检查点抑制剂已成为多种恶性肿瘤的标准治疗方案,如非小细胞肺癌、消化道肿瘤等[2-4],但免疫经治者的治疗选择尚无标准方案,且无充分循证证据。安罗替尼具有全面调控肿瘤微环境重编程的作用[5-14],可能为免疫经治人群带来临床获益。
本次ASCO公布了一项安罗替尼在免疫治疗失败的食管鳞癌患者中的研究数据。该研究回顾分析了110例受试者,结果显示,接受安罗替尼联合PD-1抑制剂治疗仍能获得5.6个月的中位无进展生存期(mPFS),11.1个月的中位总生存期(OS),疾病控制率(DCR)为69.1%[15]。
另外一项非小细胞肺癌的研究结果显示,在免疫经治的患者中(n=71),安罗替尼联合多西他赛与单用多西他赛相比,PFS显著延长至两倍以上(图2),ORR和DCR均提升至近两倍[16]。从研究结果看,安罗替尼联合其他系统治疗有望为免疫治疗失败的晚期恶性肿瘤患者提供一种更优的治疗选择。
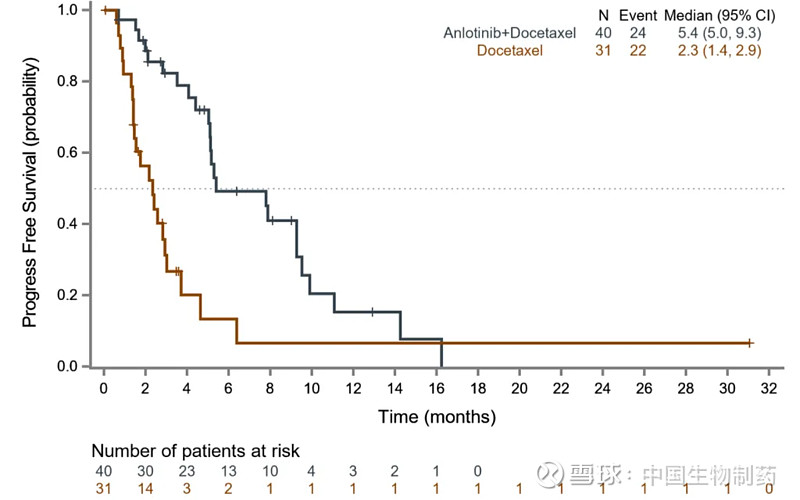
图2. 患者无进展生存期曲线(安罗替尼联合多西他赛对比多西他赛治疗免疫经治非小细胞肺癌的研究数据)
03. 贝莫苏拜单抗联合安罗替尼治疗晚期复发性或转移性子宫内膜癌
本次ASCO大会公布了安罗替尼在晚期复发性或转移性子宫内膜癌的关键注册研究数据,安罗替尼联合贝莫苏拜单抗在non-MSI-H/dMMR子宫内膜癌治疗中取得显著成果,其客观反应率(ORR)达31.76%,中位无进展生存期(mPFS)达8.38个月[17]。该方案已经成为我国子宫内膜癌non-MSI-H/dMMR人群中首个获得优先审评审批的靶免方案。
展现多元潜力 服务临床需求
作为中国生物制药肿瘤领域拳头产品,安罗替尼自2018年上市以来,已先后获批6大适应症,服务患者超90万人,显示了广泛的应用前景。此外,安罗替尼还有多个项目处于在研阶段,布局广泛,以期满足更多领域临床治疗需求,为患者提供治疗新选择。
安罗替尼已获批用于多种恶性肿瘤的治疗:单药已获批三线及以上治疗晚期非小细胞肺癌、二线及以上治疗软组织肉瘤、三线及以上治疗小细胞肺癌、甲状腺髓样癌和放射性碘难治性分化型甲状腺癌的适应症。在联合治疗方面,今年4月30日,安罗替尼联合贝莫苏拜单抗、卡铂和依托泊苷更是获批用于广泛期小细胞肺癌的一线治疗。
安罗替尼在研适应症布局广泛:联合贝莫苏拜单抗二线及以上治疗non-MSI-H/dMMR子宫内膜癌的适应症已获得优先审评审批;联合贝莫苏拜单抗在肾细胞癌一线治疗、联合派安普利单抗在肝细胞癌一线的适应症即将申报上市;此外,联合免疫或化疗的、涵盖非小细胞肺癌局晚期、非小细胞肺癌一线(PD-L1阳性)、非小细胞肺癌(非鳞)一线、肉瘤一线、结直肠一线(RAS/BRAF野生型)、肝细胞癌辅助、非小细胞肺癌(鳞癌)一线、非小细胞肺癌围术期的关键注册III期临床研究正在进行中。
关于安罗替尼
安罗替尼是一种新型的多靶点(VEGFR 1/2/3、PDGFR-α/β、FGFR1-4、c-Kit) 酪氨酸激酶抑制剂[7]。安罗替尼不仅具有直接抑制肿瘤血管新生的作用,还能全面调控肿瘤微环境重编程[5-14],在促进其他药物递送至肿瘤组织、调节免疫微环境方面具有优势,这种全面而精准的肿瘤微环境重编程作用使得安罗替尼在联合化疗、免疫或局部治疗中具有协同增效的作用[2,8,11,18]。
更重要的是,在多种恶性肿瘤的治疗中,安罗替尼联合治疗有望提升疗效、延长生存、提高患者生存质量。这为未来安罗替尼联合标准系统治疗作为更优选的治疗方案提供了可靠的循证基础。随着安罗替尼在不同晚期肿瘤治疗中的优异表现,安罗替尼将为更多的恶性肿瘤患者带来临床获益,成为抗击癌症的有力武器,我们对此充满信心。
参考文献:
1. Jiayong Liu, et al. J Clin Oncol 42, 2024 (suppl 16; abstr 11515)
2. 中国临床肿瘤学会指南工作委员会,《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南(2024版)》
3. 中国临床肿瘤学会指南工作委员会,《中国临床肿瘤学会(CSCO)小细胞肺癌诊疗指南(2024版)》
4. 中国临床肿瘤学会指南工作委员会,《中国临床肿瘤学会(CSCO)食管癌诊疗指南(2024版)》
5. XD Han, LF Zheng, et al. J Pharma Analy, doi.org/10.1016/ j.jpha.2024.100984.
6. Xie C, et al. Cancer Sci. 2018 Apr;109(4):1207-1219.
7. Lin B, et al. Gene. 2018 May 15:654:77-86
8. Su Y, et al. Clin Cancer Res. 2022 Feb 15;28(4):793-809.
9. Han X, et al. J Pharma Analy, doi.org/10.1016/ j.jpha.2024.100984
10. Liang L, et al. J Exp Clin Cancer Res. 2019 Feb 12;38(1):71.
11. Song F, et al. Cell Death Dis. 2020 Jul 24;11(7):573.
12. Ji Y, et al. Molecules. 2022 Dec 14;27(24):8873.
13. Zhu Y, et al. J Clin Med. 2022 Dec 25;12(1):162.
14. Fang F, et al. Oncol Lett. 2022 Feb;23(2):46.
15. Jing Huang, et al. J Clin Oncol 42, 2024 (suppl 16; abstr e16006)
16. Lin Wu, et al. J Clin Oncol 42, 2024 (suppl 16; abstr 8062)
17. Wu Xiaohua, et al. J Clin Oncol 42, 2024 (suppl 16; abstr 5593)
18. Li, et al. Exp Cell Res. 2022 Aug 1;417(1):113197.
声明:
1. 本新闻稿旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参阅,非广告用途。
2. 本公司不对任何药品和/或适应症作推荐。
3. 本新闻稿中涉及的信息仅供参考,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。若您想了解具体疾病诊疗信息,请遵从医生或其他医疗卫生专业人士的意见或指导。
前瞻性声明:本新闻稿中包含若干前瞻性陈述,包括有关【安罗替尼、贝莫苏拜单抗、派安普利单抗】的临床开发计划、临床获益与优势的预期、商业化展望、患者临床获益可能性,以及潜在商业机会等声明。“预期”、“相信”、“继续”、“可能”、“估计”、“期望”、“有望”、“打算”、“计划”、“潜在”、“预测”、“预计”、“应该”、“将”、“拟”、“会”和类似表达旨在识别前瞻性陈述,但并非所有前瞻性陈述都包含这些识别词。这些前瞻性陈述为公司基于当前所掌握的数据和信息所做的预测或期望,可能因受到政策、研发、市场及监管等不确定因素或风险的影响,而导致实际结果与前瞻性陈述有重大差异。请现有或潜在的投资者审慎考虑可能存在的风险,并不可完全依赖本新闻稿中的前瞻性陈述,该等陈述包含信息仅及于本新闻稿发布当日。除非法律要求,本公司无义务因新信息、未来事件或其他情况而对本新闻稿中任何前瞻性陈述进行更新或修改。