文章来源:“凯莱英药闻”微信公众号
4月7日,吉利德宣布旗下靶向TROP-2的抗体药物偶联物(ADC)Trodelvy(sacituzumab govitecan)获FDA完全批准,治疗患有无法切除的局部晚期或转移性三阴性乳腺癌(TNBC)的成人患者。
Trodelvy是首个获批上市的靶向TROP-2的ADC,于2020年4月获FDA加速批准上市,吉利德在2020年10月23日完成对Trodelvy开发企业Immunomedics的收购,在收购后的两个多月里Trodelvy销售额达到4900万美元,而吉利德收购Immunomedics的价格也相当不菲——210亿美金。
本次FDA完全批准Trodelvy基于一项全球多中心III期临床试验——ASCENT(n =482),在该项试验中,Trodelvy将疾病进展和死亡风险降低57%,中位无进展生存期由化疗的1.7个月提升至4.8个月(HR:0.43,95% CI: 0.35-0.54,p<0.0001);死亡风险降低49%,总生存期由6.9个月提升至11.8个月 (HR: 0.51,95% CI: 0.41-0.62,p<0.0001)。
安全性方面,与先前数据一致。与单药化疗相比,Trodelvy最常见3级以上不良反应是中性粒细胞减少症(52% vs. 34%),腹泻(11% vs.1%),白细胞减少症(11% vs. 6%)和贫血(9% vs. 6%)。Trodelvy组患者因不良反应导致治疗中断的比例为5%。
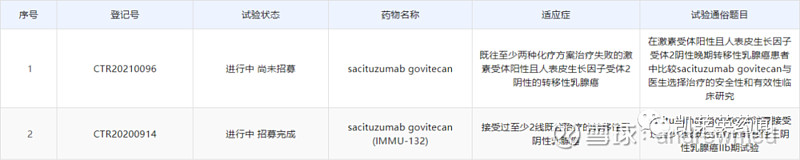
Trodelvy中国权益归属云顶新耀,目前已开展转移性三阴性乳腺癌IIb期临床试验,及HER2阴性乳腺癌III期临床试验。
Trodelvy由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。
Trodelvy结构图示

第一三共开发了基于创新Linker-drug技术成果的TROP2靶向ADC药物Dato-DXd,结构优化后的DXd活性比SN-38强10倍左右。DXd被切掉后可以穿透细胞膜进入旁边癌细胞,发挥bystander effect(旁观者效应)。同时,DXd的血浆半衰期更短,保证了毒性更小。
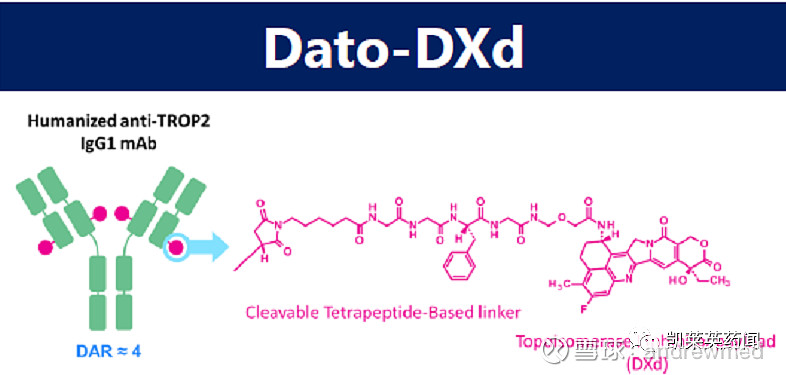
Dato-DXd目前已开展治疗非小细胞肺癌的III期临床研究,另外1项II期临床和4项I期临床正在进展,阿斯利康2020年7月耗资60亿美元获得Dato-DXd的全球开发权益,未来有望成为Trodelvy劲敌。
版权说明:本文来自凯莱英,感谢关注、转发。欢迎媒体/机构转载,转载请注明来自“凯莱英药闻”。