
$华润三九(SZ000999)$ $药明康德(SH603259)$ #CDMO# #抗生素#
【华义文随笔】
5月31日,CDE官网新公示一条拟优先审评信息,来自住友制药的醋酸来法莫林注射用浓溶液,理由也用到了2024年49号文。这是新政实施以来的第二例,第一例也是上周,来自华润九新的注射用头孢比罗酯钠。有意思的是,这两例都是抗生素产品。头孢比罗酯钠是第五代头孢。而来法莫林(Lefamulin)是截短侧耳素类抗生素,是一种不易产生耐药及交叉耐药的新型抗感染药物。
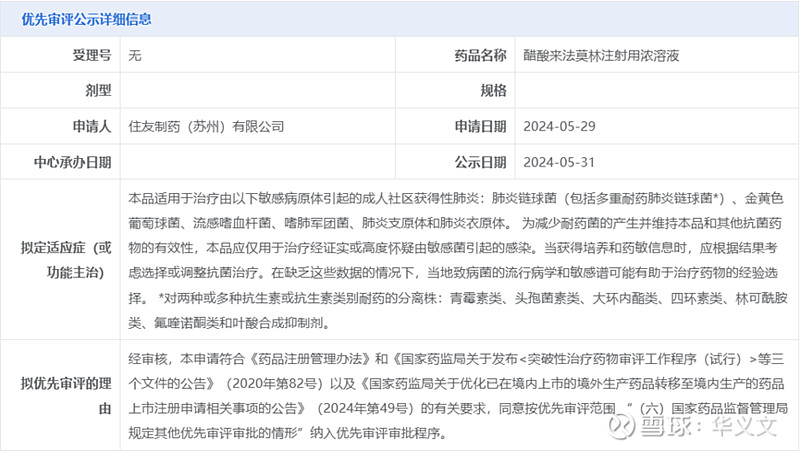
由于住友是日本药企,第一反应是住友将来法莫林的生产线从日本复制到中国来。不过查询进口药品注册信息却并不是这样。原来醋酸来法莫林注射用浓溶液的境外持有人是Nabriva,而且与住友并无股权关系。
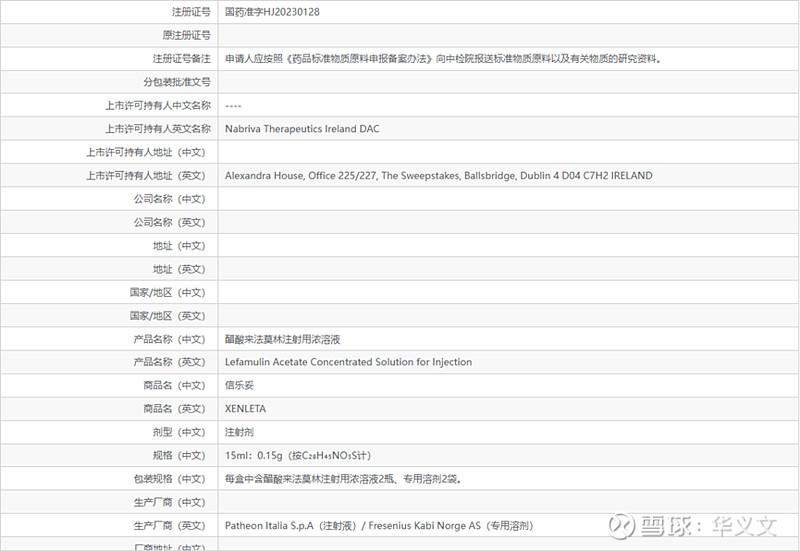
事实上,该产品也不是住友直接从Nabriva引进的。中间发生的事情,就不得不提到大名鼎鼎的Roivant公司。
2017年,Roivant联合中信产业基金在中国孵化了一家公司,名叫Sinovant也就是上海仑胜。2018年,仑胜从Nabriva引进了来法莫林片剂和注射液两个剂型的中国权益。2019年3月提交IND申请并获批,年末启动关键3期临床试验。之后的时间就是在新冠疫情的笼罩之下艰难开展临床试验。
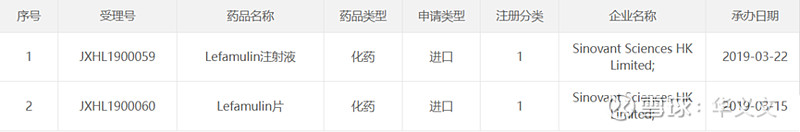
最终在2021年11月按进口药品提交上市申请。此刻,申请人已经发生了变化。
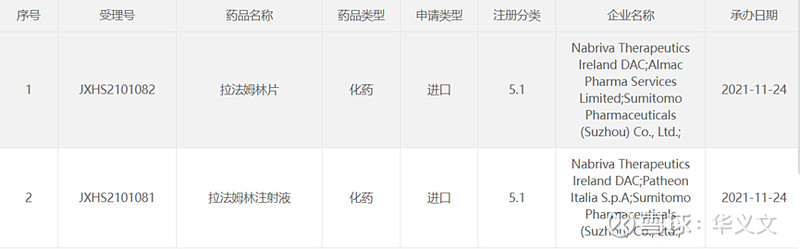
稍早时候也就是在临床试验取得积极初步结果之时,即2021年5月,在住友和Roivant的运作下,仑胜的四个研发项目一并转给了住友,其中就包括来法莫林。由此,住友拿到了来法莫林的中国权益,并接手了后续的临床试验和上市申请工作。
最终2023年11月,片剂和注射液双双获批上市。
在药物研发“得道”之时,公司却“升天”了。上海仑胜在完成历史使命之后,于2022年注销了。第二年,也就是2023年初,原研公司Nabriva 宣布董事会基于战略选择,决定有序停止公司运营,并遣散所有员工。事实上,Nabriva在2022年上半年的销售额是1720万美元。目前Nabriva还在正常经营。
这下,住友就紧张了。虽然住友拿到了中国权益,不过由于国内注册法规的限制,住友其实只是境内代理,而产品的上市持有人仍然是Nabriva。这就意味着,一旦Nabriva无法正常运营并维护进口注册证有效,那么住友手上拿到的注册证其实就是一张废纸。因此,将生产全部转移到中国,从而让住友从进口药品代理人转变为本地化生产药品的上市持有人,才是让住友踏踏实实完全拥有这个药品。
具体工作就是将原料药和制剂从境外生产转移到境内。第一步,原料药已经由合全常州工厂完成生产验证。从登记号可以判断2023年就提交了备案,可见这项工作是紧锣密鼓开展的。如果,Nabriva之前选用的原料药CDMO就是合全,那倒是十分便利的。
第二步便是制剂了。拟优先审评公示只有注射液并无片剂,而且住友尚未提交注射液的本地化生产上市申请。
那么,片剂是何策略?注射液又会选择在哪里生产呢?从住友中国网站上的上市品种来看,苏州工厂日常的生产任务是片剂和冻干粉针的分包装,是没有注射液生产线,而且本地化生产经验有限。因此,住友苏州工厂要么就新建一个注射液车间生产浓溶液以及专用溶媒,并招募有经验的工作人员。要么,就选择合适的CDMO,比如合全可能就是首选。
总之,对住友制药来说,境外生产转移到境内是迫在眉睫的事情,因此49号文的事实可以有效简化申请流程,来的真是时候。