
【华义文随笔】
美国当地时间5月28日,FDA批准Bkemv用于治疗两种罕见病PNH(阵发性睡眠性血红蛋白尿症)和aHUS(非典型溶血性尿毒症综合征)。

这款产品是依库珠单抗(Soliris)的生物类似药,由安进研发,代号ABP 959。这是FDA批准的第53个生物类似药,也是第13个可互换生物类似药。而对于上述两种罕见病而言,则是第一个可互换的生物类似药。
作为一款可互换生物类似药,Bkemv与Soliris高度相似,包括黑框警告在内相同的安全警告信息,预计会产生相同的不良反应,在临床应用上并没有差异。
依库珠单抗可与补体C5蛋白结合并抑制补体系统(人体免疫系统的一部分)的激活。这种结合可防止PNH和aHUS患者血流中红细胞破裂(血管内溶血)。
安进对补体抑制剂治疗罕见病情有独钟,在开发依库珠单抗生物类似药的同时,也在外部物色相关资产。
2022年10月,安进花费约37亿美元完成收购ChemoCentryx,从而获得后者的核心产品Tavneos(avacopan),这是一种小分子口服选择性补体5a受体(C5aR)抑制剂,于2021年10月获FDA批准,联用标准疗法作为严重活动性ANCA相关血管炎成年患者的辅助治疗,特别是肉芽肿伴多血管炎和显微镜下多血管炎(ANCA相关血管炎的两种主要形式)。
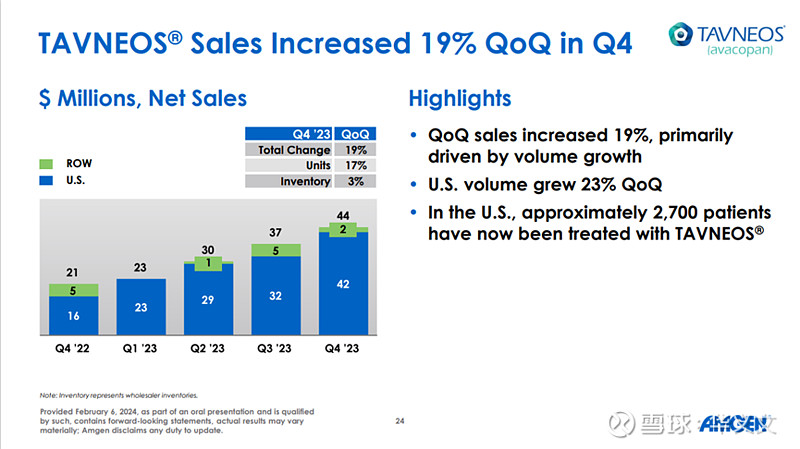
在被收购后的第一年,即2023年Tavneos就为安进贡献1.34亿美元收入。2024年第一季度直接冲到5100万美元,同比大涨122%。