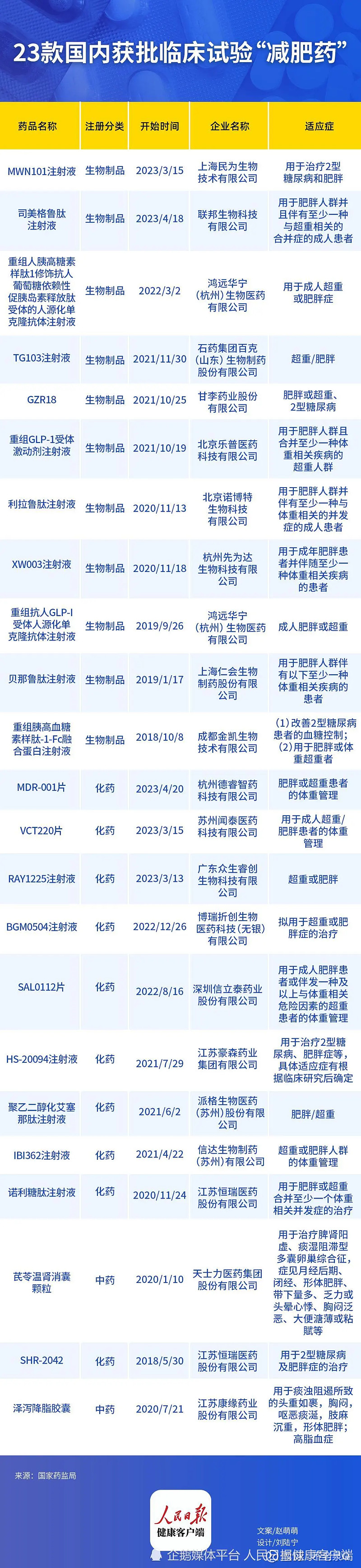
未来国内减重市场广阔,竞争也很激烈,因为销售价格不高,所以预计疗效更好的国产多靶点产品,未来会成为市场主流。下面是对国产GLP-1类减重药的梳理,欢迎大家补充指正。
单靶点国内:
华东医药:利拉鲁肽类似药减重适应症2023年6月获批上市,司美格鲁肽减重适应症临床Ⅰ期,TTP273片临床Ⅱ期,HDM1002自主研发口服药IND已受理;
仁会生物:贝那鲁肽减重适应症2023年7月获批;
恒瑞医药:诺利糖肽减重适应症处于临床Ⅲ期;口服小分子GLP-1R激动剂HRS-7535片,29天时的体重较基线平均下降4.38kg;
先为达生物:Ecnoglutide减重适应症处于临床Ⅲ期,II期结果显示每周一次皮下注射2.4mg的体重较基线降低14.7% ;
通化东宝:类似药索马鲁肽,利拉鲁肽注射液预计将于今年年内获批上市;口服小分子GLP-1受体激动剂(THDBH110胶囊)申报临床;
翰宇药业:利拉鲁肽注射液,上市申请均已获药监局受理。 SAL0112为公司自主研发的GLP-1R口服小分子偏向激动剂,2型糖尿病及减重适应症临床Ⅰ期。
联邦制药:司美格鲁肽类似药,获批临床。
双鹭药业、万邦医药:利拉鲁肽生物类似药“减重”适应症,Ⅲ期临床。
甘李药业:GZR18,Ⅱ期临床。
鸿运华宁:GMA105,格鲁塔珠单抗,Ⅱ期临床。
诺博特生物(爱美客):利拉鲁肽临床I期,与北京质肽生物医药合作司美格鲁肽类似药临床前。
乐普医疗:度拉糖肽,Ⅰ期临床试验。
信立泰:SAL0112,Ⅰ期临床试验,小分子GLP-1。
硕迪生物:GSBR-1290,GLP-1R,口服GSBR-1290正在日本和美国分别进行二期和一期临床。
先为达:XW003,GLP-1,III期临床。
惠升生物(四环医药):司美格鲁肽生物类似药,临床试验实验申请。
正大天晴:司美格鲁肽生物类似药,临床试验申请。
银诺医药:苏帕鲁肽,III期临床。
万邦生化:利拉鲁肽类似药,临床III期。
国产单靶点参与者众多,未来竞争激烈,价格比较低,估计是一篇红海。
多靶点国内:
信达生物:与礼来共同研发的玛仕度肽(GCGR/GLP-1R)减重适应症进入临床Ⅲ期;
恒瑞医药:HRS-9531,GIPR/GLP-1R,靶点同替尔泊肽,临床II期,5.4mg剂量36天减重8.0kg。
民为生物:MWN101, GCGR/GIPR/GLP-1R,减重适应症,临床申报,与乐普医疗有合作;
华东医药:GIPR/GLP-1R,SCO-094(日本引进)英国临床I期。HDM1005临床前。GLP-1R/GCGR/FGF21R三靶点DR10624(子公司道尔生物),新西兰临床Ⅰ期 。
通化东宝:GLP-1/GIP双受体激动剂(注射用THDBH120)申报临床。
联邦制药:UBT251,长效GLP-1/GIP/GCG三靶点受体激动剂,每周1次,临床试验获批。
豪森制药:GLP-1/GIPR双激动剂,HS-20094注射液,II期临床。
鸿运华宁:GMA106,GIPR/GLP-1融合蛋白,中生制药引进。
东阳光药:HEC88473,GLP-1/FGF21双重激动剂,I期临床。
博瑞医药:BGM0504,GLP-1/GIPR,II期临床。
和泽医药:HZ012,GLP-1R/GIPR,进入临床。
硕迪生物:GLP-1R/GIPR双靶点激动剂,进入临床。
目前国内共有9款GLP-1RA(原研药)上市,仅贝那鲁肽获批减重适应症, 司美格鲁肽减重适应症今年6月已提交NDA,替尔泊肽减重适应症今年8月提交上市申请。 另外司美格鲁肽化合物专利在国内将于2026年到期。