近一年多来,虽然全球生物医药领域的资本市场仍处在寒冬之中,但似乎技术迭代已经开始出现了暖意,尤其是今年以来好像逐渐改出了此前那种令人意兴阑珊的沉闷,而蹦出了越来越多令人兴奋的信号,以至于到了小小公众号这每天一篇的发文限额居然导致有点顾此失彼。
比如今天,一下子看到三条本身都足够积极的消息,而它们恰两两相关,放在一起则可能成为一部波澜壮阔的史诗的前奏。因为在笔者心目中近五年来全球医药领域最具备商业价值的突破中,AD和RNAi占据三席中之二(剩下一个是ADC);2023年7月18日AD遇上了RNAi,在未来的医药发展史上,这会不会是类似于1928年4月28日性质的一天呢?
1. AD:Eli Lilly
$礼来(LLY)$ 在JAMA发表了旗下AD药物Donanemab的三期临床完整数据(此前公布过的初步数据参见【药海听涛】阿尔茨海默药物的东方既白:礼来公布Donanemab三期临床积极结果)。

在这个代号TRAILBLAZER-ALZ2的三期临床试验中(NCT04437511),共入组了1,736例早期AD患者,按1:1分配到用药组和安慰剂组,每四周给药一次、共持续76周,淀粉样蛋白水平低于终止标准的患者可提前由用药组转入安慰剂。

从基线不难看出,Donanemab选择了比前辈Lecanemab等进展更深的患者,也就可能在真实世界中获得更大的用药范围。
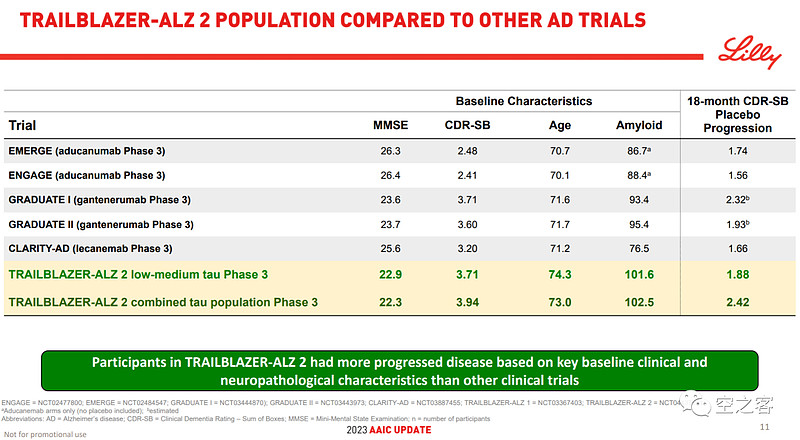
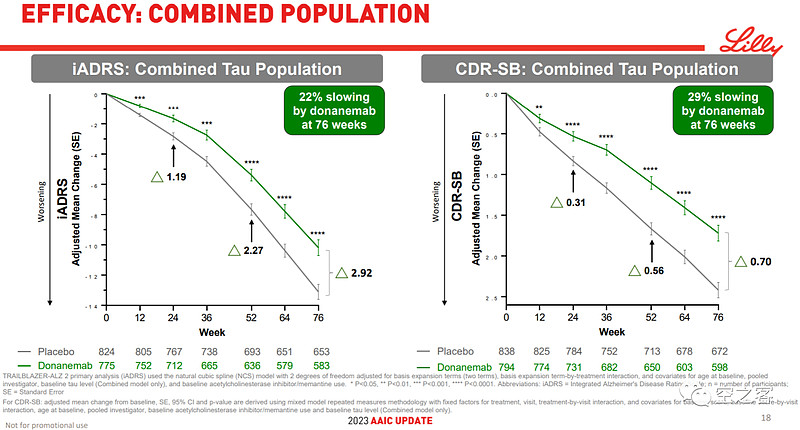
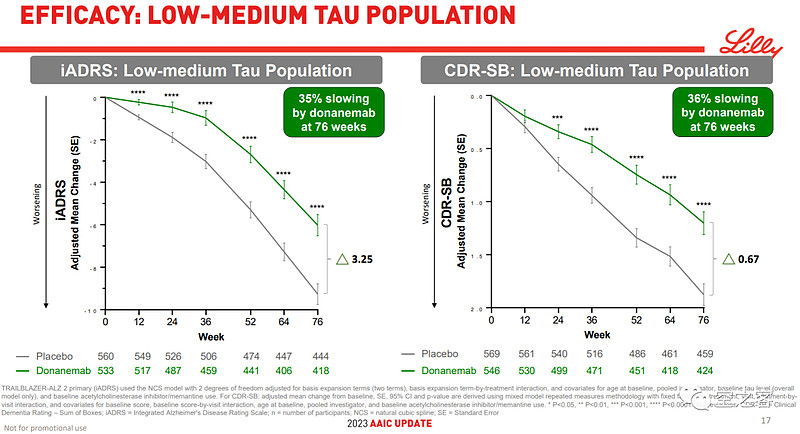
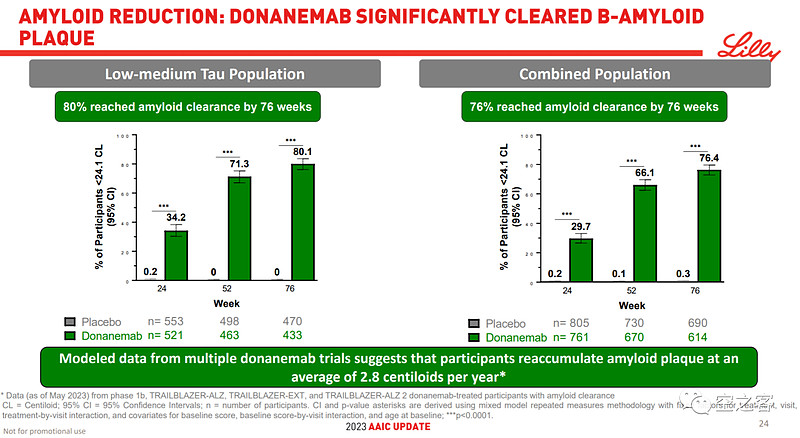
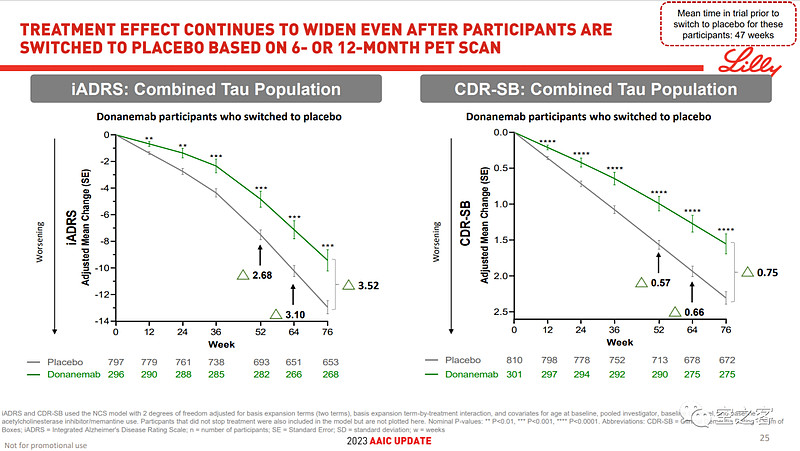
有效性方面,在给药76周后,Donanemab针对全人群能对iADRS衰退减缓22%、对CDR-SB衰退减缓29%、76%患者淀粉样蛋白清除,而针对tau蛋白低水平人群则能对iADRS衰退减缓35%、对CDR-SB衰退减缓36%、80%患者淀粉样蛋白清除;甚至对于提前转入安慰剂组的患者,后续有效性仍能维持或扩大。
安全性方面,ARIA仍是非常值得警惕的问题,ARIA-E和ARIA-H都明显偏高。
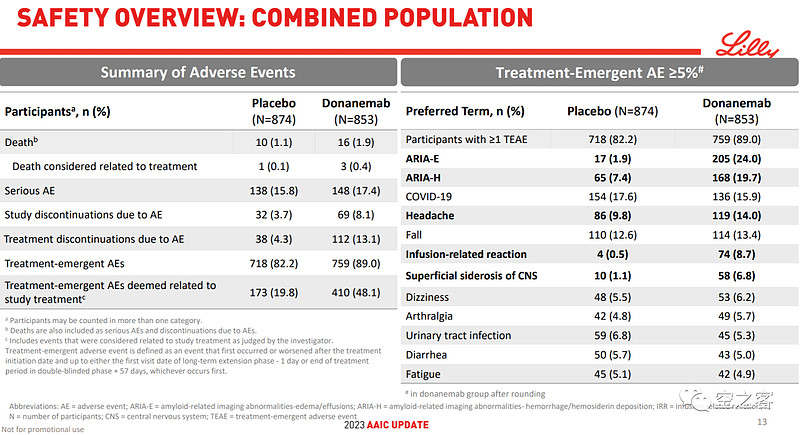
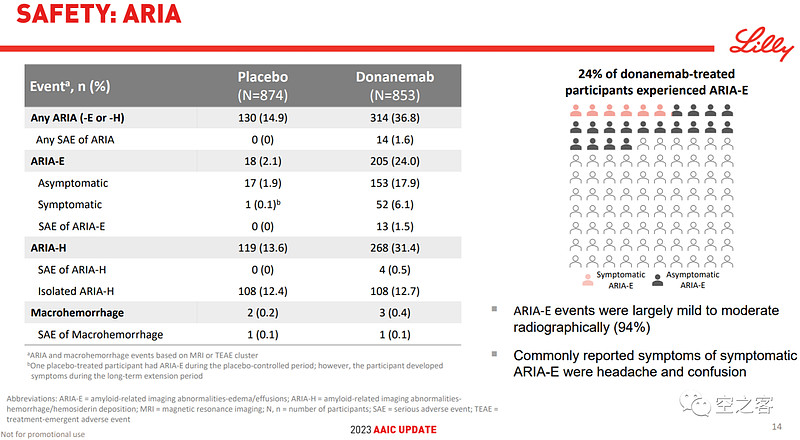

总体来说,Donanemab相比已经获批的Lecanemab而言,有效性明显上了一个新的台阶、但安全性存在隐忧,而Eli Lilly已向FDA递交BLA申请,无论如何都将成为AD治疗领域迈向下一篇章的重要尝试。
2. RNAi:Alnylam
$阿里拉姆制药(ALNY)$ 在AAIC年会上公布了ALN-APP的一期临床SAD试验结果,这是RNAi药物治疗CNS疾病的首个长时间积极临床结果。

ALN-APP应用了Alnylam开发的C16偶联技术,通过在RNAi上偶联不同的脂质分子、调整疏水性,实现向CNS组织的递送,最终靶向编码APP蛋白(APP突变被验证与早发性AD和淀粉样病变有关)的mRNA。
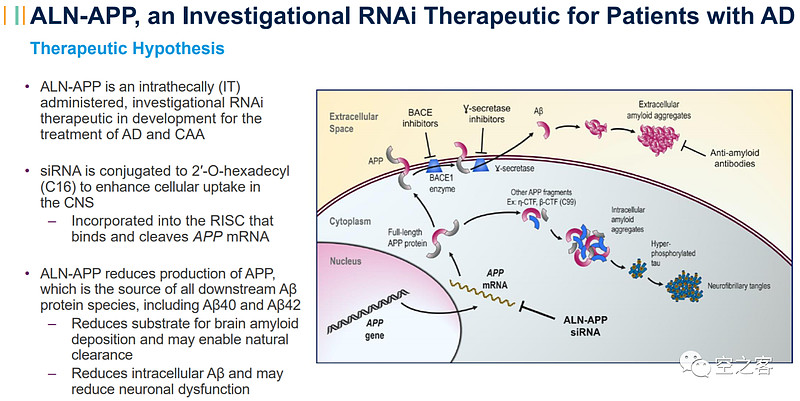

在一期临床的SAD部分,3个单次给药队列共入组了20例早发性AD患者,分别给药25/75/50mg,每个剂量按2:1或3:1的随机分配到用药组和安慰剂组。
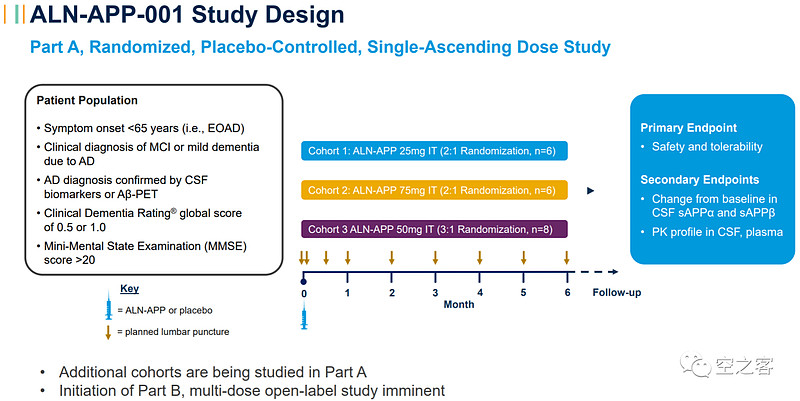
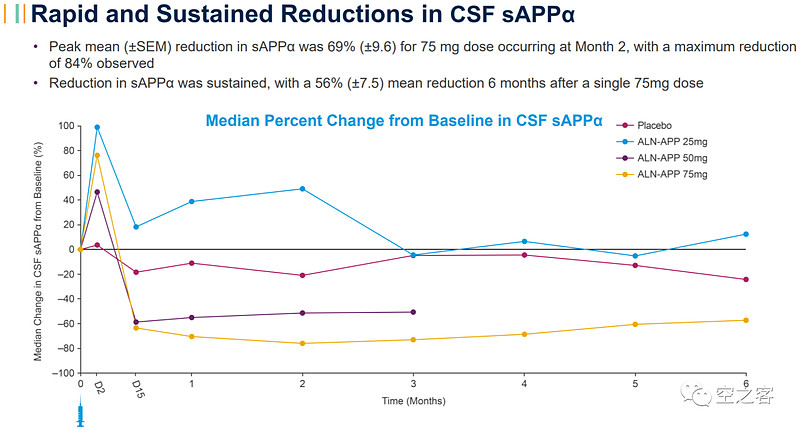
有效性方面,在最高剂量组75 mg的ALN-APP单次给药后,患者脑脊液中的可溶性APPα和可溶性APPβ(sAPPα/β,二者都是ALN-APP靶向结合的生物标志物)出现快速和持续的减少,最大降幅分别为84%和90%,给药后6个月内平均降幅分别为56%和65%。
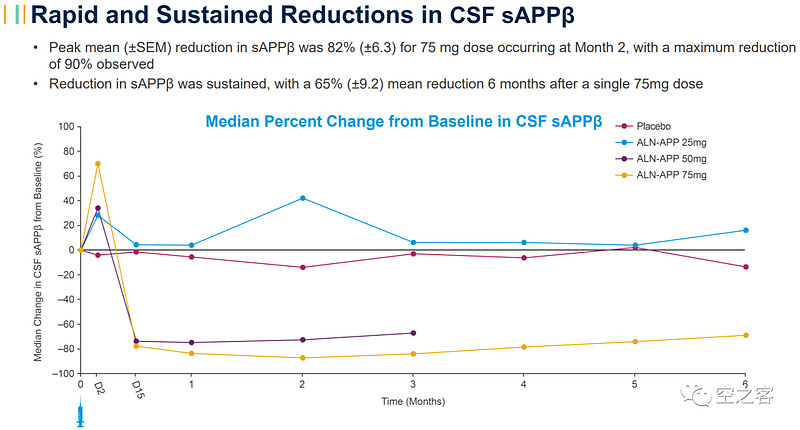
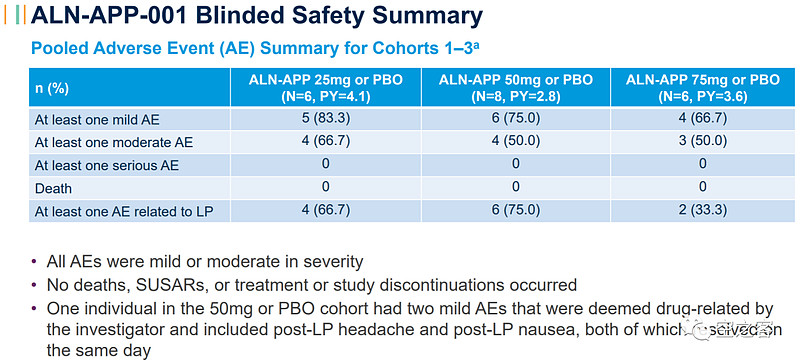
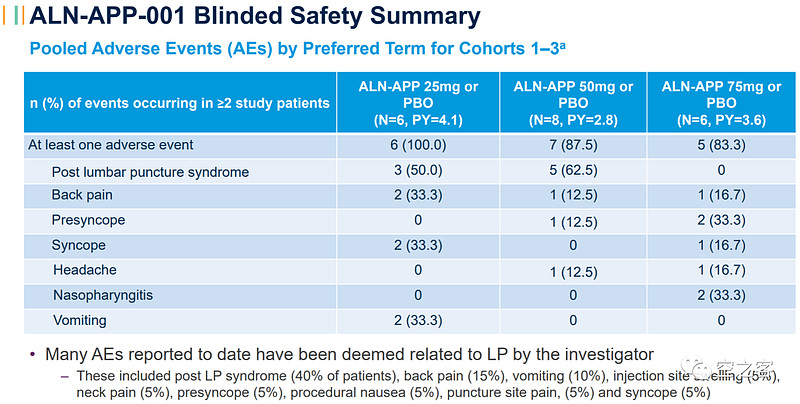
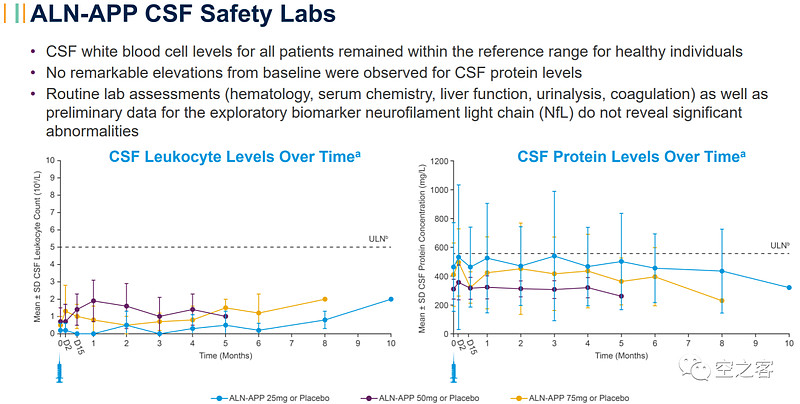
安全性方面,所有AE均为轻中度、未出现SAE或停药现象,CSF内白细胞和总蛋白水平均未较基线显著升高。
ALN-APP不仅给AD患者带来可能更加快速持久的治疗方案,更是Alnylam等RNAi企业迈出了走出肝靶向递送、而走向CNS等星辰大海的关键一步。
3. 当AD遇上RNAi:DTx of Novartis
$诺华制药(NVS)$ 宣布以10亿美元收购一家临床前阶段的RNAi技术平台公司DTx Pharma,包括5亿美元首付款+5亿美元里程碑付款。

该公司的FALCON(Fatty Acid Ligand Conjugated OligoNucleotide)平台是通过将脂肪酸偶联到RNAi上,同样能够更加灵活直接的调节疏水性,从而实现向不同组织的递送。

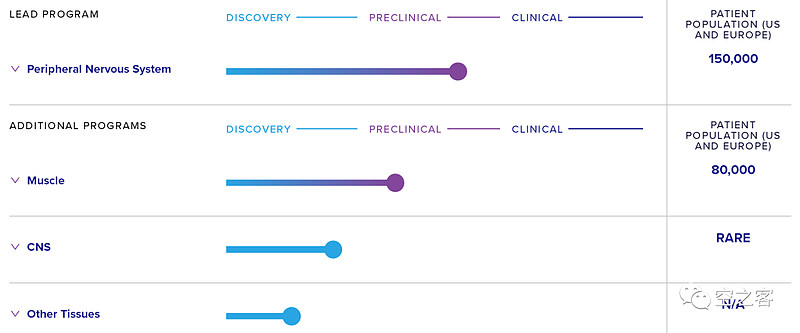
DTx的首个管线DTx-1252靶向PMP22蛋白基因,用于治疗一种神经系统的遗传病1A型腓骨肌萎缩症(CMT1A);后续还有其他治疗肌肉和CNS疾病的关系。
这种黑科技级的脑洞,顶级大药企在非常早期就豪掷10亿下手买断,无疑也是看到RNAi已经开始出现迈向更多疾病领域的切实可能性。
当AD遇上RNAi,是否能够掀起下一轮生物医药的大潮呢?