本周混迹于苏州的药促会和厦门的CSCO,除了由人满为患而引发的医药投资(特别是肿瘤)市场过热的感叹以外,聆听最优秀的这批医生、药企、监管人士的讨论,有些许以前略显模糊的观感日渐清晰,与球友们分享。
直接上结论:在政策、人才、资本的多重利好之下,中国的创新药研发能力近几年在急速追赶国际先进水平,然而现状依然是有巨大代差,而且弯道超车是非常不切实际的幻想,各个环节的能力都还需要相当长时间和相当高成本的积累,才有可能接近和达到全球领先。正如王晓东院士所说,想超车先得把车维修好,而且要在直道上稳健超越,开着破车玩弯道超车很可能就翻车了。
很多医药投资的新手会对新药研发抱有一种过于简化的猜测,好像新药就靠一两个牛逼的科学家拍脑袋想出一个非常好的分子结构就能大杀四方了,殊不知从基础研究、分子设计筛选验证、临床前和临床试验、生产和制剂工艺、注册申报、商业化等各个环节,每一步都是需要大量高水平专业人员密切配合的系统性工程,任何一点疏漏甚至是一些不知从何而来的背运,就会直接让一个本来看起来前景极好的新药品种胎死腹中。
在这个复杂的链条中,中国药企和研究者在最前端和最后端的劣势似乎大家感受应该比较直观:基础研究和基础数据积累明显不及欧美,新机制和新靶点还从来没有由我国研究者提出,像前沿生物的王昌建说到艾博卫泰是“第一个不是由白人做出的艾滋病新药”时,简直是一种令人愉悦的忧伤;注册申报和商业化也明显吃亏,国内市场和监管正在慢慢走出乱象,国际市场基本上还是国际巨头垄断以至于绝大多数中国药企踏上异国还是被迫要走co-marketing的路线。然而在中间的几个环节,似乎往往被投资新手们所忽视,甚至有不少中小型biotech公司也在创业之初大大低估了这些环节的复杂性,以至于事到临头才意识到搞不定这些问题的后果可能是灭顶之灾。
1. 研究立项
国内研究扎堆是有目共睹的现象,几十个PD-1和一大串CAR-T就是非常好的反面教材,出现这种现象一方面是上文所述发现新机制和靶点的能力匮乏,另一方面更直接的原因就是绝大多数开发者在研究立项之初就没有对临床需求进行充分的调研,开发的药物就算能够顺利成药也可能根本不具备市场竞争力。
何谓“临床未满足需求”?说简单一点就是先搞清楚要针对的适应症有多大,现在的标准治疗方案是什么,它的有效性如何、有没有安全性问题、医生和患者的依从度如何。从这一系列问题出发,才有可能判断待开发的新药是否有足够的生存空间。
一个公司在present自己的产品时的思路就很能看出研发立项过程当中所做过的工作,仅举会上看到的一正一反两个例子,未免引战,公司和药品名称就不直接引述了,知道的人自然一眼便知。
正面案例如下,非小细胞肺癌市场是十分拥挤的不假,但MET阳性患者特别是在三代EGFR-TKI药物耐药之后的仍然有很大的空间,而随着NSCLC患者生存期的延迟,这一部分患者对c-MET抑制剂的需求显然尚未被满足。这就是国际国内高水平药企应有的态度和能力,对自己要切入的临床需求非常清晰,这也会直接主导了后续的临床方案设计和商业化策略。
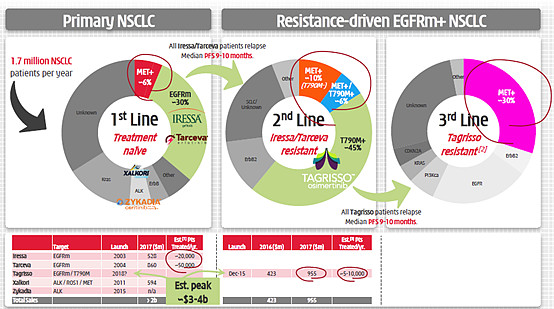
反面案例如下,是XX基公司研发的XXX定,在被CDE退回一次之后继续不折不挠,向着肝癌这个大坑前进。须知肝癌虽然在前几年只有索拉非尼一个获批的一线药物,但在近几年瑞戈非尼、PD-1数据大好,又只有中国市场可做,这时候已经是华山一条路,这次本来还想听听是不是能够真的大力出奇迹、做出什么惊世骇俗的优效结果,然而看到下面这个Phase IIb结果,抱歉我笑了,深深同情来做报告的秦叔逵院长……
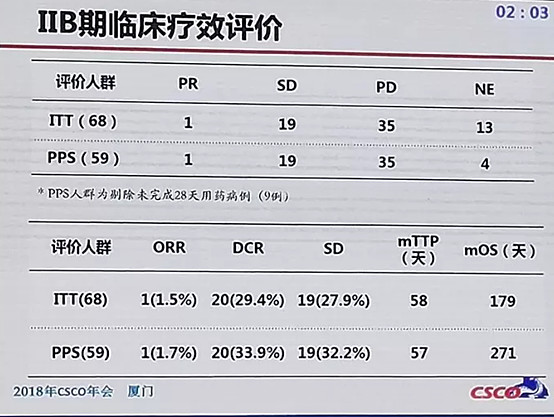
2. 临床试验
临床试验绝不是很多人想象得那样,几个医院开始招几个病人、把药一吃记录一下结果就可以申报了,这周两个会上有大量讨论都集中于临床设计和临床研究能力。
临床方案的设计需要对各线现有治疗方案、潜在竞争对手和商业化难度有非常清晰的认识,加上深厚的生物统计学功底,才可能设计出既能顺利临床推进和注册申报、又能在市场竞争中占得优势的方案。最简单的一些问题包括:选择几线方案,单药还是联用,跟谁对照,Hazard Ratio定在多少,入组多少例……每一个选择既影响最终研发的成功率、又涉及时间和资金的投入,绝不是简简单单不言自明的。
以管窥豹,我们以CDE对安罗替尼用于申报NDA的三期临床试验设计的点评为例加以说明。入组和排除标准中最重要的两条是接受过2种系统性化疗后进展+EGFR/ALK突变型患者需接受过相应TKI治疗,而在对照组选择上由于三线晚期NSCLC没有SOC则使用安慰剂。这种设计放在当时无疑是稳扎稳打的选择,面对NSCLC的巨大市场,不去跟吉非替尼、厄洛替尼、色瑞替尼、克唑替尼这些重磅药刚正面,而借助这些药成功提升患者生存期去抢占耐药后的三线晚期市场,特别是在中国市场进口的EGFR/ALK抑制剂渗透率还不够高的前提下,未来在商业推广中off-label的空间甚至更大。同时CDE也指出了明显的临床设计缺陷,即没有考虑EGFR的T790M突变,虽然这并未阻碍安罗替尼的注册上市,但很显然在三代EGFR TKI奥希替尼上市后的二三线市场竞争中埋下了炸弹。


临床研究能力更是一个看似很边缘的问题,好像医生天然应该会做临床、CRO天然应该搞得定各种临床协调工作,然而事实情况南辕北辙。
随着药企项目数量激增和审评效率提速,临床机构的研究能力几乎已经成为新药研发最主要的瓶颈,我国无论是医院医生还是患者数量都是其他国家难以想象的体量,但真正能够可靠执行临床研究的医院凤毛麟角,以至于在某些拥挤的领域药企对临床中心和PI的竞争早已白热化,很多药企发现虽然名义上很多顶级三甲医院都挂着临床中心,但实际上入组极其缓慢,因为一个医院很可能被迫同时给好几个适应症相同或相近的药做临床,根本没法兼顾。不仅是产能跟不上,在很多技术水平要求较高的临床项目上国内也有较多空白,例如心脏毒性试验很多国内临床机构根本无法执行。造成这种局面的原因一方面是过去国内临床数量质量都太低医生无法得到训练,另一方面是大医院的临床人员激励机制基本是空缺的、无法提供临床能力提升的原动力。值得一提的是,2017年10月8日的两办文件以非常直白的行文方式支持临床试验开展,其中包括“对临床试验研究者在职务提升、职称晋升等方面与临床医生一视同仁”这种大白话实属罕见,看到这种文件一种理解是承认了当前“并不一视同仁”的现实,另一种则是应该可以期待一些实质性激励机制的落地。
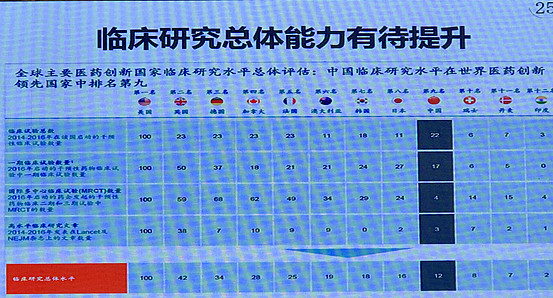
除了临床机构,药企和CRO之间也是麻烦重重,下图是McKinsey做的医药企业对外包服务满意水平的调研,令人莞尔。现在国内新药企业创业者中,真正经历过完整的新药研发全流程的人极其罕见(基本只可能是之前在big pharma里任高级职务的海龟),使得很多企业在进入临床阶段之前对需要考虑的问题一脑袋浆糊,甚至天真地以为只要付钱了就可以撒手不管扔给CRO和医院去执行,直接导致临床研究过程中状况频出甚至直接崩盘。CRO日子也不好过,外资CRO不接地气、国内CRO人员素质和质量体系都跟不上扩张速度,甚至随着药企数量大幅增加,很多CRO刚培养2-3年的CRA可能一转眼就会被药企以翻倍的薪资挖去组建临床团队,结果一大帮半懂不懂的甲方和乙方又开始各种甩锅……
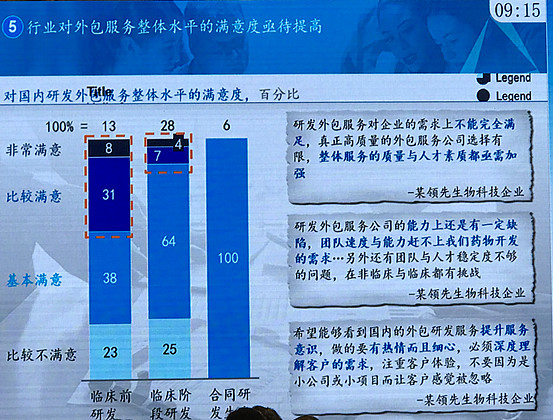
3. 生产和制剂工艺
不仅是投资者,大批新药研发企业也都对CMC问题的严重性估计不足,就不提生物药屡屡出现的拿到生产批件之后生产工艺无法支持商业化批次生产的窘况,就拿化药来说,在CSCO上CDE也专门提出了诸多药学问题。
一个好的新药,化合物分子本身特性固然是有效性和安全性的来源,但最终还是需要制剂来实现商业化,杂质、晶型、粒度、溶出从实验室小试规模到早期临床中试到最终商业化规模,一步步变更都有可能造成参数的改变,而哪一个环节达不到要求再好的分子也会到人体内展现出意想不到的面目。至少在二期临床时就应该采用适合商业化的合成路径和制剂工艺,要考虑好哪些杂质可能有代谢活性、如何降低、粒度是否符合审批要求、扩大规模后生产是否稳定、API和市场成本如何,否则在临床时做出的结果要是到了商业化申报之前发现由于扩大规模工艺变更造成临床的有效性和安全性有变,想想都惨……这种问题可能在经历了华海“杂质事件”后国内企业多多少少能引起一些重视吧。

虽然还有着各种各样层出不穷的问题,国内药企还是给了患者和投资者以巨大的希望,特别是看到头部几家公司已经在不断克服上文所述的一些共性问题,并在全球市场渐露头角,如果未来中国药企的presentation上都能呈现出下图这样的纸面条件,我想至少我们就已经站在世界医药研发第一梯队的门槛上了。
$百济神州(BGNE)$ $恒瑞医药(SH600276)$ $和黄药业(HCM)$
@今日话题