2月25日,百济神州2021年财报业绩,公司实现营业收入约76亿元人民币,同比大增281%。同时,公司净亏损为99.68亿元,同比2020年的117.4亿元净亏损额减少约13亿元,同比收窄13%。
乍一看百济神州接近百亿人民币的亏损额,也许在大部分不明就里的投资者眼中,绝对是难以想象的。但客观来看,2021年百济神州全年研发费用约95亿元(同比增长15%),净亏损的金额与研发费用已经十分接近,亏损相比往年已经下降13%。而大规模投入研发,这恰恰体现了公司有着全球创新药领军企业的觉悟,开足马力聚焦药物创新。
以百济神州2021年近百亿的研发投入体量,其已经是名副其实的“创新药研发一哥”,“老大哥”恒瑞医药2021年前三季度的研发费用也只是41.42亿。
01
直面商业化能力拷问:百济交出惊艳2021成绩单
百济神州作为一家立志于成为全球Big Pharma的创新药企业,无疑承载了太多投资者的厚望。但希望有时候会加剧焦虑,由此部分市场投资者对于百济神州的商业化能力也产生了不少的质疑、诟病,如果从创新药领域“双十定律”的客观规律来看,成立11年多的百济神州,真正的商业化征程和成长曲线,才刚刚开始。
百济神州的这份2021年成绩单,不仅粉碎了市场对公司全球化战略和商业化能力的质疑,同时我们也看到非常多超出预期的数据。
百济神州的营收由产品销售收入和合作授权收入两大部分组成,2021年公司产品收入、合作收入分别为40.9亿元、34.99亿元。
最值得注意的是公司商业化产品放量带来的收入增长,2021年百济神州产品收入为40.9亿元,同比实现翻倍增长。产品端收入的爆发式增长,泽布替尼和替雷利珠单抗两大主力产品功不可没。
2021年,首个出海新药BTK抑制剂泽布替尼全球累计销售额约14亿元,同比增长423%,在中、美两国的快速放量是销量快速放大的主因。2021年美国收入7.46亿元,同比大增535%;2021年中国销售收入6.52亿元,同比增长331%。
这也只是泽布替尼的起点,百济神州已经通过一项头对头三期研究,证明了泽布替尼同类最优BTK抑制剂的“帝位”,要知道被PK掉的伊布替尼全球销售峰值超过80亿美元。目前泽布替尼在国际上获批的国家及地区多达45个,随着泽布替尼更多新适应症全球各个地区获批,相信未来销售会进一步放量。
相较于泽布替尼的稳健,市场更关注的或许是PD-1替雷利珠单抗。在国内医保谈判的降价压力下,2021年替雷利珠单抗在国内销售额仍然实现了良好的增长,全年累计销售额约16亿元,同比增长56%。
由于向美国递交的新药上市许可申请要到2022年7月才会有最终结果,虽然这是一项重要的全球化里程碑,但2022年替雷利珠单抗收入的主要市场看点仍在国内。2021年底的医保谈判,替雷利珠单抗治疗非鳞状非小细胞肺癌等3项新增适应症被纳入医保,使得替雷利珠单抗超越恒瑞医药、君实生物、信达生物,成为纳入医保目录适应症最多的PD-1产品,这无疑给替雷利珠单抗的放量和超车竞争对手装上了强力加速器。
截至2021年底,百济神州的商业化产品组合已增加至16款之多,其中除上述两款产品外,PARP抑制剂帕米帕利胶囊在2021年5月在国内获批上市且同年被纳入医保目录,而百济神州分别从BMS和安进引进的多款商业化产品2021年也实现了良好的销售增长,如根据美股2021年财报披露,安进授权的一揽子产品国内销售额从2020年的850万美元提升至5880万美元。
自2019年11月百济神州第一款自主研发产品泽布替尼获批,2021年实际只能算公司走上商业化道路的第二个年头,这个成绩已然算不错。随着百济神州核心管线海外审批预期进一步兑现,未来业绩有望呈现爆发式增长。
02
拒绝“捷径”&踏实做MRCT,百济全球化战略稳如磐石
2月10日,信达生物PD-1信迪利单抗被FDA拒绝批准,令国内一众梦想凭借me-too管线出海掘金的Biotech心生寒意。
据人民日报数据统计,近一年来有17款产品被FDA拒绝,其中不乏默沙东、礼来等MNC的身影,总结下来有四大原因:安全性数据存疑、患者临床数据单一、临床获益不够明显、生产设施存在缺陷。
尽管作为最快报批FDA的两款国产PD-1之一,信达生物的PD-1信迪利单抗的BLA更像一场豪赌。而目前,君实生物和百济神州的PD-1仍在等待审批中。百济神州在全球研发布局上一贯是稳扎稳打,坚定地执行全球多中心临床的策略,通过扎实细致的临床研究、高质量的数据规避“雷”,因此替雷利珠单抗是出海美国确定性最高的国产PD-1之一。这背后,既是对全球市场规则的深刻理解,也源自对自身发展策略的差异化定位。
资料显示,替雷利珠单抗针对食管鳞癌在美国FDA的BLA申请是基于一项全球三期临床结果,该试验纳入了512例来自亚洲、欧洲、北美的11个国家或地区的患者,近40%的患者是在中国以外招募,其中也覆盖了美国多个临床试验中心,保证了临床患者的多样性。
一款新药的研发,其中75%-90%的开发成本都在临床项目阶段。
百济神州深谙临床研究对一款药物的重要性,通过全球范围内的广泛布局,已构建起公司自主执行全球临床运营的能力,可高效地推进包括中国在内的全球临床试验。截至2021年底,百济神州在超过45个国家和地区执行超过100项计划中或正在进行的临床试验,包括38项3期或潜在注册可用的临床试验,总入组患者及健康受试者超过14500人,其中海外入组接近半数。
凭借着强大的全球化临床团队,百济神州也达成了国内99%创新药企尚未曾想象的成就。
百济神州的泽布替尼是全球唯一一款在针对两项血液恶性肿瘤的治疗中,开展头对头临床试验以评估疗效和安全性的BTK抑制剂,是国内首个与进口药物开展头对头三期优效性试验的抗癌新药。同时,百济神州也在全球开展了大量的临床试验,如泽布替尼目前全球入组患者已达到约4000人。替雷利珠单抗目前正在全球35个国家地区开展约50项临床试验,入组受试者超过9000人,其中近3000人来自海外入组。
这也能够解释,百济神州为何能够不断刷新国内创新药的License out记录。这离不开公司前瞻性自建了强大的前端发现、临床、商业化团队,不依赖于CXO,使得从百济神州能够在药物发现之初致力于自主开发最优的分子,同时全球化的临床开发和商业化团队能够挖掘出药物的最大价值。
03
无惧生物医药融资寒冬,“中国研发一哥”收获期将近
2022年的春天似乎格外寒冷,由于医药生物上市公司市值持续下行,倒挂效应使得Biotech在一级市场的融资变得格外困难。据医药魔方数据显示,无论是数量还是金额,2022年2月份同比减少2/3,环比2022年1月减少1/2。
越来越多的Biotech开始关注自身现金储备的问题,它们同时也面临来市场的质疑和拷问:是否有足够现金流支撑到在研管线上市商业化?现有管线价值能否持续吸引到新的融资?
而百济神州还没有这样的烦恼。
截至2021年12月31日,百济神州的现金和现金等价物、限制性现金和短期投资总额合计约合人民币418亿元(不包括于2022年1月授权诺华TIGIT单抗的3亿美元预付款)。这意味着,即便百济神州连续三年保持如2021年高强度的研发投入,光是现金储备即可支撑,同时还没考虑到公司逐年增长的产品商业化收入和大额授权合作分成。
从另外一个层面看,百济神州作为A+H+N三地上市的生物医药公司,同样可以通过多地市场再融资快速补充现金流。
百济神州十年如一日的高强度创新研发投入,使得其构建起了多元化的前沿新药技术平台,包括高通量筛选,虚拟筛选、化学激活的降解技术CDAC、功能基因组技术、免疫激活ADC和杀伤型ADC等,丰富的研发“工具箱”是公司产出爆款药物的利器。
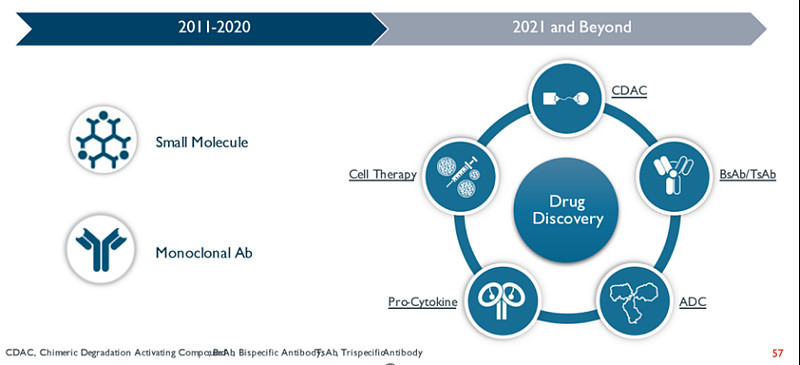
同时,凭借着大约700名科学家组成的全球临床前研究团队,百济神州的研发策略也在快速迭代,以公司管理层的话来说就是从fast follow、best in class的1.0时代,升级到first in class的2.0时代。
目前,公司构建了涵盖50项处于临床阶段的管线梯队,除了BTK、PD-1、PARP成功商业化的产品外,多款具备差异化的在研管线已经或将陆续进入关键性临床,包括TIGIT,Bcl-2,PI3Kδ,OX40,HPK-1,TIM3等。另外部分核心管线研发进度也处于全球前列,如TIGIT抗体欧司珀利单抗,是全球第三款进入三期全球临床阶段的TIGIT抗体,位居全球第一梯队前列。
如果说可以从处于临床研发阶段的产品管线窥探一家创新药企在短期3-4年的走向,那么临床前项目的储备则是决定了其5-10年的长远发展。
目前,百济神州的临床前项目超过50项,其中约有一半具备Fist-in-class潜力,10多个项目将在未来24个月中进入临床阶段。
如果说在研管线是百济神州手里正在发芽的种子,市场投资者更希望看到树上结的果子,百济神州商业化管线多个重大里程碑将在今年密集兑现。
据2021年财报预计,2022年百济神州将更新泽布替尼在一项全球头对头关键性试验中的结果数据,将实现泽布替尼在海外针对慢性淋巴细胞白血病(CLL)适应症的批准,并计划新增在另外10多个国家获批;另外,PD-1替雷利珠单抗在FDA的首个上市申报的目标决议时间为7月12日,有望在今年实现首次出海...
未来随着公司越来越多在研管线的License out以及商业化管线的放量,“中国研发一哥”将羽翼丰满,在全球各地展翅翱翔。
结语:素来生物医药市场对于百济神州式“高投入、高亏损”发展模式争议颇多,也经常被人拿来与恒瑞医药进行比较。
在我看来,两者实际上是“攻守之道”的代表,相信两者未来都能取得成功,但时间、路径的差异一定是巨大的。
百济神州从成立之初就立志成为全球化的Big Pharma,坚定贯彻“高举高打”、全球化布局的战略,是无比进取的,而这种独一无二的发展路径,后来者几乎很难复制。
最后,立足百济神州现有成果和趋势来看,这条路是一条康庄大道,而公司正越走越顺畅。
(来源:瞪羚社)