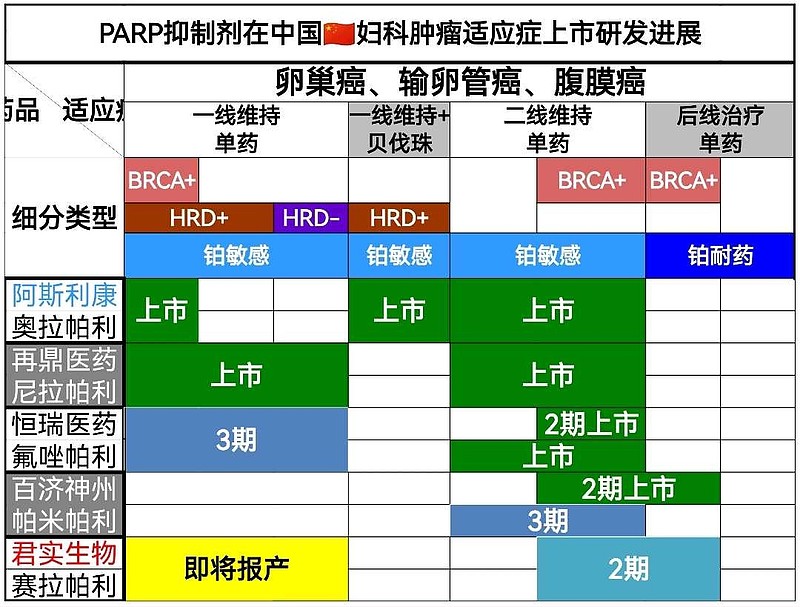
$再鼎医药(09688)$ 披露2022年报告,PD-1(默沙东K药)联合尼拉帕利(PARP抑制剂)治疗实体瘤#国际多中心3期临床# 进行中。
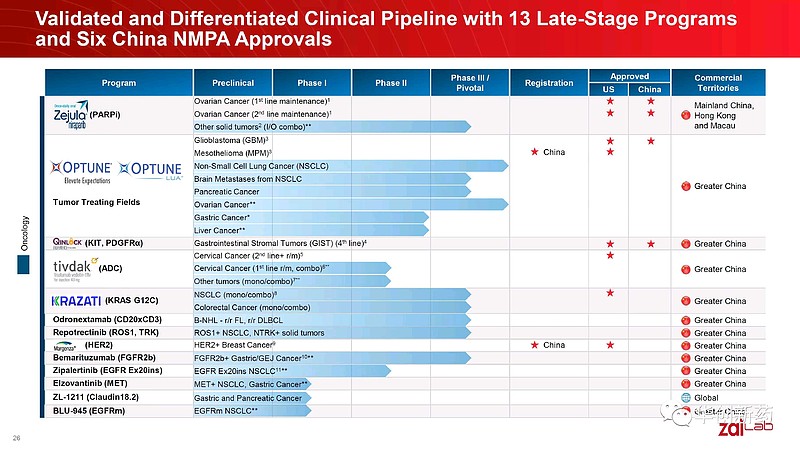
联合治疗的理论基础,
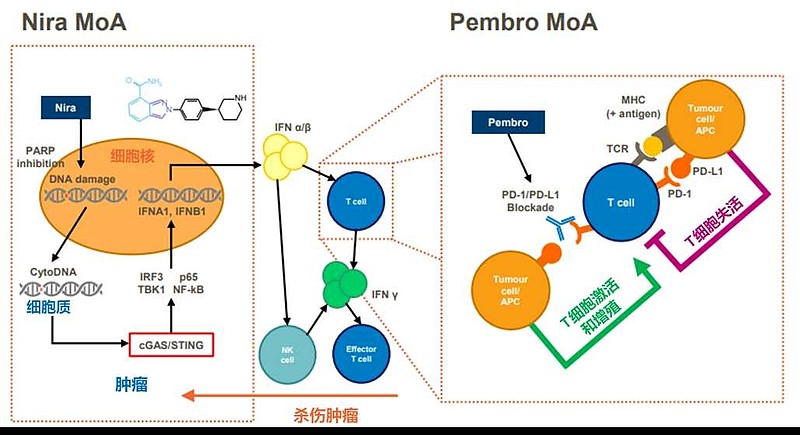
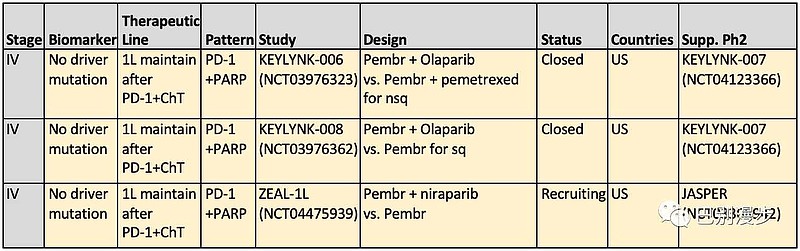
ZEAL-1L研究,国际多中心3期临床试验,一线治疗非小细胞肺癌,治疗方案设计。
招募开始于2020年11月。
一线治疗诱导,PD-1+含铂化疗,6个周期,
序贯,
一线治疗维持,PD-1+PARP,16个周期,一年时间。
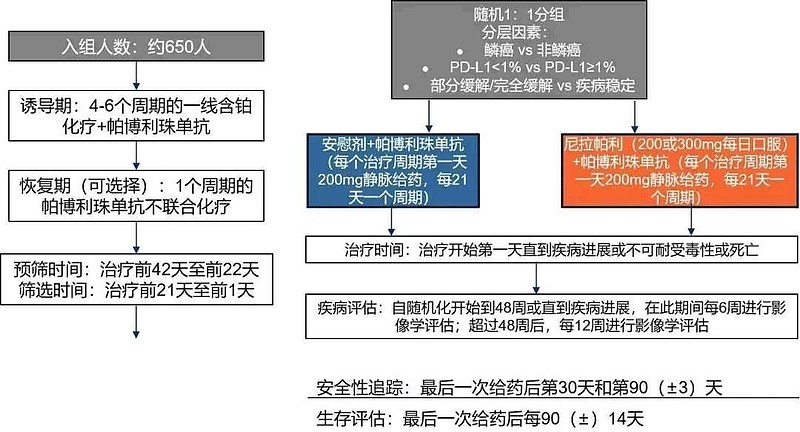
ZEAL-1L研究的依据是,Jasper研究2期临床数据。
发表在《Annals of Oncology》的JASPER研究,旨在评估尼拉帕利联合PD-1单抗一线治疗晚期NSCLC的疗效和安全性。
研究的入组标准为未经化疗的局部晚期/转移性NSCLC患者,EGFR敏感突变/ALK/ROS1重排阴性。既往未接受PD-(L)1治疗的患者按照PD-L1 TPS分层:≥50%(1队列),1%~49%(2队列)。
患者每3周静脉注射帕博利珠单抗200 mg,每日口服尼拉帕利200 mg。主要终点是研究者评估的客观缓解率(ORR)。次要终点为(在mITT中评估)缓解持续时间(DoR)、无进展生存率(PFS)和安全性(服用≥1剂研究药物的患者)。
1队列和2队列分别纳入17例和21例患者,最终意向治疗人群中,1队列和2队列分别有16例和20例患者。
1队列ORR为56.3%,其中2例完全缓解。2队列ORR为20%。中位DoR分别为19.7个月和9.4个月,两队列的中位PFS分别为8.4个月和4.2个月。
最常见的3级及以上治疗相关不良事件(两个队列均>10%)包括贫血(1队列24%,2队列29%)、肺炎(24%,14%)和乏力(12%,14%)。
因此,尼拉帕利+帕博利珠单抗可为晚期NSCLC患者带来持久缓解,在PD-L1高表达人群中疗效更显著。该联合用药方案未出现新的安全性事件。
需要注意
keynote024研究,PD-L1 TPS≥50%,帕博利珠单抗单药的中位PFS=7.7个月,ORR=46.1%。
keynote042研究,PD-L1 TPS≥50%,帕博利珠单抗单药的中位PFS=6.5个月,ORR=39.1%。
中国Biotech创新药企,拥有PARP抑制剂产品的,
包括$君实生物-U(SH688180)$ ,$百济神州-U(SH688235)$ ,恒瑞医药,再鼎医药。