前文
$君实生物-U(SH688180)$ VV116在中国🇨🇳获批上市,甚至还要在美国🇺🇸获批上市,需要像唐僧取经那样,#经历九九八十一难# ,才可以修成正果 。
(一)瑞德西韦的5项国际多中心关键注册临床试验
如同吉利德科学的瑞德西韦,开展了5项全球3期关键注册临床试验,①ACTT-1研究,NCT04280705,双盲头对头对照,降低吸氧新冠患者死亡率。②ACTT-2研究,NCT04401579,双盲头对头对照,联合用药增强瑞德西韦疗效。③SIMPLE-Severe研究,NCT04292899,开放标签,降低新冠重症患者死亡率。④SIMPLE研究,NCT04292730,开放标签,改善新冠中症患者临床症状。⑤PINETREE研究,NCT04501952,双盲头对头对照,降低新冠轻症患者住院率。

(二)超适应症用药
另外,辉瑞口服药Paxlovid虽然在#未接种疫苗的高风险患者# 开展3期临床试验成功,但是并不影响给予美国🇺🇸拜登(已经接种4剂新冠疫苗)口服药物治疗,也不属于超适应症用药。
(三)瑞德西韦的中国3期临床试验,为什么失败了?
有些小朋友会问了,为什么2020年临床数据发表在《柳叶刀》的瑞德西韦中国🇨🇳3期临床试验失败了?
这项瑞德西韦的中国3期临床试验登记号:NCT04257656。中日医院副院长曹彬教授和 #北京协和医学院# (中国医学科学院)校长 @王辰 院士领导的瑞德西韦临床试验结果——失败了。
这是一项随机、双盲、对照临床,选取的病人都是重症患者,血氧饱和值<94%,都是需要吸氧的。
该研究共入组了236例(瑞德西韦组158例,安慰剂组78名例)来自武汉10家医院的重症COVID-19成人住院患者。研究的主要终点是直到第28天的临床改善时间。(研究设计初期计划入组重症患者453例,最后纳入患者数量236例,比原定目标明显减少。)
临床试验的结果是:瑞德西韦vs安慰剂,HR=1.23,临床改善时间=21天vs23天。无显著差异,P值=0.24。统计学不显著。第28天死亡率=瑞德西韦组14%vs安慰剂组13%。
临床设计出现了哪些问题一步一步看:
问题一:样本量太小,对照组仅79人,试验组仅158人,
问题二:两组的基线状态并不平衡:在瑞德西韦组里有基础性疾病并发症的群体远远超过>安慰剂对照组:
瑞德西韦组高血压患者占比46%,对照组仅38%。
瑞德西韦组糖尿病患者占比25%,对照组21%。
瑞德西韦组心血管疾病占比9%,对照组仅占比3%。
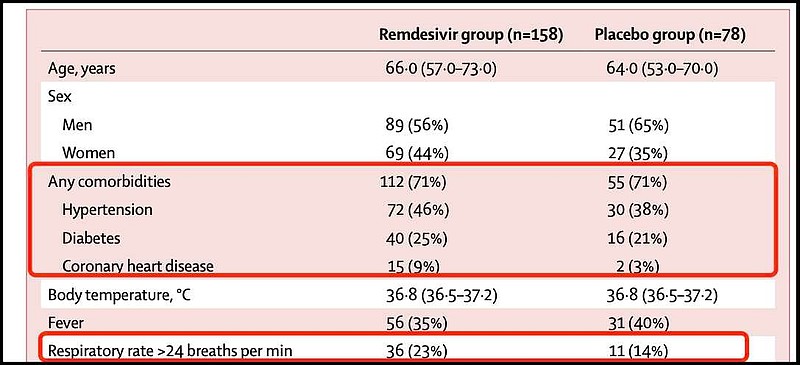
最夸张的在于呼吸频率!
瑞德西韦组喘气过快的患者占23%,对照组仅占14%。嗯……都快差一倍了。
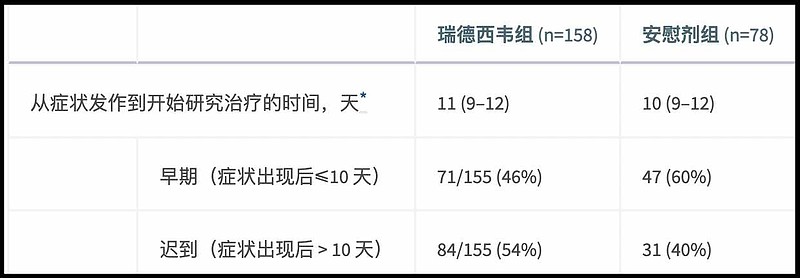
瑞德西韦组早期患者占46%,对照组早期患者占60%,瑞德西韦组晚期患者占了多数……
综上所述,不难看出,瑞德西韦组入组的病人严重程度远远超过对照组,几声叹息!
在入组前患者差别这么大的情况下,我们仍然看到了很多的亚组数据有改善趋势:
比如对于早期患者(症状出现10天内治疗组),症状恢复中位时间=瑞德西韦组18天vs安慰剂组23天,HR=1.52,95%CI=0.95 to 2.43,数据相当好,相当于节省了将近一周时间的治疗,可以避免医疗挤兑。
在有创机械通气(呼吸机治疗)的亚组,中位恢复时间是瑞德西韦组7天vs安慰剂组15.5天,其中幸存者的有创中位通气时间是瑞德西韦组19天vs安慰剂组42天,两组数据差别非常大。
所以,中国🇨🇳3期临床瑞德西韦没有统计学显著差异,根本原因就在于——入组患者数量太少+间接导致两组患者基线状态不平衡。
总结
君实生物VV116就是瑞德西韦的me-better创新药,在VV116治疗新冠重症国际多中心3期临床招募入组600例患者,在VV116治疗新冠轻症国际多中心3期临床招募入组2000例患者。
就是吸取了……前车之鉴的教训。