(一)VV116究竟是瑞德西韦口服版? 还是me-better创新药?
$君实生物-U(SH688180)$ 散户股东从公开宣传了解到,VV116——由中国科学院早期研究——由君实生物负责中国和海外研发+商业化。
由于VV116是通过氘代、酰化等设计,获得了新的母体核苷结构和药物分子结构。新的分子结构展现了和瑞德西韦不同的药代动力学特征,规避了瑞德西韦注射繁琐、肝毒性等弊端。从而成为可口服,且无明显肝毒性的新冠口服候选药物。
VV116的母体核苷名为116-N1,与瑞德西韦母体核苷GS-441524非常相似,区别在于116-N1在吡咯并三嗪(pyrrolotriazine)上引入了氢的同位素氘。由于GS-441524容易遭到酶类通过双键氧化和三嗪开环的方式降解,氘代有潜力带来药代动力学的优化。
要判断一个潜在药物的价值,主要是看它的半最大效应浓度(EC50)。一般来说,EC50越小越好,表明可以在很低的浓度就能起到作用。116-N1的EC50约0.39 ± 0.08 μM,GS-441524的EC50为0.59μM。
所以,VV116是me-better创新药。
当然,有些行业大佬认为,VV116就是瑞德西韦口服版。
请忽略图片内容,重点在文字。

(二)全球开展了7项瑞德西韦III期关键注册临床试验,有哪些大型临床研究成功了?
①ACTT-1研究,NCT04280705,双盲头对头对照,降低吸氧新冠患者死亡率
瑞德西韦vs安慰剂,与安慰剂相比,29天中位恢复时间=瑞德西韦组10天vs安慰剂组15天,P值<0.001。
从总体上看,瑞德西韦组和安慰剂组患者的死亡率在第15天分别为6.7%和11.9%(HR,0.55;95% CI,0.36-0.83),第29天分别为11.4%和15.2%(HR, 0.73;95% CI,0.52 -1.03),均表现出下降的趋势(没有获得统计学显著差异)。
但是,需要吸入低流量氧气的患者(队列5)亚组,获益最大,接受瑞德西韦治疗的此类患者在第15天的死亡率为3.1%,比安慰剂组的10.5%降低了72%( HR,0.28;95% CI,0.12-0.66);在第29天获益趋势仍得到了很好的保持,两组的死亡率分别为4%和13%,瑞德西韦组的死亡率降低了70%(HR,0.30;95% CI,0.14-0.64)。
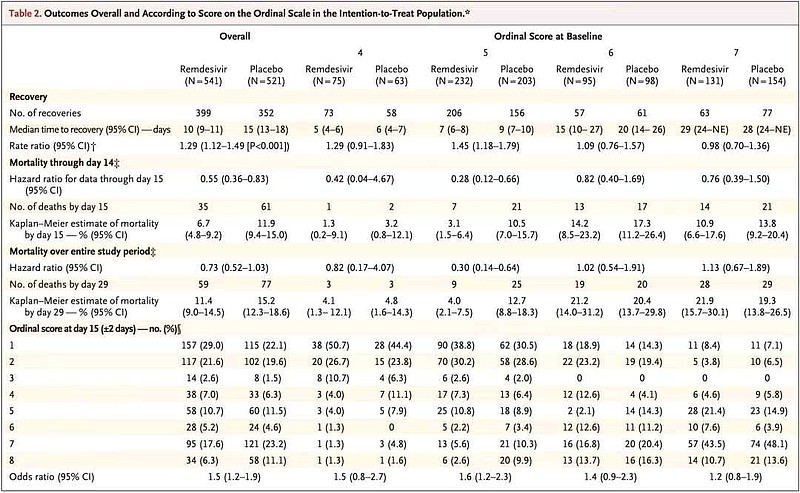
瑞德西韦,获得美国🇺🇸FDA批准(EUA,紧急使用批准)新增——新冠重症适应症。
君实生物VV116今年3月启动了治疗中重度COVID19的国际多中心、随机、双盲、对照III期临床研究(NCT05279235),目的是在国际多中心(上海公卫中心、乌兹别克斯坦第二传染病专科医院)的中重度COVID-19受试者中确证性评价VV116对比标准治疗(法匹拉韦)的有效性和安全性,主要终点为截至第29天进展为(危)重型COVID-19或全因死亡的受试者百分比。
计划于2022年7月30日完成III期临床。

②ACTT-2研究,NCT04401579,双盲头对头对照,增强瑞德西韦疗效
瑞德西韦+巴瑞替尼vs瑞德西韦,中位康复时间=联合用药组7天vs瑞德西韦组8天,P值=0.03。
瑞德西韦+巴瑞替尼,联合用药获得美国🇺🇸FDA批准新增——新冠重症适应症。
③SIMPLE-Severe研究,NCT04292899,开放标签,#降低新冠重症患者死亡率#
这项研究认为瑞德西韦10天用药与5天用药效果不显著。与安慰剂相比,14天死亡率=7.6%vs12.5%,P值<0.001。28天死亡率可降低54%(HR:0.46,P值<0.001)。
需要注意, ACTT-1研究(双盲对照试验),显示治疗29天瑞德西韦不能显著降低全部人群死亡率,只是有降低趋势。
根据这项开放标签,而不是双盲对照试验,瑞德西韦被美国🇺🇸FDA完全批准用于新冠重症。
这里需要提醒朋友们,那些大威说,君实生物VV116 vs 辉瑞Paxlovid头对头对照上海多中心单盲试验,证据级别不足的,可以思考一下。
究竟是中国🇨🇳单盲头对头试验证据级别效力高,还是美国🇺🇸开放标签(与安慰剂对照)试验证据级别效力更高?
④SIMPLE研究,NCT04292730,开放标签,#改善新冠中症患者临床症状#
SIMPLE研究第二项研究(临床试验设计中途更改),中度(血氧饱和度>94%)新型冠状病毒肺炎住院患者,接受瑞德西韦5日疗程的患者在第11天时更易出现临床改善,且改善相比较于标准治疗组高出65%。临床试验成功。
⑤PINETREE研究,NCT04501952,双盲头对头对照,#降低新冠轻症患者住院率#
这项随机、双盲、安慰剂对照试验旨在评价瑞德西韦在症状出现7天内治疗高危COVID-19患者的有效性。高危人群指至少有一个危险因素的COVID-19患者(年龄≥60岁、肥胖或有慢性合并症) ,而且招募入组患者没有接种疫苗。
患者被随机分入瑞德西韦组(第1天200mg iv,第2和3天100mg iv)、或安慰剂组。平均年龄为50岁,47.9%的患者为女性,糖尿病61.6%、肥胖55.2%和高血压47.7%。
瑞德西韦组有2名患者因COVID-19住院,安慰剂组有15人住院(住院/死亡风险比 0.13;P值=0.008)。瑞德西韦组和安慰剂组分别有4名患者和21名患者28天内再次就诊(疾病进展风险比 0.19)。没有记录到28天内死亡的病例。
根据这项研究,2022年,瑞德西韦被美国🇺🇸FDA批准用于新冠轻中症、非住院、高风险患者。
(1)NCT05341609 研究是一项中国上海多中心、单盲、随机、对照 III 期临床研究,旨在评价君实生物VV116 对比辉瑞口服药奈玛特韦片/利托那韦片( Paxlovid)用于轻中度 COVID19 患者早期治疗的有效性和安全性。
这里需要提醒朋友们,那些大威说,君实生物VV116 vs 辉瑞Paxlovid头对头对照上海多中心单盲试验,没有降低死亡率/重症发生率,证据级别不足的,可以思考一下。
瑞德西韦的临床试验成功,依据的是——降低住院率,而不是降低死亡率。
(2)NCT05242042 研究是一项中国内地、中国HK(计划招募患者包括东南亚国家)国际多中心、双盲、随机、安慰剂对照、II/III期临床研究,旨在评估君实生物VV116对比安慰剂在轻度至中度COVID-19患者早中期治疗的疗效、安全性和药代动力学。
计划招募入组2000例,计划于2022年12月15日完成。
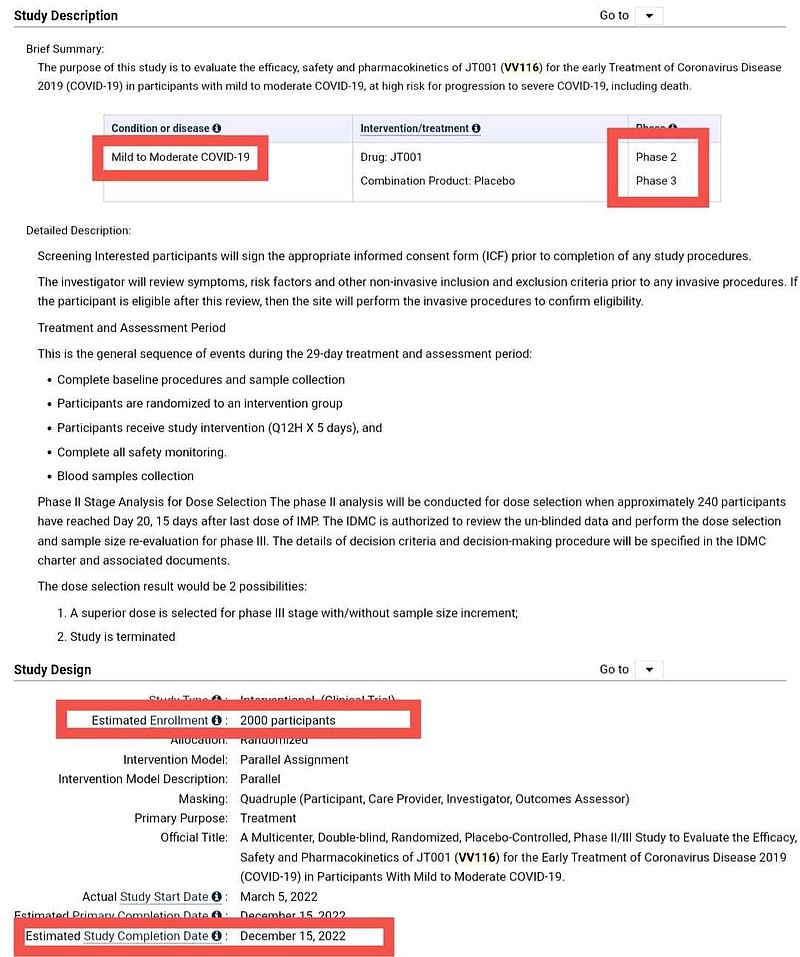
(三)瑞德西韦开展了新冠患者全部人群的关键注册临床试验,全部达到主要临床终点。瑞德西韦是——美国🇺🇸适应症应用最广泛的新冠药物。
从轻症、中症、重症每个种类新冠患者的临床症状不同,设置不同的主要临床试验终点,是国际惯例。
根据真实生物阿兹夫定的新闻稿,阿兹夫定只是改善临床症状,降低病毒载量,所以中国🇨🇳NMPA仅仅批准了——新冠普通型适应症。
阿兹夫定没有降低死亡率,就不能批准治疗新冠重症。
阿兹夫定没有降低住院率,就不能批准治疗新冠轻症。
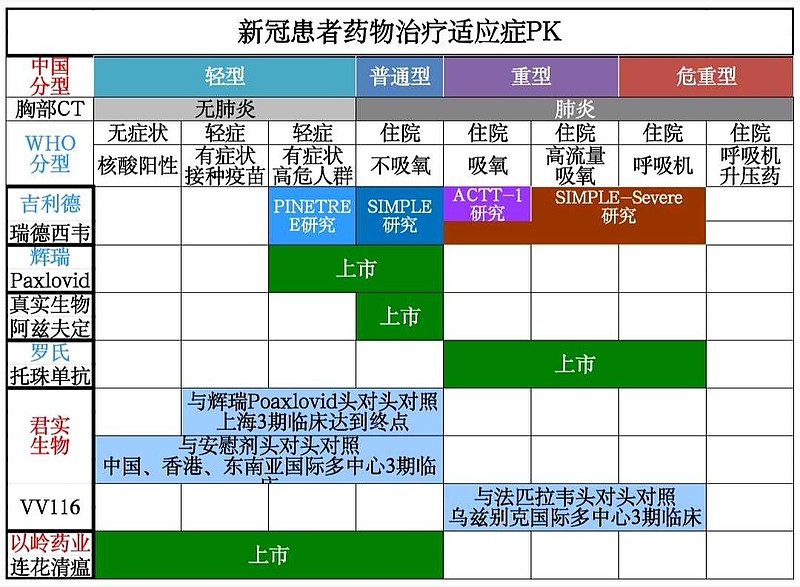
瑞德西韦成功完成了新冠轻症、普通型、重型、危重型5个关键注册临床试验,所以美国🇺🇸FDA批准瑞德西韦注册了‘‘新冠患者全部人群适应症(包括成年人和儿童)’’。
总结
根据瑞德西韦的临床试验设计+关键注册临床数据,君实生物VV116可能实现——青出于蓝而胜于蓝。
转发,$复星医药(SH600196)$ ,$华润双鹤(SH600062)$ ,新华制药,沃森生物,信达生物,恒瑞医药
@今日话题 @水里望月 @生煎只爱大壶春 @柳叶刀找脊梁 @招财小黄鸭 @Rich_李唐 @startan @北京栗男 @炒股南瓜侠 @亥m2c @大个的鼹鼠 @云火锅